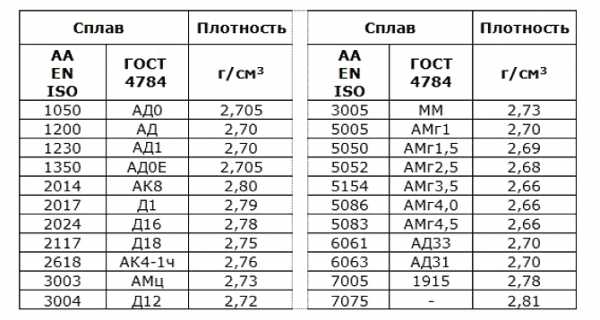
Физические и химические свойства металлов. Основные физические свойства металлов
Физические и химические свойства металлов
Различают технологические, физические, механические и химические свойства металлов. К физическим относят удельный вес, цвет, электропроводность. К характеристикам этой группы относятся также теплопроводность, плавкость и плотность металла.
К механическим характеристикам относят пластичность, упругость, твердость, прочность, вязкость.
Химические свойства металлов включают в себя коррозийную стойкость, растворимость и окисляемость.
Такие характеристики, как «жидкотекучесть», прокаливаемость, свариваемость, ковкость, являются технологическими.
Физические свойства
- Цвет. Металлы не пропускают свет сквозь себя, то есть непрозрачны. В отраженном свете каждый элемент обладает своим собственным оттенком – цветом. Среди технических металлов окраску имеет только медь и сплавы с ней. Для остальных элементов характерным является оттенок от серебристо-белого до серо-стального.
- Плавкость. Эта характеристика указывает на способность элемента под воздействием температуры переходить в жидкое состояние из твердого. Плавкость считается важнейшим свойством металлов. В процессе нагревания все металлы из твердого состояния переходят в жидкое. При охлаждении же расплавленного вещества происходит обратный переход – из жидкого в твердое состояние.
- Электропроводность. Данная характеристика свидетельствует о способности переноса свободными электронами электричества. Электропроводность металлических тел в тысячи раз больше, чем неметаллических. При увеличении температуры показатель проводимости электричества снижается, а при уменьшении температуры, соответственно, повышается. Необходимо отметить, что электропроводность сплавов будет всегда ниже, нежели какого-либо металла, составляющего сплав.
- Магнитные свойства. К явно магнитным (ферромагнитным) элементам относят только кобальт, никель, железо, а также ряд их сплавов. Однако в процессе нагревания до определенной температуры указанные вещества теряют магнитность. Отдельные сплавы железа при комнатной температуре не относятся к ферромагнитным.
- Теплопроводность. Эта характеристика указывает на способность перехода тепла к менее нагретому от более нагретого тела без видимого перемещения составляющих его частиц. Высокий уровень теплопроводности позволяет равномерно и быстро нагревать и охлаждать металлы. Среди технических элементов наибольшим показателем обладает медь.
Металлы в химии занимают отдельное место. Наличие соответствующих характеристик позволяет применять то или иное вещество в определенной области.
Химические свойства металлов
- Коррозийная стойкость. Коррозией называют разрушение вещества в результате электрохимического или химического взаимоотношения с окружающей средой. Самым распространенным примером считается ржавление железа. Коррозийная стойкость относится к важнейшим природным характеристикам ряда металлов. В связи с этим такие вещества, как серебро, золото, платина получили название благородных. Обладает высокой коррозийной сопротивляемостью никель и прочие цветные металлы. Черные металлы подвержены разрушению быстрее и сильнее, нежели цветные.
- Окисляемость. Эта характеристика указывает на способность элемента вступать в реакцию с О2 под влиянием окислителей.
- Растворимость. Металлы, обладающие в жидком состоянии неограниченной растворимостью, при затвердении могут формировать твердые растворы. В этих растворах атомы от одного компонента встраиваются в кристаллическую решетку другого составляющего только в определенных пределах.
Необходимо отметить, что физические и химические свойства металлов являются одними из основных характеристик этих элементов.
fb.ru
Общие физические свойства металлов
Металлические элементы занимают преимущественно левую нижнюю часть Периодической системы химических элементов Д. И. Менделеева. К металлических элементов относятся те элементы, в чьих атомах на внешнем электронном уровне находится небольшое (от одного до четырех) число электронов, атомы могут легко отдавать.
Металлы имеют ряд общих физических свойств:
- Хорошую электропроводность;
- Хорошую теплопроводность;
- Металлический блеск;
- Хорошую пластичность (ковкость)
- Обычно высокую твердость;
- Чаще всего находятся в твердом агрегатном состоянии.
О принадлежности вещества к металлам нельзя судить только по одному признаку. Так, некоторые неметаллы могут проводить электрический ток (графит), имеют металлический блеск (йод), имеют пластичность (пластическая сера). Таким образом, относить ту или иную простое вещество к металлам или неметаллов можно только по совокупности признаков. Общие физические свойства металлов (электропроводность, теплопроводность, блеск и т.д.) объясняются наличием подвижных электронов, иначе говоря, особым характером металлического связи. 0днако различные металлы все-таки имеют различные физические свойства, такие как температура плавления, плотность и т.д.. Эти свойства во многом зависят от кристаллических структур металлов.
Благодаря металлической связи отдельные слои в кристаллах металлов могут смещаться относительно друг друга. Это придает металлам пластичности (ковкости) - способности изменять свою форму без разрыва химических связей. Например, наиболее ковкой металлом является золото - с 1 г золота можно вытянуть проволоку длиной 2,4 км и толщиной в несколько раз меньше толщины волоса. Вместе металл труба очень хрупкий - его даже можно растирать в порошок в ступке.
0скилькы различные металлы имеют сходные металлические связи, а в ряде случаев образуют подобные металлические кристаллы, то многие из них при переходе в расплавленное состояние могут смешиваться друг с другом, образуя сплавы. Сплавы имеют более разнообразные свойства по сравнению с металлами, поэтому в промышленности редко используют чистые металлы. В большинстве случаев для изготовления деталей различных машин и приборов применяют сплавы. Так, медь, олово и цинк - это мягкие металлы, тогда как сплав на их основе - бронза - очень твердый, поэтому бронзу люди издавна использовали для изготовления оружия, плугов и других изделий, где требуется повышенная жесткость. Сплав олова со свинцом (третник) применяют при пайке, так как он имеет сравнительно низкую температуру плавления. Наиболее распространенными из сплавов является чугун и сталь - сплав железа с углеродом и другими неметаллами.
worldofscience.ru
Физические и химические свойства металлов
Металлы широко распространены в природе и могут встречаться в различном виде: в самородном состоянии (Ag, Au, Rt, Cu), в виде оксидов (Fe3O4, Fe2O3, (NaK)2O×AlO3), солей (KCl, BaSO4, Ca3(PO4)2), а также сопутствуют различным минералам (Cd – цинковые руды, Nb, Tl – оловянные и т.д.).
Физические свойства металлов
Всем металлам присущи металлический блеск (однако In и Ag отражают свет лучше других металлов), твердость (самый твердый металл – Cr, самые мягкие металлы – щелочные), пластичность (в ряду Au, Ag, Cu, Sn, Pb, Zn, Fe наблюдается уменьшение пластичности), ковкость, плотность (самый легкий металл – Li, самый тяжелый – Os), тепло – и электропроводность, которые уменьшаются в ряду Ag, Cu, Au, Al, W, Fe.
В зависимости от температуры кипения все металлы подразделяют на тугоплавкие (Tкип > 1000С) и легкоплавкие (Tкип < 1000С). Примером тугоплавких металлов может быть – Au, Cu, Ni, W, легкоплавких – Hg, K, Al, Zn.
Среди металлов присутствуют s-, p-, d- и f-элементы. Так, s- элементы – это металлы I и II групп Периодической системы (ns1, ns2), р- элементы – металлы, расположенные в группах III – VI (ns2np1-4). Металлы d-элементы имеют большее число валентных электронов по сравнению с металлами s- и p-элементами. Общая электронная конфигурация валентных электронов металлов d-элементов – (n-1)d1-10ns2. Начиная с 6 периода появляются металлы f-элементы, которые объединены в семейства по 14 элементов (за счет сходных химических свойств) и носят особые названия лантаноидов и актиноидов. Общая электронная конфигурация валентных электронов металлов f-элементов – (n-2)f1-14(n-1)d0-1ns2.
Химические свойства металлов
Металлы способны реагировать с простыми веществами, такими как кислород (реакция горения), галогены, азот, сера, водород, фосфором и углеродом:
2Al + 3/2 O2 = Al2O3 (оксид алюминия)
2Na + Cl2 = 2NaCl (хлорид натрия)
6Li + N2 = 2Li3N (азид лития)
2Li+2C = Li2C2 (карбид лития)
2K +S = K2S (сульфид калия)
2Na + h3 = NaH (гидрид натрия)
3Ca + 2P = Ca3P2 (фосфид кальция)
Металлы взаимодействуют друг с другом, образуя интерметаллические соединения:
3Cu + Au = Cu3Au
Щелочные и некоторые щелочноземельные металлы (Ca, Sr, Ba) взаимодействуют с водой с образованием гидроксидов:
Ba + 2h3O = Ba(OH)2 + h3↑
2Na + 2h3O = 2NaOH + h3↑
В ОВР металлы являются восстановителями – отдают валентные электроны и превращаются в катионы. Восстановительная способность металла — его положение в электрохимическом ряду напряжений металлов. Так, чем левее в ряду напряжений стоит металл, тем более сильные восстановительные свойства он проявляет.
Металлы, стоящие в ряду активности до водорода способны реагировать с кислотами:
2Al + 6HCl = 2AlCl3 + 3 h3↑
Zn + 2HCl = ZnCl2 + 2h3↑
Fe + h3SO4 = FeSO4 + h3↑
Получение металлов
Щелочные, щелочноземельные металлы и алюминий получают электролизом расплавов солей или оксидов этих элементов:
2NaCl = 2Na + Cl2↑
CaCl2 = Ca + Cl2↑
2Al2O3 = 4Al + 3O2↑
Тяжелые металлы получают восстановлением из руд при высоких температурах и в присутствии катализатора (пирометаллургия) (1) или восстановлением из солей в растворе (гидрометаллургия) (2):
Cu2O + C = 2Cu + CO (1)
CuSO4 + Fe = Cu + FeSO4 (2)
Некоторые металлы получают термическим разложением их неустойчивых соединений:
Ni(CO)4 = Ni + 4CO
Примеры решения задач
ru.solverbook.com
Физические свойства металлов
Всем металлам присущи металлический блеск (однако In и Ag отражают свет лучше других металлов), твердость (самый твердый металл – Cr, самые мягкие металлы – щелочные), пластичность (в ряду Au, Ag, Cu, Sn, Pb, Zn, Fe наблюдается уменьшение пластичности), ковкость, плотность (самый легкий металл – Li, самый тяжелый – Os), тепло – и электропроводность, которые уменьшаются в ряду Ag, Cu, Au, Al, W, Fe.
В зависимости от температуры кипения все металлы подразделяют на тугоплавкие (Tкип > 1000С) и легкоплавкие (Tкип < 1000С). Примером тугоплавких металлов может быть – Au, Cu, Ni, W, легкоплавких – Hg, K, Al, Zn.
Физические свойства металлов IА группы
Металлы, расположенные в IA группе, называют щелочными. Все щелочные металлы легкие (обладают небольшой плотностью), очень мягкие (за исключением Li легко режутся ножом и могут быть раскатаны в фольгу), имеют низкие температуры кипения и плавления (с ростом заряда ядра атома щелочного металла происходит понижение температуры плавления).
В свободном состоянии Li, Na, K и Rb – серебристо-белые металлы, Cs – металл золотисто-желтого цвета.
Щелочные металлы хранят в запаянных ампулах под слоем керосина или вазелинового масла, поскольку они обладают высокой химической активностью.
Щелочные металлы обладают высокой тепло- и электропроводностью, что обусловлено наличием металлической связи и объемоцентрированной кристаллической решетки
Физические свойства металлов IIА группы
Металлы, расположенные в IIA группе, называют щелочноземельными. В свободном состоянии Be – металл серо-стального цвета, обладающий плотной гексагональной кристаллической решеткой, достаточно твердый и хрупкий. На воздухе Be покрывается оксидной пленкой, что придает ему матовый оттенок и снижает его химическую активность.
Магний в виде простого вещества представляет собой белый металл, который, также, как и Be, при нахождении на воздухе приобретает матовый оттенок за счет образующейся оксидной пленки. Mg мягче и пластичнее бериллия. Кристаллическая решетка Mg – гексагональная.
Ca, Ba и Sr в свободном виде – серебристо-белые металлы. При нахождении на воздухе мгновенно покрываются желтоватой пленкой, которая представляет собой продукты их взаимодействия с составными частями воздуха. Кальций – достаточно твердый металл, Ba и Sr – мягче.
Ca и Sr имею кубическую гранецентрированную кристаллическую решетку, барий – кубическую объемоцентрированную кристаллическую решетку.
Все щелочноземельные металлы характеризуются наличием металлического типа химической связи, что обуславливает их высокую тепло- и электропроводность. Температуры кипения и плавления щелочноземельных металлов выше, чем щелочных металлов.
Физические свойства металлов IIIА группы
Металлы, находящиеся в IIIA группе – Al, Ga, In, Tl – в свободном виде представляют собой металлы серебристого цвета с характерным металлическим блеском, обладающие высокими значениями тепло- и электропроводности. За счет образования оксидной пленки при пребывании на воздухе Tl темнеет.
При переходе от Al к Tl, т.е. с ростом заряда ядра атома химического элемента, происходит уменьшение температур кипения и плавления простых веществ.
Физические свойства металлов IVА группы
Металлы, находящиеся в IVA группе – Ge, Sn, Pb. В свободном виде Ge представляет собой металл серебристо-белого цвета, Pb – металл сине-серого цвета. Для олова характерно явление аллотропии, так, различают белое и серое олово, различающиеся строением кристаллической решетки (тетрагональная у белого олова и кубическая у серого).
Физические свойства металлов IVВ группы
В эту группу входят Ti, Zr и Hf, которые в свободном состоянии и в виде слитков представляют собой металлы серебристо-белого цвета, характеризующиеся ковкостью и пластичностью, хотя присутствие примесей, даже незначительное резко изменяет их характеристики – твердые и хрупкие. Для этих металлов характерна гексагональная плотноупакованная кристаллическая решетка, низкие температуры плавления (тугоплавкие металлы) и кипения, а также невысокая электропроводность.
Физические свойства металлов VВ группы
Ванадий, ниобий и тантал – представители металлов VВ группы. В свободном виде V, Nb, Ta – металлs бледно-серого («стального») цвета. Для ванадия характерны: твердость, пластичность, высокая плотность, легкость, высокая температура плавления. Твердость, ковкость и тугоплавкость – основные характеристики Nb и Ta.
Физические свойства металлов VIВ группы
Для металлов VIB группы характерны высокая электропроводность и твердость, они являются парамагнетиками и в свободном виде представляют собой светло-серые металлы. При переходе от Cr к W, т.е. с увеличением заряда ядра атома химического элемента, значения температур плавления и кипения, а также плотности увеличиваются. Cr, Mо и W обладают объемно-центрированной кубической кристаллической решеткой.
Физические свойства металлов VIIВ группы
Металлы, входящие в VIIВ группу – Mn, Tc и Re – в свободном виде – серебристо-белые металлы, для них, как и для металлов VIВ группы с увеличением заряда ядра атома химического элемента характерно увеличение значений температур плавления и кипения, а также плотности. Для технеция и рения характерна плотная гексагональная кристаллическая решетка. Tc – хрупкий металл, Re – более пластичен.
Для марганца характерно несколько модификаций, в зависимости от структуры кристаллической решетки: сложная кубическая – α-марганец, примитивная кубическая – β- марганец, гранецетрированная кубическая – γ- марганец, объемно-центрированная кубическая – δ- марганец.
Физические свойства металлов VIIIВ группы
Металлы, входящие в состав VIII группы – Fe, Co, Ni, Ru, Rh, Pd, Os, Ir, Pt – условно разделяют на 2 подгруппы: элементы подгруппы железа (Fe, Co, Ni) и элементы подгруппы платины (Ru, Rh, Pd, Os, Ir, Pt).
Железо – металл серебристо-белого цвета, кобальт и никель – металлы серовато-белого цвета. Для железа характерны 4 модификации, для кобальта – две, для никеля – одна, в зависимости от структуры кристаллической решетки и температуры, до которой нагревают эти металлы.
Выделяют α- (объемно-центрированная кристаллическая решетка, характерны ферромагнитные свойства, T<910C), β- (объемно-центрированная кристаллическая решетка, характерны парамагнитные свойства, T=769C), γ- (кубическая гранецентрированная кристаллическая решетка, T=769-910 C), и δ- железо (кубическая объемно-центрированная кристаллическая решетка, T=1400C). Для железа характерны, ковкость, пластичность и тугоплавкость.
Различают α- (гексагональная кристаллическая решетка, T<427C) и β-модификации кобальта (кубическая гранецентрированная кристаллическая решетка T>427C). Для кобальта характерны, ковкость и тягучесть.
Для никеля характерна кубическая гранецентрированная кристаллическая решетка. В отличие от железа и кобальта, магнитные свойства никеля значительно ниже.
Элементы подгруппы платины, в зависимости от значений их плотности, разделяют на легкие (Ru, Rh, Pd) и тяжелые (Os, Ir, Pt), для них характерны серовато-белый цвет, тугоплавкость, твердость, хрупкость и высокая плотность.
Примеры решения задач
ru.solverbook.com
Основные физические свойства чистых металлов
| Металл | Хим.символ | Атомныйномер | Плотн.г/(см^3) | Тплав.°С | Уд. теплоемк.Дж/(кг*°К) | Уд. теплопр.Вт/(м*°К) | Тепл. коэф лин.расш. (10^6)/°К | ЧислоБринеля | Уд. сопрот. мкОм*м | Магнитные свойства |
| Алюминий | Al | 13 | 2,70 | 660 | 923 | 218,0 | 21,0 | 25 | 0,026 | Парамагнетик |
| Барий | Ba | 56 | 3,75 | 710 | 285 | - | 19,0 | 4,2 | 0,500 | Парамагнетик |
| Берилий | Be | 4 | 1,84 | 1280 | 1800 | 184 | 12,0 | 61 | 0,041 | Диамагнетик |
| Ванадий | V | 23 | 6,11 | 1900 | 503 | 31 | 8,3 | 64 | 0,248 | Парамагнетик |
| Висмут | Bi | 83 | 9,80 | 271 | 126 | 8,4 | 13,3 | 9,6 | 1,160 | Диамагнетик |
| Вольфрам | W | 74 | 19,30 | 3400 | 142 | 167,0 | 4,4 | 262 | 0,055 | Парамагнетик |
| Гадолиний | Gd | 64 | 7,89 | 1310 | - | 8,8 | 9,7 | - | 1,400 | Ферромагнетик |
| Галлий | Ga | 31 | 5,92 | 30 | 336 | 29,3 | 18,1 | 6,1 | 0,136 | Диамагнетик |
| Гафний | Hf | 72 | 13,29 | 2220 | 138 | 22,0 | 5,9 | 173 | 0,351 | Парамагнетик |
| Железо | Fe | 26 | 7,87 | 1540 | 453 | 73,3 | 10,7 | 50 | 0,097 | Ферромагнетик |
| Золото | Au | 79 | 19,30 | 1063 | 134 | 312,0 | 14,0 | 18 | 0,0225 | Диамагнетик |
| Индий | In | 49 | 7,30 | 156 | 239 | 72 | 28,4 | 0,9 | 0,090 | Диамагнетик |
| Иридий | Ir | 77 | 22,40 | 2410 | 130 | 146,0 | 6,5 | 170 | 0,054 | Парамагнетик |
| Иттрий | Y | 39 | 4,47 | 1525 | 310 | 14,6 | 9,3 | 60 | 0,650 | Парамагнетик |
| Кадмий | Cd | 48 | 8,65 | 320,9 | 231 | 92,8 | 29,0 | 21 | 0,074 | Диамагнетик |
| Калий | K | 19 | 0,86 | 63 | 754 | 97,0 | 83,3 | 0,04 | 0,065 | Парамагнетик |
| Кальций | Ca | 20 | 1,53 | 851 | 650 | 98 | 18,5 | 17 | 0,040 | Парамагнетик |
| Кобальт | Co | 27 | 8,85 | 1500 | 445 | 69,5 | 13,5 | 102 | 0,064 | Ферромагнетик |
| Лантан | La | 57 | 6,18 | 920 | 188 | 13,8 | 5,2 | 37 | 0,568 | Парамагнетик |
| Литий | Li | 3 | 0,53 | 180 | 3285 | 71 | 56 | - | 0,086 | Парамагнетик |
| Магний | Mg | 12 | 1,74 | 651 | 1040 | 170,0 | 27 | 30 | 0,045 | Парамагнетик |
| Марганец | Mn | 25 | 7,44 | 1244 | 477 | 66,7 | 22,3 | 196 | 1,850 | Антиферромагн. |
| Медь | Cu | 29 | 8,92 | 1083 | 386 | 406,0 | 16,6 | 35 | 0,017 | Диамагнетик |
| Молибден | Mo | 42 | 10,20 | 2620 | 272 | 150,0 | 5,3 | 153 | 0,050 | Парамагнетик |
| Натрий | Na | 11 | 0,97 | 98 | 1220 | 134,0 | 72,0 | 0,07 | 0,042 | Парамагнетик |
| Никель | Ni | 28 | 8,96 | 1453 | 440 | 75,5 | 13,2 | 68 | 0,068 | Ферромагнетик |
| Ниобий | Nb | 41 | 8,57 | 2470 | 268 | 50,0 | 7,2 | 75 | 0,150 | Парамагнетик |
| Олово | Sn | 50 | 7,29 | 231,9 | 226 | 63,1 | 23,0 | 5,2 | 0,113 | Парамагнетик |
| Осмий | Os | 76 | 22,50 | 3000 | 129 | - | 4,6 | 400 | 0,095 | Парамагнетик |
| Палладий | Pd | 46 | 12,02 | 1552 | 243 | 70,7 | 9,5 | 46 | 0,108 | Парамагнетик |
| Платина | Pt | 78 | 21,45 | 1773 | 134 | 71,1 | 9,5 | 40 | 0,098 | Парамагнетик |
| Рений | Re | 75 | 21,02 | 3180 | 138 | 52,0 | 6,7 | 135 | 0,214 | Парамагнетик |
| Родий | Rh | 45 | 12,48 | 1970 | 247 | 88,0 | 8,5 | 102 | 0,043 | Парамагнетик |
| Ртуть | Hg | 80 | 13,50 | - 39 | 138 | 7,9 | 182,0 | - | 0,958 | Диамагнетик |
| Рубидий | Rb | 37 | 1,53 | 39 | 335 | 35,6 | 90,0 | 0,022 | 0,120 | Парамагнетик |
| Рутений | Ru | 44 | 12,4 | 2250 | 239 | - | 9,1 | 220 | 0,075 | Парамагнетик |
| Свинец | Pb | 82 | 11,34 | 327 | 130 | 35,0 | 28,3 | 3,9 | 0,190 | Диамагнетик |
| Серебро | Ag | 47 | 10,49 | 960,5 | 235 | 453,0 | 18,6 | 25 | 0,015 | Диамагнетик |
| Скандий | Sc | 21 | 3,00 | 1540 | 545 | 11,3 | 11,4 | 75 | 0,660 | Парамагнетик |
| Стронций | Sr | 38 | 2,63 | 770 | 737 | - | 21,0 | 14 | 0,227 | Парамагнетик |
| Таллий | Tl | 81 | 11,85 | 303 | 147 | 35 | 28,0 | 2,7 | 0,180 | Диамагнетик |
| Тантал | Ta | 73 | 16,6 | 3000 | 150 | 50 | 6,6 | 47 | 0,124 | Парамагнетик |
| Титан | Ti | 22 | 4,52 | 1670 | 550 | 21,9 | 8,1 | 73 | 0,470 | Парамагнетик |
| Торий | Th | 90 | 11,6 | 1750 | 113 | 37,0 | 11,5 | 41 | 0,130 | Парамагнетик |
| Уран | U | 92 | 19,05 | 1130 | - | 26,7 | 14,0 | 244 | 0,300 | Парамагнетик |
| Хром | Cr | 24 | 7,19 | 1900 | 462 | 88,6 | 6,2 | 114 | 0,130 | Антиферромагн. |
| Цезий | Cs | 55 | 1,90 | 28 | 220 | 18,4 | 97 | 0,015 | 0,190 | Парамагнетик |
| Церий | Ce | 58 | 6,78 | 795 | 210 | 10,9 | 7,1 | 20 | 0,750 | Парамагнетик |
| Цинк | Zn | 30 | 7,14 | 419,5 | 336 | 113,0 | 30,0 | 42 | 0,059 | Диамагнетик |
| Цирконий | Zr | 40 | 6,50 | 1855 | 277 | 29,5 | 6,3 | 66 | 0,410 | Парамагнетик |
Основные материалы таблицы получены из справочника по электротехническим материалам том 3 под ред. Ю.В. Корицкого, В.В. Пасынкова, Б.М. Тареева
temperatures.ru
Основные свойства металлов
Прикладная наука, изучающая во взаимосвязи состав, строение и свойства металлов и сплавов, устанавливает зависимость строения и свойств от методов производства и обработки металлов и сплавов, а также изменение их под влиянием механических, термических и других внешних воздействий на металлы называется металловедение.
Свойство (property, quality) - это совокупность характеристик металлов и сплавов от которых зависит пригодность изготовления деталей и конструкций. Одни из них легкие (магний, алюминий, титан), другие тяжелые (свинец). Олово, свинец - металлы, которые легко плавятся, а для расплава железа или платины необходимо потратить много энергии. Прочность является одним из главных факторов при произведенные металла для изготовления деталей, но не все одинаково прочны. Различают физические, химические, механические и технологические свойства металлов:
А) Физические свойства металлов проявляются при действии физических явлений, действуя на металл, не изменяют его состава. Например, при нагревании металл расплавляется, но его состав остается прежним.
Плотность (solidity, strength) - величина, равная отношению массы металла к занимаемому им объему. Например, плотность железа равна 7800 кг/м3, алюминия 2700 кг/м3, свинца 11300 кг/м3.
Цветом называется способность металлов отражать световые лучи, на них попадают. Лучи света, отраженные от различных металлов, действующие на органы зрения по-разному, что создает ощущение того или иного цвета. Например, медь имеет розово-красный цвет, алюминий - белый.
Теплопроводностью (heat / thermalconductivity) называют способность металлов проводить тепло. Чем больше теплопроводность, тем быстрее тепло распространяется по металлу при его нагревании и отдается им при охлаждении. Высокую теплопроводность имеют медь алюминий. Железо, сталь, чугун проводят тепло в 4-6 раз хуже, чем медь.
Теплоемкость (thermal / heatcapacity) определяет количество тепла, необходимого для нагрева металла на 10. Низкую теплоемкость имеют платина и свинец. Теплоемкость стали и чугуна почти в 4 раза выше теплоемкости свинца.
Плавление (melting) - это процесс перехода металла из твердого состояния в жидкое. Металлы с высокой температурой плавления считают тугоплавкими (вольфрам, хром, платина), а металлы с низкой температурой плавления относятся к легкоплавких (олово, свинец). Например, температура плавления железа-15390, меди-1083, олова-2319, углеродистой стали - 1420-1520 0С.
Тепловое (термическое) расширение означает способность нагреваемого, увеличивать свои размеры.
Электропроводностью называют способность металла проводить электрический ток. Хорошими проводниками тока являются серебро, медь, алюминий. Некоторые металлы и сплавы (нихром) оказывают электрическому току большое сопротивление.
Б) Химические свойства. Это - способность металлов и сплавов взаимодействовать с окружающей средой, вступать в химические соединения, растворяться, корродировать, сопротивляться действию агрессивных сред. Наиболее важные из них - это окисление на воздухе, кислотостойкость, щелочестойкости, жаропрочность.
В) Механические свойства связаны с понятием о нагрузке, деформацию и напряжение. От механических свойств металла зависит его поведение при деформации и разрушении под действием внешних сил конструкций или деталей. Этим свойствам будет подробно рассмотрено далее, потому что именно им уделено основное внимание в этом разделе.
Прочность (durability) - это свойство металлов, не разрушаясь, сопротивляться действию приложенных внешних сил. Прочность металлов характеризуется условной величиной - пределом прочности. Пределом прочности является нагрузка, приложенная к образцу в момент разрыва, отнесенное к площади поперечного сечения образца.
Упругость (resilience) - способность металлов изменять свою форму под действием внешних сил и восстанавливать ее после прекращения действия этих сил; Отношение нагрузки, при котором образец начинает иметь остаточные удлинения, в плоскости его поперечного сечения называется пределом упругости. Например, предел упругости стали до 300; меди 25; свинца 2,5 МПа.
Пластичность (plasticity) - способность металлов, не разрушаясь, изменять под действием внешних сил свою форму, после прекращения действия сил. Сталь в значительной степени пластична, а при нагревании ее пластичность возрастает. Это свойство используют при получении изделий путем проката и ковки.
Утомляемость (tiredness) - изменение механических и физических свойств материалов под действием сил, циклически меняются при напряжений и деформаций. В условиях действия таких нагрузок в работающих деталях образуются и развиваются трещины, приводящие к полному разрушению деталей. Подобные разрушения опасны тем, что могут проходить под действием напряжений значительно меньших пределов прочности и текучести.
Хрупкость (fragile) - свойство металла разрушаться сразу после действия приложенных к нему сил, не показывая никаких признаков деформации (чугун).
Твердость (hardness) - способность металла сопротивляться вдавливанию в него другого, более твердого материала. Чугун и сталь имеют высокую твердость, свинец - низкую. Для проверки твердости металлов существует три метода испытания, названных по именам их изобретателей - Бринелля, Роквелла, Виккерса:
- Испытание по способу Бринелля заключается в том, что в поверхность образца металла, под определенной нагрузкой, вдавливают стальную закаленную шарик диаметром 2,5; 5,0; 10 мм. После вдавливания образца на поверхности остается отпечаток шарика. С помощью специального микроскопа измеряется диаметр отпечатка, а затем определяется число твердости НВ: отношение приложенного к шарику нагрузки к плоскости поверхности отпечатка называется числом твердости по Бринелю НВ. Числа твердости по Бринелю НВ для углеродистой стали - 1300-2800, меди - 300. свинец - 30-80 МПа,
- Испытания образца по способу Роквелла (HR) заключается в том, что с помощью пресса в поверхность образца вдавливают алмазный конус с углом при вершине 1200. Твердость определяется глубиной вдавливания конуса,
- Испытание по способу Виккерса (HV) применяют для измерения твердости на небольших участках термически обработанных металлов. В образец металла с помощью пресса вдавливают правильную четырехгранную алмазную пирамиду с углом при вершине 1360.
Ударная вязкость - способность металлов или не разрушаться при воздействии на них ударных нагрузок. Ударная вязкость определяется с помощью маятникового копра. Образец стандартной формы устанавливают в опорах и разрушают падающим с высоты грузом.
Г) Технологические свойства определяют способность металлов получать ту или иную обработку. К технологическим свойствам металлов относятся: обработка резанием, ковкость, жидкотекучесть, усадка, свариваемость.
Ковкость (malleable) называется способность металлов, не разрушаясь, принимать нужную форму под действием внешних сил. Сталь в нагретом состоянии имеет хорошую ковкость.
Редко текучестью (seldom-fluidity) называется способность расплавленных металлов заполнять литейные формы. Высокую жидкотекучесть имеет серый чугун, низкую - медь.
Усадкой (shrinkage) называется способность расплавленных металлов уменьшать свой объем при охлаждении. Это свойство имеет значение в литейном деле. Модели отливок изготавливают с учетом усадки, т.е. больших размеров чем размеры отливки. Кроме того, усадка приводит к образованию трещин в отливках. Наименьшую усадку имеют серый чугун, цинковые и алюминиевые сплавы.
Обработка резанием - это способность металлов подвергаться воздействию режущих инструментов. Учитывая меньшую твердость, некоторые цветные металлы легче обрабатывать резанием, чем черные
Свариваемостью называется способность металлов прочно соединяться путем расплавления места соединения. Хорошо свариваются стали с низким содержанием углерода. Чугун и сплавы цветных металлов свариваются значительно сложнее.
worldofscience.ru
1.2. Основные свойства металлов и сплавов
Металлы и сплавы характеризуются комплексом физических, механических, химических и технологических свойств.
Физические свойства металлов и сплавов – блеск, плотность, температура плавления, теплопроводность, теплоемкость, электропроводность, магнитные свойства, расширяемость при нагревании и фазовых превращениях.
Механические свойства металлов и сплавов – твердость, упругость, прочность, хрупкость, пластичность, вязкость, износостойкость, сопротивление усталости, ползучесть.
Химические свойства металлов и сплавов определяют их способность сопротивляться воздействию окружающей среды. При контакте с окружающей средой металлы и сплавы подвергаются коррозии, растворяются окисляются и снижают свою жаропрочность.
Технологические свойства металлов и сплавов – ковкость, свариваемость, прокаливаемость, склонность к обезуглероживанию, обрабатываемость резанием, жидкотекучесть, закаливаемость. Они характеризуют способность металлов и сплавов обрабатываться различными методами. Кроме того, они позволяют определить, насколько экономически эффективно можно изготовить изделие.
Ковкость – способность металла и сплава обрабатываться путем пластического деформирования.
Свариваемость – способность металла и сплава образовывать неразъемное соединение, свойства которого близки к свойствам основного металла (сплава).
Прокаливаемость – способность металла и сплава закаливаться на определенную глубину.
Склонность к обезуглероживанию металла и сплава – возможность выгорания углерода в поверхностных слоях изделий из сплавов и сталей при нагреве в среде, содержащей кислород и водород.
Обрабатываемость резанием – поведение металла и сплава под воздействием режущего инструмента.
Жидкотекучесть – способность расплавленного металла и сплава заполнять литейную форму.
Закаливаемость – способность металла и сплава к повышению твердости при закалке (нагрев и быстрое охлаждение).
Физические свойства металлов и сплавов важны для самолетостроения, автомобилестроения, медицины, строительства, изготовления космических аппаратов и часто являются основными характеристиками, по которым определяют возможность использования того или иного металла или сплава.
Блеск – способность поверхности металла и сплава направленно отражать световой поток.
Плотность – масса единицы объема металла или сплава. Величину, обратную плотности, называют удельным объемом.
Температура плавления – это температура, при которой металл или сплав целиком переходит в жидкое состояние.
Теплопроводность – количество теплоты, проходящее в секунду через сечение в 1см2, когда на расстоянии в 1см изменение температуры составляет в 10С.
Теплоемкость – количество теплоты, необходимой для повышения температуры тела на 10С.
Электрическая проводимость – величина, обратная электрическому сопротивлению. Под удельным электрическим сопротивлением понимают электрическое сопротивление проводника длиной 1 м и площадью поперечного сечения в 10-6м2 при пропускании по нему электрического тока.
К магнитным свойствам металлов и сплавов относятся: начальная магнитная проницаемость, максимальная магнитная проницаемость, коэрцитивная сила, намагниченность насыщения, индукция насыщения, остаточная магнитная индукция, точка Кюри, петля гистерезиса.
При помещении стального образца в магнитное поле возникающая в нем магнитная индукция (b) является функцией напряженности магнитного поля (Нm).
Намагниченность (М) пропорциональна напряженности магнитного поля. Эти величины связаны между собой коэффициентом 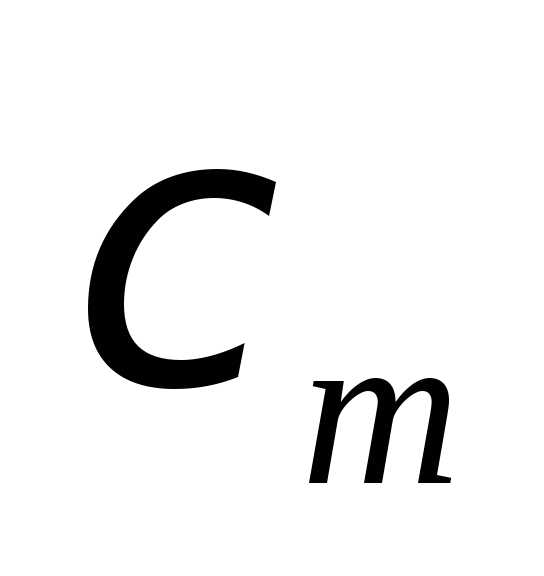 , который называется магнитной восприимчивостью стали или сплава.
, который называется магнитной восприимчивостью стали или сплава.
(1)
Между магнитной индукцией и напряженностью магнитного поля существует аналитическая связь
(2)
где 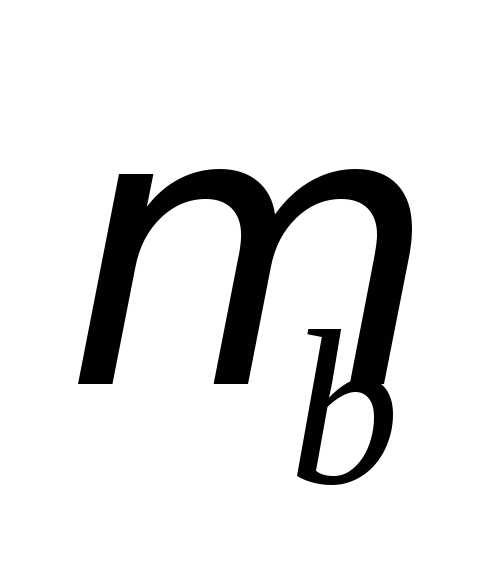 - магнитная проницаемость вакуума.
- магнитная проницаемость вакуума.
Для ферромагнетиков (сплавов, способных намагничиваться до насыщения в малых магнитных полях) , где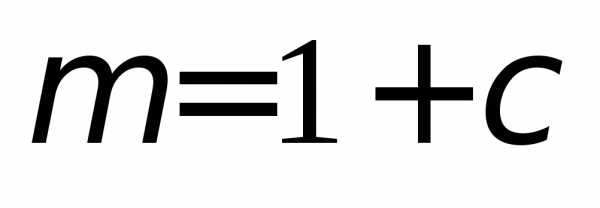 - коэффициент магнитной проницаемости.
- коэффициент магнитной проницаемости.
При намагничивании ферромагнитных материалов (стали, полученные соединением ферромагнетиков с парамагнетиками) намагниченность сначала плавно возрастает, потом резко повышается и постепенно достигает насыщения. При уменьшении напряженности магнитного поля Нm после намагничивания и реверсирования (изменение направления поля) его кривая изменения индукции образует замкнутую петлю. Эта петля называется петлей гистерезиса.
Основными параметрами начальной кривой и петли гистерезиса являются остаточная индукция br, коэрцитивная сила Нс, напряженность насыщающего поля Нн и намагниченность насыщения Мs. По начальной кривой определяется кривая магнитной проницаемости, в которой основными точками являются начальная магнитная проницаемость 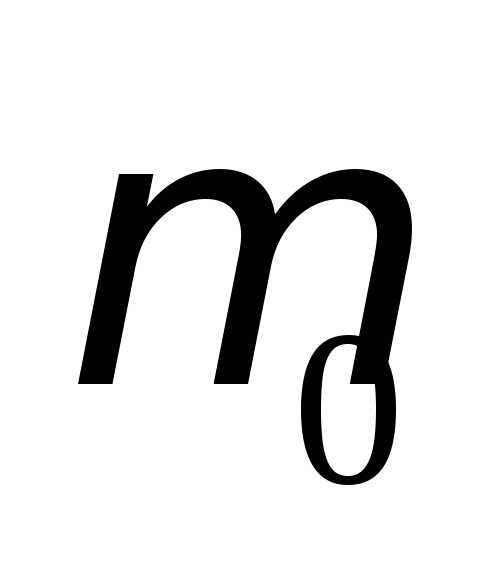 и максимальная магнитная проницаемость
и максимальная магнитная проницаемость .
.
Наибольшее значение индукции на петле гистерезиса называется индукцией насыщения 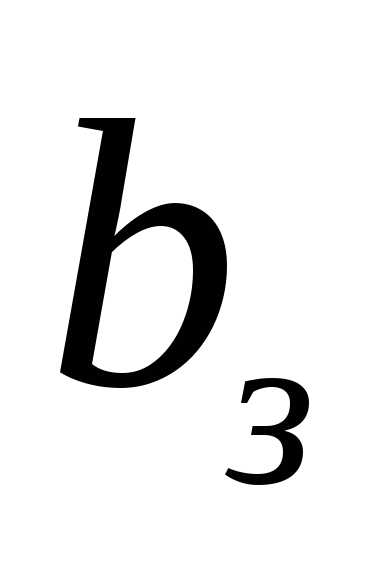 .
.
Ферромагнетики при нагреве до определенной температуры переходят в парамагнитное состояние (в состояние с малой магнитной восприимчивостью). Эта температура называется точкой Кюри. Точка Кюри определяется в основном химическим составом сплава или стали и не зависит от давлений, напряжений и других факторов.
Все характеристики ферромагнитных материалов можно разделить на структурно нечувствительные и структурно чувствительные. К структурно нечувствительным характеристикам относятся точка Кюри, намагниченность насыщения, зависящие от произвольной намагниченности, к структурно чувствительным – магнитная проницаемость, остаточная индукция и коэрцитивная сила.
Структурно нечувствительные характеристики ферромагнитных материалов зависят в основном от химического состава и числа фаз и практически не зависят от кристаллической структуры, размера частиц зерна металла. Следовательно, измерение точки Кюри, намагниченности насыщения и т.д. необходимо для качественного фазового анализа стали и сплава.
Измерение структурно чувствительных характеристик необходимо при изучении структурных изменений в сплавах и сталях при термической или механической обработке.
Магнитная проницаемость, коэрцитивная сила и остаточная индукция изменяются при обработке сплавов и сталей. Расширение при нагревании изделий из сталей и сплавов – изменение размеров и формы зерен, характеризуется температурными коэффициентами объемного расширения и линейного расширения. Расширение при нагревании в интервале температур фазовых превращений сталей и сплавов характеризуется коэффициентом линейного расширения отдельных фаз. Внутренние (фазовые и структурные) превращения в металлах и сплавах характеризуются изменением объема, линейных размеров и коэффициента расширения. При фазовых превращениях в металлах и сплавах происходит выделение или поглощение скрытой теплоты превращения, изменяется теплоемкость изделия. Поэтому при изменении структуры металла или сплава, нагреваемого или охлаждаемого с постоянной скоростью, могут появиться отклонения от нормальной кривизны на кривых изменения температуры по времени. По этим кривым, называемым термическими кривыми, определяют температуру (температурный интервал) превращения.
studfiles.net