Формула пропана. Пропан 2 он
Пропанол-1 — WiKi
Пропиловый спирт (пропан-1-ол, 1-пропанол) C3H7OH — одноатомный спирт. Встречается в природе в небольших количествах как продукт ферментации. Так, он является компонентом сивушного масла. Существует изомер 1-пропанола — изопропиловый спирт (пропан-2-ол, 2-пропанол).
| Пропанол-1 | |
| пропан-1-ол | |
| пропиловый спирт, 1-пропанол | |
| C3H7OH | |
| жидкость | |
| 60,09 г/моль | |
| 0,80 г/см³ | |
| 2,256*10-3 Па·с | |
| 10,15±0,01 эВ[1] | |
| −127 °C | |
| 97,4 °C | |
| 72±1 °F[1] | |
| 2,2±0,1 об.%[1] | |
| 147,2 (25°C) Дж/(моль·К) | |
| 0,16 Вт/(м·K) | |
| -5071,4 кДж/моль | |
| 89,43 кДж/моль | |
| 749,01 кДж/моль | |
| 0,956 *10-3 K-1 | |
| 1,928 (20°C), 6,986 (40°C), 20,292 (60°C), 50,750 (80°C) кПа | |
| 16 | |
| смешивается | |
| 1,3850 | |
| 1,68 D | |
| 71-23-8 | |
| 1031 | |
| 200-746-9 | |
| UH8225000 | |
| 28831 | |
| 1274 | |
| 1004 | |
| 1870 мг/кг | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Физические свойства
Химические свойства
Получение
В промышленности 1-пропанол получают путём гидроформилирования этилена с последующим гидрированием образовавшегося пропаналя.
C2h5+CO+h3→Ch4Ch3CHO+D{\displaystyle {\mathsf {C_{2}H_{4}+CO+H_{2}\rightarrow CH_{3}CH_{2}CHO+D}}} Ch4Ch3CHO+h3→Ch4Ch3Ch3OH{\displaystyle {\mathsf {CH_{3}CH_{2}CHO+H_{2}\rightarrow CH_{3}CH_{2}CH_{2}OH}}}1-Пропанол получается в качестве побочного продукта при сбраживании зерна на этанол, но этот способ получения не имеет особого промышленного значения.
Применение
1-Пропанол применяют в качестве растворителя для восков, полиамидных чернил, природных и синтетических смол, полиакрилонитрила; в производстве полиэтилена низкого давления; для получения карбометоксицеллюлозы; как обезжириватель металлов; сорастворитель поливинилхлоридных адгезивов; желатинирующий и пластифицирующий агент целлюлозноацетатных плёнок; алкилирующий агент. Его используют также для синтеза пропионовой кислоты, пропионового альдегида, пропилацетата, пропиламина, ПАВ, пестицидов, некоторых фармацевтических препаратов.
Топливо
1-Пропанол имеет высокое октановое число (118). Однако производство его слишком дорого для того, чтобы он стал широко применяемым топливом.
Токсикология
Употребление пропилового спирта, также как и этилового спирта, вызывает алкогольное опьянение. В организме человека пропиловый спирт окисляется до пропионовой кислоты, более едкой, чем уксусная кислота, в связи с чем токсичность пропилового спирта значительно выше, чем у этилового (ЛД50 для пропилового спирта = 1870 мг/кг, для этилового спирта 7060 мг/кг). В то же время по сравнению с метиловым спиртом, ЛД50 которого составляет 1500 мг/кг, пропиловый спирт относительно безопасен.
На 2011 год был зафиксирован один смертельный случай отравления пропиловым спиртом[6].
Безопасность
Горюч. ПДК пропилового спирта в воздухе рабочей зоны 10 мг/м3, в атмосферном воздухе населенных пунктов — не более 0,3 мг/м3.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4 (Пол-Три). — 639 с. — ISBN 5-82270-092-4.
Примечания
- ↑ 1 2 3 http://www.cdc.gov/niosh/npg/npgd0533.html
- ↑ Органикум. Том 1. Москва, Мир, 1992, стр. 274
- ↑ Методы получения химических реактивов и препаратов. Москва, ИРЕА, Выпуск 2, 1961, стр. 45 (см. стр. 46)
- ↑ Органикум. Том 2. Москва, Мир, 1992, стр. 84 (см. табл. на стр. 85)
- ↑ Синтезы органических препаратов. Сборник 2.Москва, Иностранная Литература, 1949, стр. 424
- ↑ N-PROPANOL Health-Base Assessment and Recommendation for HEAC. Архивировано 8 августа 2012 года.
ru-wiki.org
Пропан - это... Что такое Пропан?
Пропа́н, C3H8 — органическое вещество класса алканов. Содержится в природном газе, образуется при крекинге нефтепродуктов, при разделении попутного нефтяного газа, «жирного» природного газа, как побочная продукция при различных химических реакциях. Как представитель углеводородных газов пожаро- и взрывоопасен, малотоксичен, не имеет запаха, обладает слабыми наркотическими свойствами[1][2].
Физические свойства
Бесцветный газ без запаха[3]. Очень мало растворим в воде. Точка кипения −42,1 °C. Точка замерзания −188 °C. Образует с воздухом взрывоопасные смеси при концентрации паров от 2,1 до 9,5 %. Температура самовоспламенения пропана в воздухе при давлении 0,1 МПа (760 мм рт. ст.) составляет 466 °С. Критическая температура пропана Tкр = 370 К, критическое давление Pкр = 4,27 МПа, критический удельный объем Vкр = 0,0444 м3/кг[4] Плотность сжатого и сжиженного пропана при 298 K — 0,493 кг/л.
- Плотность жидкой фазы = 510 кг/м3[5].
- Плотность газовой фазы при нормальных условиях = 2,019 кг/м3.
- Плотность газовой фазы при температуре при 15°С = 1,900 кг/м3.
Химические свойства
Аналогичны свойствам других представителей ряда алканов (дегидрирование, хлорирование и т. д.)
Применение
Топливо
Баллон пропана на лёгком грузовике- При выполнении газопламенных работ на заводах и предприятиях:
- в заготовительном производстве;
- для резки металлолома;
- для сварки неответственных металлоконструкций.
- При кровельных работах.
- Для обогрева производственных помещений в строительстве.
- Для обогрева производственных помещений (на фермах, птицефабриках, в теплицах).
- Для газовых плит, водогрейных колонок в пищевой промышленности.
- В быту
- при приготовлении пищи в домашних и походных условиях;
- для подогрева воды;
- для сезонного обогрева отдалённых помещений — частных домов, отелей, ферм;
- для сварки труб, теплиц, гаражей и других хозяйственных конструкций с использованием газосварочных постов.
- В последнее время широко используется в качестве автомобильного топлива, так как дешевле и экологически безопаснее бензина.
Хранится и перевозится в металлических баллонах ярко-красного цвета (не путать с коричневыми баллонами для гелия)
Химия и пищевая промышленность
В химической промышленности используется при получении мономеров для производства полипропилена.
Является исходным сырьём для производства растворителей.
Используется как пропеллент.
В пищевой промышленности пропан зарегистрирован в качестве пищевой добавки E944.
Хладагент
Смесь из осушенного чистого пропана (R-290a) (коммерческое обозначение для описания изобутаново-пропановых смесей) с изобутаном (R-600a) не разрушает озонового слоя и обладает низким коэффициентом парникового потенциала (GWP). Смесь подходит для функционального замещения устаревших хладагентов (R-12, R-22, R-134a) в традиционных стационарных холодильных установках и систем кондиционирования воздуха (с обязательной сменой типа компрессорного масла).
Примечания
dic.academic.ru
Формула пропана в химии
Определение и формула пропана
Химическая формула –
Молярная масса равна г/моль.
Физические свойства – газ без цвета и запаха, мало растворим в воде и этаноле, но растворим в диэтиловом эфире. Горит слабо светящимся пламенем.
Содержится в природном газе.
Образуется при крекинге нефтепродуктов, при разделении попутного нефтяного газа, «жирного» природного газа, как побочная продукция при различных химических реакциях.
Пропан весьма пожаро- и взрывоопасен.
Химические свойства пропана
- Как типичный алкан, вступает в реакции галогенирования по радикальному механизму:
- Из других химических свойств следует отметить иные реакции протекающие по свободнорадикальному механизму, а именно, нитрование, сульфохлорирование, сульфоокисление. Исчерпывающие окисление пропана протекает до углекислого газа и воды под воздействием кислорода. Также можно проводить термолиз пропана с образованием непредельного соединения.
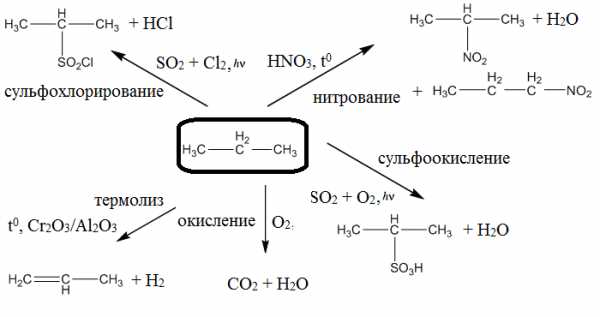
Применение
Пропан находит широкое применение в различных областях. В первую очередь он служит в качестве топлива.
Используется при выполнении газопламенных работ на заводах и предприятиях, обогрева помещений, для газовых плит, а также в качестве автомобильного топлива.
Является сырьем для получения полипропилена в химической промышленности.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Пропан или бутан – отличие двух газов
Пропан или бутан – отличие двух газов
Опубликовано: 31.12.2016 11:58Пропан и бутан используются как основные компоненты сжиженного углеводородного газа, использующегося в системах автономной газификации объектов. Как и пропан, бутан может использоваться в качестве топлива самостоятельно, однако разница в физических свойствах газов существенна, что накладывает ограничения на их самостоятельную эксплуатацию.
Пропан благодаря хорошей теплотворной способности, имеет широкое применение в быту и промышленности - от автомобильного топлива и источника питания для газовых плит и систем отопления до процесса резки металлов и сварки металлических конструкций. Бутан широко используется в качестве топлива для зажигалок, в качестве реагента в холодильных установках.
Существенную разницу составляет коэффициент объемного расширения газов - у пропана он в 1,5 раза выше (0,003 против 0,002 на 1 градус по Цельсию). Пропан гораздо более «упругий» газ - упругость его паров достигает 1,5МПа, в то время, как бутан при той же температуре сжимается на 283кПа. Практическую ценность эта разница имеет при выборе баллона - для хранения чистого жидкого пропана нужна более прочная емкость, чем для бутана.
Однако наиболее продуктивно газы используются в смеси. Так, ГОСТ 20448-90 «Газы углеводородные сжиженные топливные для коммунально-бытового потребления» запрещает самостоятельное использование бутана или пропана в системах газификации, а также устанавливает ограничения на то, как бутан или пропан (в процентном соотношении) могут быть использованы в смеси.

Бутан имеет химическую формулу С4Н10, пропан – С3Н8. Оба газа относятся к классу алканов (углеводородов, ряд которых описывается формулой СnН2n+2). Различия в составе бутана и пропана почти не сказываются на отличиях в их физических свойствах. Оба газа имеют схожий молекулярный вес и теплотворную способность. Однако бутан кипит (имеет температуру кипения) всего в -0,5оС, в то время как пропан гораздо более устойчив к отрицательных температурам. Температура кипения пропана – -43оС.
То есть, бутан не может эксплуатироваться топлива при отрицательных температурах. В газовый котел доставляется не жидкий бутан, а вещество в газообразной форме (в то время, как наш газ при температуре окружающего воздуха ниже нуля находится в состоянии жидкости).
В свою очередь, пропан также имеет существенный недостаток. Использование в качестве топлива чистого пропана опасно при высоких температурах. При нагревании происходит существенное расширение пропана, газ начинает давить на стенки баллона или газгольдера, что, в конечном итоге, приводит к появлению трещин на внутренней поверхности сосуда и к взрыву.
В отличие от пропана, газ С4Н10 более устойчив к высоким температурам. Поэтому ГОСТ 20448-90 устанавливает параметры пропан-бутановой смеси (сжиженного углеводородного газа) в процентном соотношении содержания обоих газов. Для пропана и бутана установлены минимальная и максимальная процентная величина соответственно. Так, в зимнее время пропан для северных регионов страны должен присутствовать в смеси в количестве не менее 75% от общего объема обоих газов. А содержание бутана в смеси не должно превышать 60%.
gazekoset.ru
ПРОПАН

Пропан — органическое вещество класса алканов (насыщенные углеводороды, парафины — ациклические углеводороды линейного или разветвлённого строения, содержащие только простые связи и образующие гомологический ряд с общей формулой Cnh3n+2). Содержится в природном газе, образуется при крекинге нефтепродуктов (высокотемпературная переработка нефти и её фракций с целью получения, как правило, продуктов меньшей молекулярной массы — моторных топлив, смазочных масел и т. п., а также сырья для химической и нефтехимической промышленности).
Бесцветный газ без запаха, очень мало растворим в воде. Температура кипения -42,1°С. Температура плавления -187,6°С. Образует с воздухом взрывоопасные смеси при концентрации паров от 2,1 до 9,5%. Температура самовоспламенения пропана в воздухе при давлении 0,1 МПа (760 мм рт. ст.) составляет 466 °С.
Аналогичны свойствам других представителей ряда алканов (горение, дегидрирование, галогенирование, нитрирование, крегинг).
Благодаря своим свойствам, таким как высокая теплотворная способность при сгорании, сгорание без остатка, безвредность и безопасность при правильной эксплуатации, удобство в использовании, пропан является универсальным газом и широко используется и на производстве, и в быту. Для производственных и бытовых целей поставляется в виде смеси пропан-бутановой технической. Бутан (C4h20) — органическое соединение класса алканов. На сегодняшний день спрос на СПБТ огромен.
На производстве При выполнении газопламенных работ на заводах и предприятиях: - в заготовительном производстве; - для резки металлолома; - для сварки неответственных металлоконструкций. При кровельных работах. Для обогрева производственных помещений в строительстве. Для обогрева производственных помещений (на фермах, птицефабриках, в теплицах). Для газовых плит, водогрейных колонок в пищевой промышленности. В быту - при приготовлении пищи в домашних и походных условиях; - для подогрева воды; - для сезонного обогрева отдалённых помещений - частных домов, отелей, ферм; - для сварки труб, теплиц, гаражей и других хозяйственных конструкций с использованием газосварочных постов.
В последнее время широко используется в качестве автомобильного топлива, т.к. дешевле и экологически безопаснее бензина. В химической промышленности используется при получении мономеров для производства полипропилена. Является исходным сырьём для производства растворителей. В пищевой промышленности пропан зарегистрирован в качестве пищевой добавки E944, как пропеллент.
Хладагент. Смесь из осушенного чистого пропана (R-290a) (коммерческое обозначение для описания изобутаново-пропановых смесей) с изобутаном (R-600a) не разрушает озонового слоя и обладает низким коэффициентом парникового потенциала (GWP). Смесь подходит для функционального замещения устаревших хладагентов (R-12, R-22, R-134a) в традиционных стационарных холодильных установках и систем кондиционирования воздуха.
Показатели качества газов углеводородных сжиженных определяются по ГОСТ 10157-79.
Пропан транспортируется и хранится в баллонах красного цвета с надписью «Пропан» ГОСТ 15860-84 , либо в специальных цистернах.
Пропан - взрывоопасный газ. С воздухом образует взрывоопасную смесь. Однако, при правильной эксплуатации практически безвреден.
www.gas-weld.ru
Пр. газ содержит 92% метана 4% этана 1% пропана 2% углекислого газа 1% азота(по объему). Какой объем кислорода? химия
Природный газ одного из местОрОждений содержит 92% метана 4% этана 1% пропана 2% углекислого газаи 1% азота (по объему) . Какой объем кислорода потребуется для сжигания 200 л этого газа? Решение: V(СН4)=200*0,92=184(л) V(С2Н6)=200*0,04=8(л) V(С3Н8)=200*0,01=2(л) 184л--------Хл СН4++++2О2====>СО2+2Н2О 1моль----2моль Х=368(л) 8л--------------Ул 2С2Н6++++7О2===>4СО2+6Н2О 2моль--------7моль У=28(л) 2л--------------Zл С3Н8+++++5О2====>3СО2+4Н2О 1моль-------5моль Z=10л V(O2)=X+Y+Z=406(л) это ответ. В первой задаче ответы на порядок меньше.
кислород - долевое участие в углекислом газе менее 1%
92=4=1=2=1=100 О каком кислороде может идти речь?
touch.otvet.mail.ru









