Содержание
Кристаллизация и аллотропические превращения металлов
Категория:
Автомобильные эксплуатационные материалы
Публикация:
Кристаллизация и аллотропические превращения металлов
Читать далее:
Основы теории металлических сплавов
Кристаллизация и аллотропические превращения металлов
В чистых металлах и сплавах при определенных температурах происходит изменение агрегатного состояния: твердое состояние сменяется жидким при температуре плавления. При обратном переходе из жидкого состояния в твердое образуется кристаллическая решетка и возникают кристаллы. Этот процесс называется кристаллизацией.
Основы кристаллизации разработаны русским ученым Д. К. Черновым, который установил два составных процесса кристаллизации: зарождение мельчайших частиц кристаллов (зародышей или центров кристаллизации) и рост из них кристаллов.
Процесс кристаллизации схематично представлен на рис. 1. Здесь на площади, ограниченной окружностями, показаны последовательные этапы зарождения из атомов первичных центров кристаллизации, их роста и возникновения новых зародышей, дальнейшего Роста кристаллов до соприкосновения их граней и окончания процесса кристаллизации. В результате образуется структура зерен кристаллов с неправильной геометрической формой.
1. Здесь на площади, ограниченной окружностями, показаны последовательные этапы зарождения из атомов первичных центров кристаллизации, их роста и возникновения новых зародышей, дальнейшего Роста кристаллов до соприкосновения их граней и окончания процесса кристаллизации. В результате образуется структура зерен кристаллов с неправильной геометрической формой.
Рекламные предложения на основе ваших интересов:
Дополнительные материалы по теме:
Рис. 1. Схема процесса кристаллизации
Величина верен зависит от количества зародышей кристаллизации и скорости их роста. На рис. 4 схематично показано влияние скорости охлаждения на возникновение центров кристаллизации и величину зерен. Если скорость охлаждения мала, то возникает небольшое число зародышей и в конце кристаллизации образуются крупные зерна. При большой скорости охлаждения количество зерен возрастает, но они становятся мельче. Это можно наблюдать на практике — в тонких сечениях литых деталей, где структура стали мелкозернистая, так как происходит быстрое охлаждение. Чтобы сделать зерно мелким, в металл вводят специальные вещества — модификаторы. Процесс искусственного регулирования величины зерел получил название модифицирования.
Чтобы сделать зерно мелким, в металл вводят специальные вещества — модификаторы. Процесс искусственного регулирования величины зерел получил название модифицирования.
Рис. 2. Влияние скорости охлаждения на процесс кристаллизации:
а — медленное охлаждение; б — ускоренное охлаждение; в — быстрое охлаждение
Рис. 3. Схема дендритной кристаллизации
Рис. 4. Кривые охлаждения при кристаллизации:
1 — теоретическая кривая; 2 — кривая реального процесса
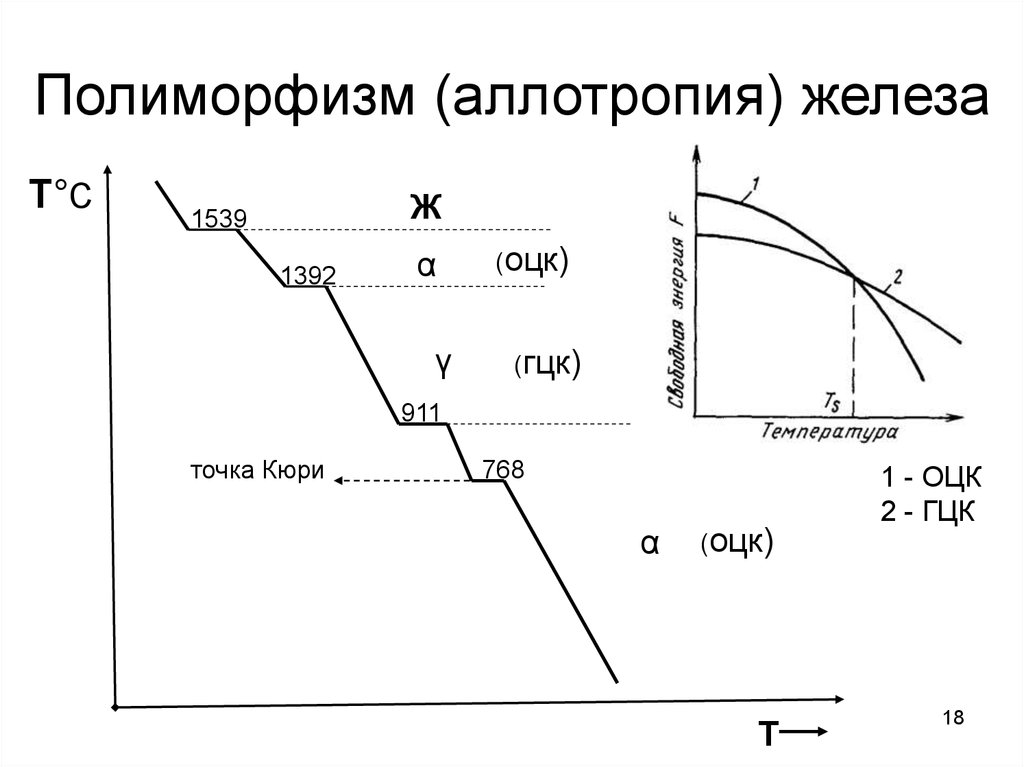
Рис. 5. Кривая охлаждения железа
Процесс образования кристаллов носит дендритный (древовидный) характер, на что впервые обратил внимание Д. К. Чернов. Сущность его состоит в том, что после образования зародышей рост их идет по направлениям кристаллической решетки, где имеется меньшая плотность упаковки атомов. Поэтому образуются оси первого порядка, затем от них под определенными углами начинают формироваться оси второго порядка, от них растут оси третьего порядка и т. д. В результате заполняется все пространство и образуется структура (дендрит), внешне напоминающая строение дерева. Если условия кристаллизации благоприятны, то могут возникнуть огромные дендриты, достигающие в длину нескольких десятков сантиметров. Нормальные дендриты в литых металлах имеют длину, равную всего нескольким миллиметрам. После горячей механической обработки (ковки, прокатки и прессовки) дендриты вытягиваются вдоль направления течения металла и образуют волокна, которые при наилучшем расположении распределяются вдоль контура изделия. Это оказывает положительное влияние на его механические свойства.
Если условия кристаллизации благоприятны, то могут возникнуть огромные дендриты, достигающие в длину нескольких десятков сантиметров. Нормальные дендриты в литых металлах имеют длину, равную всего нескольким миллиметрам. После горячей механической обработки (ковки, прокатки и прессовки) дендриты вытягиваются вдоль направления течения металла и образуют волокна, которые при наилучшем расположении распределяются вдоль контура изделия. Это оказывает положительное влияние на его механические свойства.
Для определения температуры кристаллизации металла термическим методом используют термоэлектрический пирометр, состоящий из термопары и гальванометра. Термопару помещают в расплав металла и по величине термоэдс измеряют температуру охлаждения через определенные промежутки времени, получая кривую охлаждения
Теоретически кривая охлаждения имеет вид, показанный на рис. 4 (кривая 1). Здесь при охлаждении начало кристаллизации (точка А) совпадает с равновесной температурой кристаллиэа-ции Тк. Далее процесс кристаллизации до ее окончания (точка Б) проходит при постоянной температуре, так как отвод тепла компенсируется выделяющейся скрытой теплотой кристаллизации. По окончании этого процесса температура вновь начинает понижаться.
Далее процесс кристаллизации до ее окончания (точка Б) проходит при постоянной температуре, так как отвод тепла компенсируется выделяющейся скрытой теплотой кристаллизации. По окончании этого процесса температура вновь начинает понижаться.
В реальных условиях затвердение металла не может происходить при равновесной температуре Тк, а начинается при более низкой температуре Тф (кривая 2), которая называется фактической температурой кристаллизации или температурой переохлаждения. Для большинства металлов температура переохлаждения очень незначительно отличается от равновесной (теоретической) температуры кристаллизации. Однако при увеличении скорости охлаждения температура Тф понижается.
Аллотропические превращения возникают в структуре кристаллической решетки некоторых металлов при изменении температуры. Они представляют собой перегруппировку атомов и переход одного вида кристаллической решетки в другой, Существование одного металла в нескольких кристаллических формах называется аллотропией, или полиморфизмом, а процесс перехода из одной кристаллической формы в другую — аллотропическим превращением.
Различные кристаллические формы металла называются аллотропическими, или полиморфными, модификациями и обозначаются начальными буквами греческого алфавита а, р, у и т. д. Буква ос обозначает модификацию металла, существующего при самой низкой температуре. Следующие буквы относятся к модификациям с более высокой температурой.
Процесс аллотропического превращения происходит при постоянной температуре и сопровождается выделением скрытой теплоты кристаллизации при охлаждении (или поглощением при нагреве). Вследствие этого аллотропическое превращение отмечается на кривой охлаждения горизонтальной линией.
Например, железо может существовать в нескольких модификациях (рис. 5). До температуры 911 °С железо имеет объемно-центрированную кубическую решетку. При 768 °С на кривой охлаждения получается ступенька, связанная не с перестройкой решетки, а с потерей магнитных свойств До этой температуры телезо магнитно и называется а-железо, а выше указанной температуры желе-80 теряет магнитные свойства и до температуры 911 °С называется железо.
В интервале температур 911—1392 °С железо образует гране-центрированную кубическую решетку и называется v-железо. Высокотемпературная модификация железа устойчивая, при температурах от 1392 °С до 1539 °С, имеет объемно-центрированную кубическую решетку а-железа и в отличие от него называется 3-железо.
Аллотропические превращения различных металлов имеют свои особенности. Знание их необходимо для практического использования при получении сплавов, а также для проведения термической пли химико-термической обработки.
7 Аллотропическое превращение и магнитное превращение в металлах (превращения в твердых состояниях.
Пространственные
кристаллические решетки в некоторых
металлах не всегда являются постоянными.
При определенных условиях решетки могут
изменяться. Это изменение происходит
главным образом под влиянием температуры.
Не исключено влияние и других факторов
— изменения давления, наличия посторонних
примесей и т. п. Способность металла
иметь различные формы кристаллической
решетки называется аллотропией, или
полиформизмом.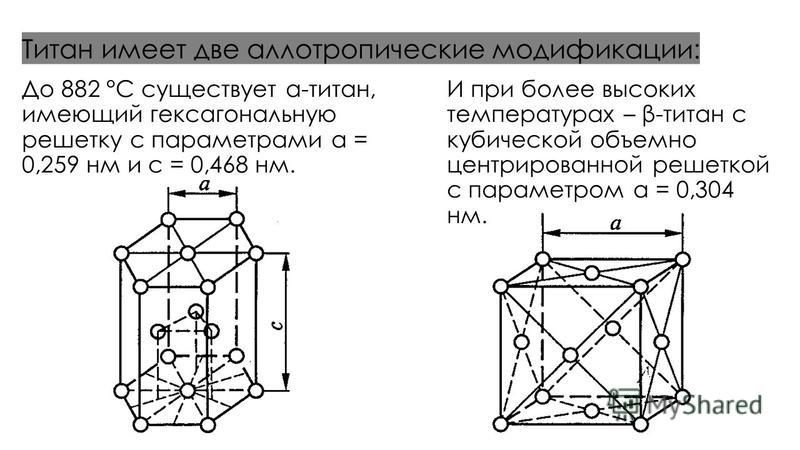
Аллотропические
превращения происходят в железе, олове,
титане, кобальте и других металлах.
Медь, алюминий не претерпевают
аллотропических превращений. Сущность
аллотропии состоит в том, что при
определенных температурах в твердом
металле возникают новые центры
кристаллизации, в процессе роста которых
образуется новая решетка. Формирование
новой решетки происходит с поглощением
тепла при нагревании и с выделением
тепла при охлаждении. Поэтому в период
перестройки решетки температура остается
неизменной и на кривой охлаждения
характеризуется горизонтальной
площадкой.
Различные формы
кристаллической решетки для данного
металла называются модификациями.
Модификацию, существующую при
низких температурах, обозначают буквой
а.
Важнейшее значение в технике
имеют аллотропические превращения в
железе.
До 1535° железо остается
жидким, а при 1535° начинается кристаллизация
железа. После затвердевания образуется
решетка объемноцентрированного куба
б-железа с параметром 2,93 А. Эта решетка
сохраняется до 1390°, после чего происходит
перестройка ее на новую модификацию у,
имеющую гранецентрированную кубическую
решетку с параметром 3,65 А. Ниже температуры
Ниже температуры
910° железо неустойчиво и переходит в
новую форму, имеющую объемноцентрированную
кубическую решетку с параметром 2,9 А.
При температуре 768° происходит последняя
температурная остановка, но она связана
не с перестройкой решетки, а с образованием
модификации а и появлением магнитных
свойств.
В кристаллах
всегда имеются дефекты (несовершенства)
строения, обусловленные нарушением
правильного расположения атомов
кристаллической решетки. Дефекты
кристаллического строения подразделяют
по геометрическим признакам
на точечные, линейные и поверхностные.
Атомы совершают колебательные
движений возле узлов решетки, и с
повышением температуры амплитуда этих
колебаний увеличивается. Большинство
атомов данной кристаллической решетки
имеют одинаковую (среднюю) энергию и
колеблются при данной температуре с
одинаковой амплитудой. Однако
отдельные атомы обладают энергией,
значительно большей средней энергии,
и перемещаются из одного места в другое.
Наиболее легко перемещаются атомы
поверхностного слоя, выходя на
поверхность. Место, где находился такой
атом, называется вакансией (рис. 2, а).
Рис.
2. Дефекты в кристаллах:
а — вакансия,
б — внедренный атом, в краевая
линейная дислокация, г — неправильное
расположение атомов на границе зерен
1 и 2
На это место
через некоторое время перемещается
один из атомов соседнего слоя и т. д.
Таким образом вакансия перемещается в
глубь кристалла. С повышением температуры
количество вакансий увеличивается
и они чаще перемещаются из одного
узла в другой. В диффузионных процессах,
протекающих в металлах, вакансии
играют определяющую роль. К точечным
дефектам относят также атом, внедренный
в междоузлие кристаллической решетки
(рис. 2, б), и замещенный атом, когда место
атома одного металла замещается в
кристаллической решетке другим,
чужеродным атомом. Точечные дефекты
вызывают местное искажение кристаллической
решетки.
Линейные дефекты являются
другим важнейшим видом несовершенства
кристаллической решетки, когда в
результате сдвига на одно межатомное
расстояние одной части решетки
относительно другой вдоль какой-либо
плоскости число рядов атомов в верхней
части решетки на один больше, чем в
нижней.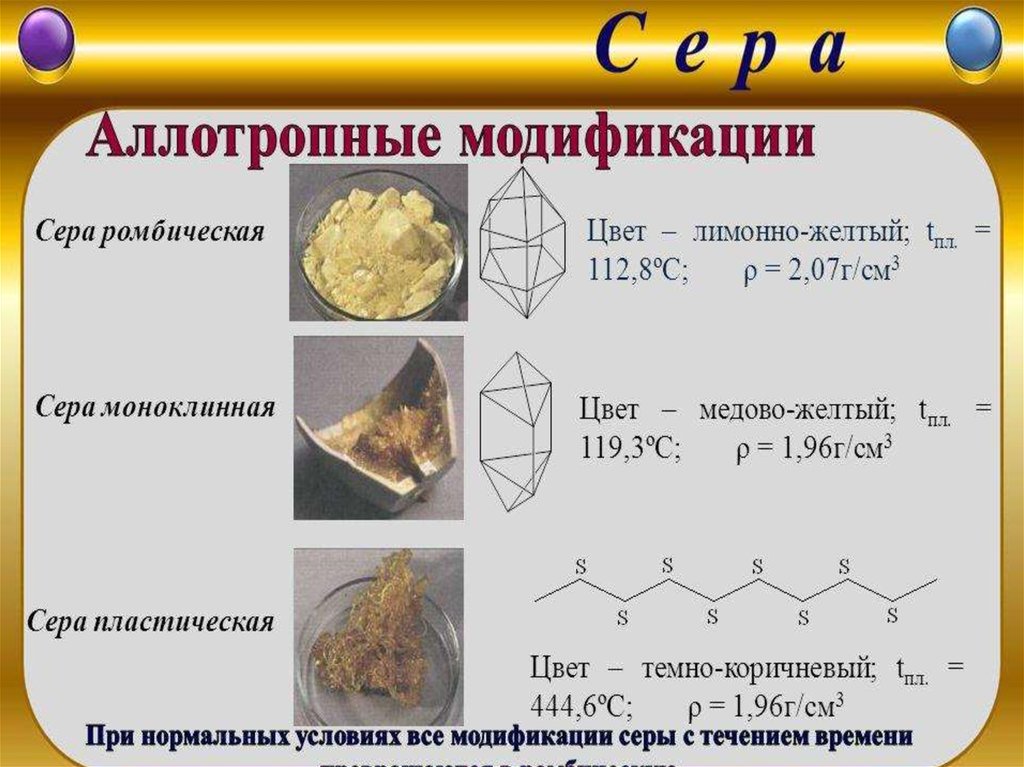 В данном случае в верхней части
В данном случае в верхней части
решетки появилась как бы лишняя
атомная плоскость (экстраплоскость).
Край экстраплоскости, перпендикулярный
направлению сдвига, называется
краевой, или линейной, дислокацией (рис.
2, в), длина которой может достигать
многих тысяч межатомных расстояний.
Шириной дислокации считают расстояние
от центра дефекта до места решетки без
искажения. Ширина дислокации мала и
составляет несколько атомных расстояний.
Кристаллическая решетка в зоне
дислокации упруго искажена, поскольку
атомы в этой зоне смещены относительно
их равновесного состояния. Для
дислокации характерна их легкая
подвижность. Это объясняется тем,
что атомы, образующие дислокацию,
стремятся переместиться в равновесное
состояние. Дислокации образуются в
процессе кристаллизации металлов (см.
гл.1, § 2), а также при пластической
деформации, термической обработке
и других процессах.
Поверхностные
дефекты представляют собой границы
раздела между отдельными кристаллами
(рис. 2, г). На границе раздела атомы
кристалла расположены менее правильно,
чем в его объеме. Кроме того, по границам
Кроме того, по границам
раздела скапливаются дислокации и
вакансии, а также концентрируются
примеси, что еще больше наpyшает порядок
расположения атомов. При этом сами
кристаллы разориентированы, т. е. могут
быть повернуты относительно друг друга
на десятки градусов. Прочность металла
может либо увеличиваться вследствие
искажений кристаллической решетки
вблизи границ, либо уменьшаться из-за
наличия примесей и концентрации
дефектов. Дефекты в кристаллах
существенно влияют на свойства
металлов.
Анизотропия
кристаллов. Неодинаковость физических
свойств среды в разных направлениях
называют анизотропией. Анизотропия
кристаллов обусловлена различаем
плотности упаковки атомов в решетке
в различных направлениях. Все кристаллы
анизотропны, а аморфные тела (стекло,
смола) изотропны, т. е. имеют одинаковую
плотность атомов в различных направлениях.
Анизотропия свойств важна при
использовании монокристаллов —
одиночных кристаллов, частицы которых
расположены единообразно по всему их
объему.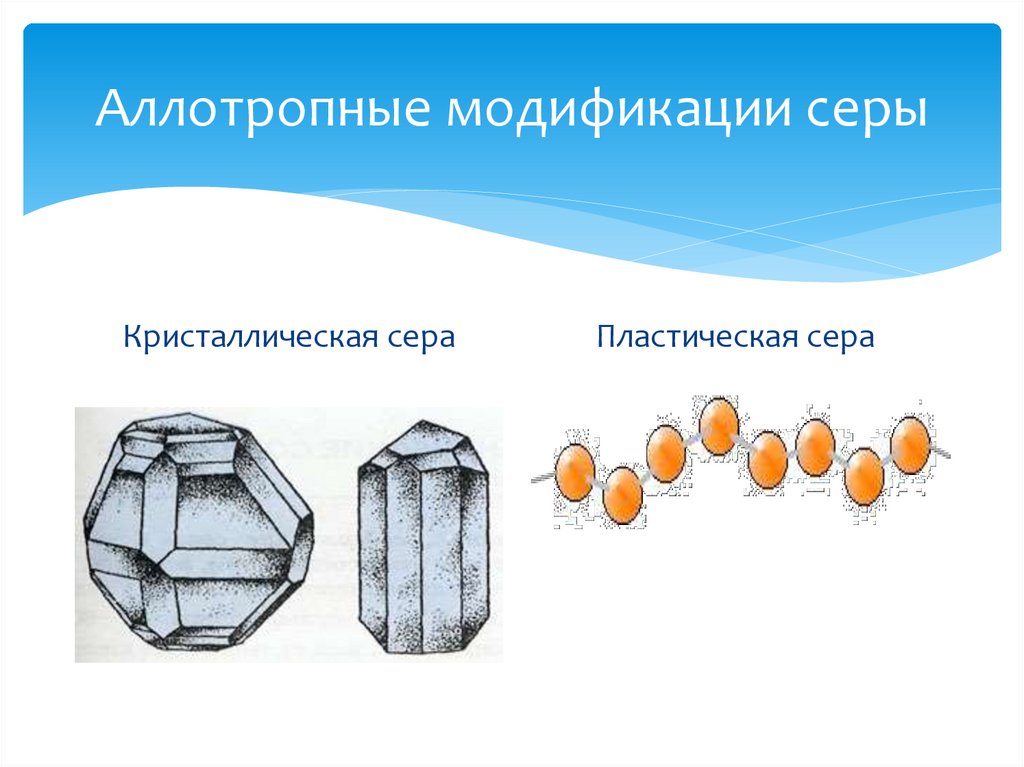 Монокристаллы имеют правильную
Монокристаллы имеют правильную
кристаллическую огранку (в форме
естественных многогранников),
анизотропны по механическим,
электрическим и другим физическим
свойствам.
Металлы и сплавы, применяемые
в технике, обычно имеют поликристаллическую
структуру, т. е. состоят из множества
мелких и различно ориентированных
кристаллов, не имеющих правильной
кристаллической огранки и называемых
кристаллитами (или зернами). В каждом
зерне поликристалла наблюдается
анизотропия. Однако вследствие
разнообразной, беспорядочной ориентировки
кристаллографических плоскостей в
различных зернах поликристалл может
иметь одинаковые свойства по разным
направлениям и не обнаруживать
анизотропию (когда размеры зерен
значительно меньше размеров пол и
кристалла и количество их весьма велико).
Это обстоятельство во многих случаях
позволяет рассматривать поликристаллическое
тело как подобное изотропному, несмотря
на анизотропию свойств отдельных
составляющих его зерен.
9
Упругая и пластическая деформация.
Деформация
– это изменение формы и размеров тела,
деформация может вызываться воздействием
внешних сил, а также другими
физико-механическими процессами, которые
происходят в теле. К деформациям относятся
такие явления, как сдвиг, сжатие,
растяжение, изгиб и кручение.
Упругая
деформация – это деформация, которая
исчезает после снятия нагрузки. Упругая
деформация не вызывает остаточных
изменений в свойствах и структуре
металла; под действием приложенной
нагрузки происходит незначительное
обратимое смещение атомов.
При
растяжении монокристалла возрастают
расстояния между атомами, а при сжатии
атомы сближаются. При смещении атомов
из положения равновесия нарушается
баланс сил притяжения и электростатического
отталкивания. После снятия нагрузки
смещенные атомы из-за действия сил
притяжения или отталкивания возвращаются
в исходное равновесное состояние и
кристаллы приобретают первоначальные
размеры форму.
Деформация
может быть упругой, исчезающей после
снятия нагрузки, и пластической,
остающейся после снятия нагрузки.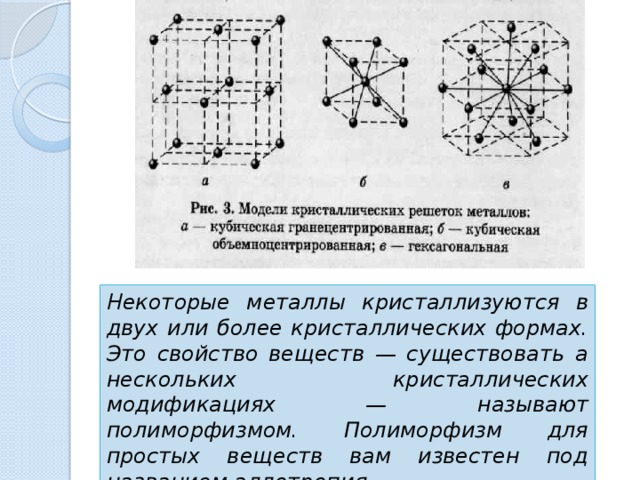
Самое
малое напряжение вызывает деформацию,
причем начальные деформации являются
всегда упругими и их величина находится
в прямой зависимости от напряжения.
Основными механическими свойствами
являются прочность, пластичность,
упругость.
Важное
значение имеет пластичность, она
определяет возможность изготовления
изделий различными способами обработки
давлением. Эти способы основаны на
пластическом деформировании металла.
Материалы,
которые имеют повышенную пластичность,
менее чувствительны к концентраторам
напряжений. Для этого проводят
сравнительную оценку различных металлов
и сплавов, а также контроль их качества
при изготовлении изделий.
Физическая
природа деформации металлов
Под
действием напряжений происходит
изменение формы и размеров тела.
Напряжения возникают при действии на
тело внешних сил растяжения, сжатия, а
также в результате фазовых превращений
и некоторых других физико-химических
процессов, которые связанны с изменением
объема.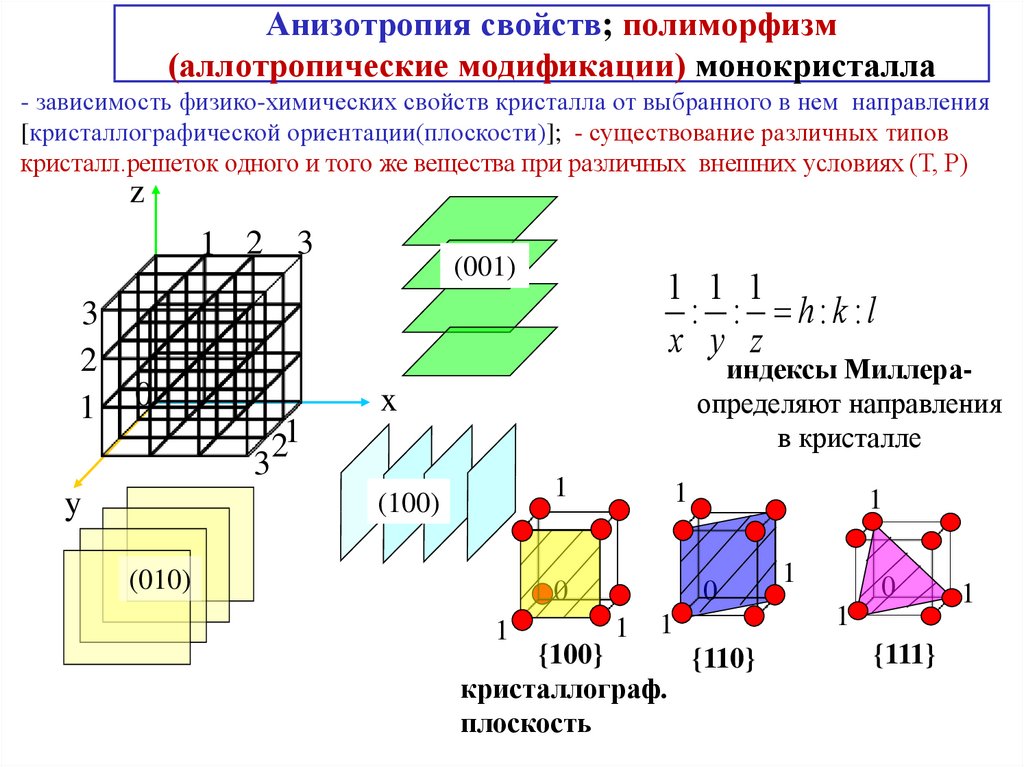 Металл, который находится в
Металл, который находится в
напряженном состоянии, при любом виде
напряжения всегда испытывает напряжения
нормальные и касательные, деформация
под действием напряжений может быть
упругой и пластической. Пластическая
происходит под действием касательных
напряжений.
Упругая
– это такая деформация, которая после
прекращения действия, вызвавшего
напряжение, исчезает полностью. При
упругом деформировании происходит
изменение расстояний между атомами в
кристаллической решетке металла.
С
увеличением межатомных расстояний
возрастают силы взаимного притяжения
атомов. При снятии напряжения под
действием этих сил атомы возвращаются
в исходное положение. Искажение решетки
исчезает, тело полностью восстанавливает
свою форму и размеры. Если нормальные
напряжения достигают значения сил
межатомной связи, то произойдет хрупкое
разрушение путем отрыва. Упругую
деформацию вызывают небольшие касательные
напряжения.
Пластической
называется деформация, остающаяся
после прекращения действия вызвавших
ее напряжений. При пластической деформации
При пластической деформации
в кристаллической решетке металла под
действием касательных напряжений
происходит необратимое перемещение
атомов. При небольших напряжениях атомы
смещаются незначительно и после снятия
напряжений возвращаются в исходное
положение. При увеличении касательного
напряжения наблюдается необратимое
смещение атомов на параметр решетки,
т. е. происходит пластическая
деформация.
При
возрастании касательных напряжений
выше определенной величины деформация
становится необратимой. При снятии
нагрузки устраняется упругая составляющая
деформации. Часть деформации, которую
называют пластической, остается.
При
пластической деформации необратимо
изменяется структура металла и его
свойства. Пластическая деформация
осуществляется скольжением и
двойникованием.
Скольжение
в кристаллической решетке протекает
по плоскостям и направлениям с плотной
упаковкой атомов, где сопротивление
сдвигу наименьшее. Это объясняется тем,
что расстояние между соседними атомными
плоскостями наибольшее, т.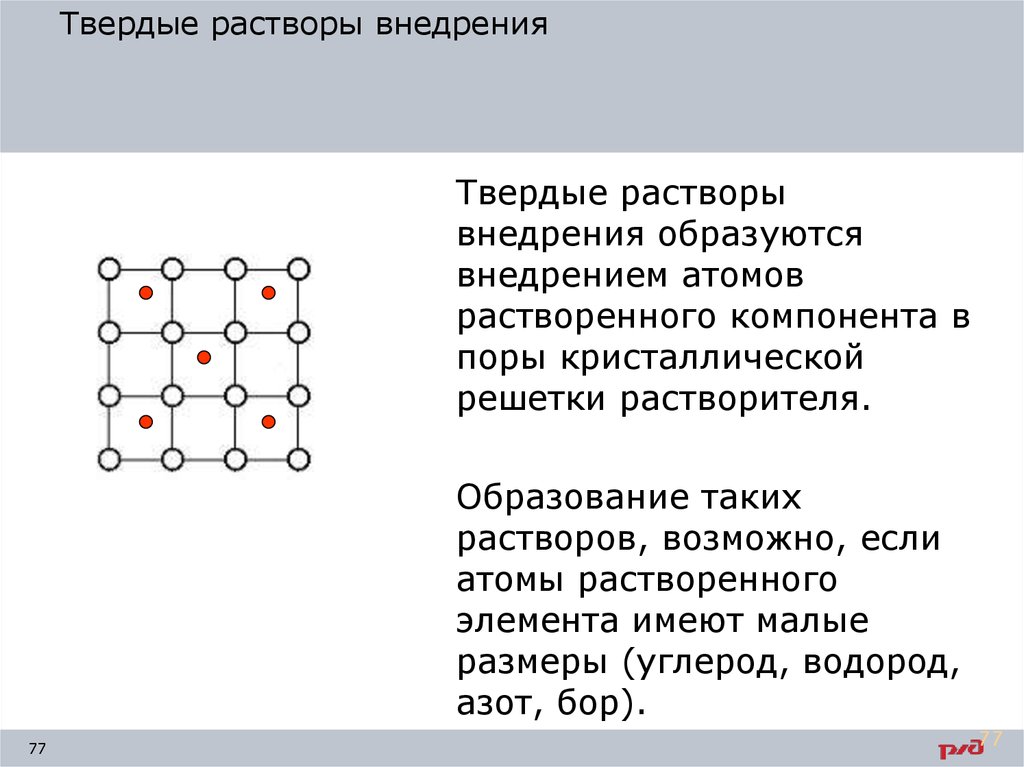 е. связь
е. связь
между ними наименьшая. Плоскости
скольжения и направления скольжения,
лежащие в этих плоскостях, образуют
систему скольжения. В металлах могут
действовать одна или одновременно
несколько систем скольжения.
Металлы
с кубической кристаллической решеткой
(ГЦК и ОЦК) обладают высокой пластичностью,
скольжение в них происходит во многих
направлениях.
Процесс
скольжения не следует представлять как
одновременное передвижение одной части
кристалла относительно другой, оно
осуществляется в результате перемещения
в кристалле дислокаций. Перемещение
дислокации в плоскости скольжения ММ
через кристалл приводит к смещению
соответствующей части кристалла на
одно межплоскостное расстояние, при
этом справа на поверхности кристалла
образуется ступенька.
Аллотропия металлов (с диаграммой)
РЕКЛАМА:
В этой статье мы поговорим об аллотропии металлов.
Многие металлические элементы (даже такие соединения, как кремнезем и т. д. ) существуют более чем в одной кристаллической форме (но по одной за раз) в зависимости от внешних условий температуры или давления, или того и другого. Это явление называется полиморфизмом или аллотропией. Множественные кристаллические структуры одного и того же состава обычно называют полиморфами.
) существуют более чем в одной кристаллической форме (но по одной за раз) в зависимости от внешних условий температуры или давления, или того и другого. Это явление называется полиморфизмом или аллотропией. Множественные кристаллические структуры одного и того же состава обычно называют полиморфами.
Термин «аллотропия» обычно используется для обозначения такого поведения чистых элементов, в то время как полиморфизм является более общим термином. Различные фазы называются аллотропами. Это изменение может также произойти в некоторых элементах, когда они подвергаются необычной термической или механической обработке.
РЕКЛАМА:
При нормальных условиях атмосферного давления каждая аллотропная форма металла с определенной кристаллической структурой существует в равновесии в диапазоне температур, а затем переходит в другую кристаллическую форму при критической температуре.
Обычно аллотроп, стабильный при самой низкой температуре, обозначается греческой буквой-α (альфа), предшествующей химическому символу металла, например α-Fe. Следующая более высокая температурная модификация называется β, затем γ и при еще более высоких температурах как δ (дельта). На рис. 1.44 показаны аллотропные изменения железа при изменении температуры при атмосферном давлении. Ниже 910°C железо имеет кристаллическую структуру ОЦК и называется α-железом. Но выше 910°С железо называют γ-железом с кристаллической структурой ГЦК.
Следующая более высокая температурная модификация называется β, затем γ и при еще более высоких температурах как δ (дельта). На рис. 1.44 показаны аллотропные изменения железа при изменении температуры при атмосферном давлении. Ниже 910°C железо имеет кристаллическую структуру ОЦК и называется α-железом. Но выше 910°С железо называют γ-железом с кристаллической структурой ГЦК.
При 1394°C γ-железо переходит в δ-железо (структура ОЦК), второе аллотропное превращение. Рис. 1.44 (b) иллюстрирует, что по мере того, как свободная энергия фазы становится меньше при температуре, она становится устойчивой, и более ранняя фаза превращается в эту стабильную фазу. Почти все свойства меняются при переходе металла из одной аллотропной формы в другую. Рис. 1.44 (в) иллюстрирует изменение объема при изменении аллотропных форм (при изменении температуры).
Полиморфное или аллотропное изменение — это фазовый переход, такой же, как переход из жидкой фазы в твердую. Таким образом, как и в процессе замораживания, здесь также наблюдаются два явления: а) переохлаждение, б) выделение теплоты реакции. Оба эти эффекта наблюдаются и при фазовых превращениях в твердом состоянии, т. е. при полиморфных изменениях.
Оба эти эффекта наблюдаются и при фазовых превращениях в твердом состоянии, т. е. при полиморфных изменениях.
РЕКЛАМА:
Переохлаждение – это задержка фазового перехода до температуры ниже температуры равновесия. Жидкости переохлаждаются на несколько градусов, прежде чем произойдет замерзание, но твердые тела могут быть переохлаждены в гораздо большей степени, прежде чем образуется новая фаза. Новые кристаллы, образующиеся в результате аллотропного превращения, имеют различный размер и форму.
Например, если металл нагреть до температуры чуть больше критической температуры полиморфного превращения, например, α-железо нагреть до температуры чуть больше 910°С образуются мелкие зерна g-железа. Таким образом, фазовое превращение способствует измельчению зерен, если раньше у нас были крупные зерна.
Аллотропные превращения в металлах очень часто изучают методом термического анализа, который заключается в обнаружении отклонений от нормальной кривой охлаждения (или нагревания) вещества за счет выделения (или поглощения) теплоты реакции при фазовом превращении. Таким образом, отклонение от нормальной кривой охлаждения указывает на протекание фазового превращения.
Таким образом, отклонение от нормальной кривой охлаждения указывает на протекание фазового превращения.
РЕКЛАМА:
Аллотропные изменения происходят при резком изменении всех свойств металлов и сплавов, таких как удельный объем, теплопроводность, электропроводность, магнитные свойства; механические и химические свойства и т. д. В табл. 1.7 показаны некоторые металлы, имеющие различную кристаллическую структуру вследствие полиморфных изменений.
Проблема:
Титан претерпевает изменение фазы ОЦК в ГПУ при 880°C при охлаждении. Рассчитайте % изменения объема. При заданных параметрах решетки
РЕКЛАМА:
a ВСС = 3,32 А,
и HCP = 2,956 А и с = 4,683 А.
Решение:
Наша основа – элементарные ячейки обеих кристаллических структур. В структуре ОЦК на элементарную ячейку приходится 2 атома, а в структуре ГПУ — 6 атомов на элементарную ячейку. Поскольку число атомов после фазового превращения остается прежним, поэтому 3 элементарные ячейки ОЦК дают одну элементарную ячейку ГПУ.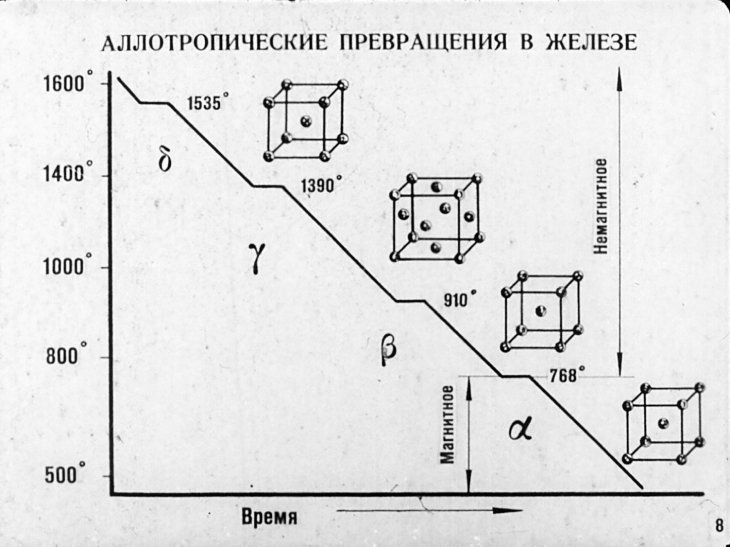 Найдем объем одной элементарной ячейки ГПУ и трех элементарных ячеек ОЦК и найдем разницу объемов.
Найдем объем одной элементарной ячейки ГПУ и трех элементарных ячеек ОЦК и найдем разницу объемов.
РЕКЛАМА:
Объем 3-элементных потолков BCC = 3(3,32 А) 3
= 109,8 А 3
Объем элементарной ячейки ГПУ- В плоскости базиса имеется шесть равносторонних треугольников. Таким образом, объем одной элементарной ячейки HCP
Таким образом, происходит сжатие, когда титан (ОЦК) превращается в титан (ГПУ) при охлаждении. Сжатие также происходит, когда α-Fe превращается в γ-Fe при нагревании, как показано на рис. 1.29.(в), когда резкое уменьшение объема происходит при 910°С.
Полиморфные превращения также были вызваны применением высоких давлений. Превращения при повышении давления обычно дают более плотную кристаллическую структуру (плотноупакованную), что также соответствует принципу Ле Шателье.
Чистое железо при одном атмосферном давлении, как мы видели, существует в виде альфа (ОЦК) и гамма (ГЦК) железа, но переходит в новую кристаллическую фазу ГПУ (ԑ) при давлениях выше 100 кбар с а = 2,95 А°, с = 3,93 А° и с/а = 1,61.
Полиморфное изменение можно разделить на два класса в зависимости от обратимости изменения:
(i) Энантиотропия (греческое слово — противоположное изменение):
Полиморфы называются энантиотропными, когда каждый из них имеет определенный диапазон стабильности, и одна форма обратимо переходит в другую в определенных точках перехода, определяемых давлением или температурой, как это происходит в случае железа. Этот тип изменений распространен. Например- Fe, Ti и т.д.
(ii) Монотропия (греческое слово — одно изменение):
Монотропия – это состояние, когда один полиморф стабилен, а другой метастабилен на всем протяжении существования. Здесь только метастабильная форма может перейти в стабильную форму. Например, фосфор.
Кинетика полиморфных изменений колеблется в широких пределах от бесконечности до нуля. Преимущества получаются, если метастабильная форма может продолжать существовать за пределами диапазона стабильности, особенно если эта форма обладает более желательными свойствами.