Читать реферат по химии: "Аллотропные модификации". Аллотропия металлов реферат по химии
Аллотропия металлов — реферат
Аллотропия металлов
аллотропический физический свойство металл
Введение
Аллотропией, или полиморфизмом, называют способность металла в твердом состоянии иметь различные кристаллические формы. Процесс перехода из одной кристаллической формы в другую называют аллотропическим превращением. При нагреве чистого металла такое превращение сопровождается поглощением тепла и происходит при постоянной температуре, что связано с необходимостью затраты определенной энергии на перестройку кристаллической решетки. Аллотропические превращения имеют многие металлы: железо, олово, титан и др. Например, железо в интервале температур 911 -1392°С имеет гранецентрированную кубическую решетку (ГЦК) г-Fe (рис. 7). В интервалах до 911°С и от 1392 до 1539°С железо имеет объемно-центрированную кубическую решетку (ОЦК) - б-Fe. Аллотропические формы металла обозначаются буквами а, в, г и т. д. Существующая при самой низкой температуре аллотропическая форма металла обозначается через букву б, которая в виде индекса добавляется к символу химического элемента металла и т. д.
При аллотропических превращениях происходит изменение свойств металлов - изменение объема металлов (особенно характерно для олова) и растворимости углерода (характерно для железа).
Методы изучения строения металлов
Изучение строения металлов и сплавов производится методами макро- и микроанализа, рентгеновского, а также дефектоскопии (рентгеновской, магнитной, ультразвуковой).
Методом макроанализа изучается макроструктура, т. е. структура, видимая невооруженным глазом или с помощью лупы, при этом выявляются крупные дефекты: трещины, усадочные раковины, газовые пузыри и т. д., а также неравномерность распределения примесей в металле. Макроструктуру определяют по изломам металла, по макрошлифам. Макрошлиф - это образец металла или сплава, одна из сторон которого отшлифована, тщательно обезжирена, протравлена и рассматривается с помощью лупы с увеличением в 5 -10х.
Микроанализ выявляет структуру металла или сплава по микрошлифам, приготовленным так же, как и для макроанализа, но дополнительно отполированным до зеркального блеска. Шлифы рассматривают в отраженном свете под оптическим микроскопом при увеличении до 3000х. Из-за различной ориентировки зерен металла они травятся не в одинаковой степени и под микроскопом свет также отражается неодинаково. Границы зерен благодаря примесям травятся сильнее, чем основной металл, и выявляются более рельефно. В сплаве структурные составляющие травятся также различно. В электронном микроскопе рассматривают реплику - слепок с особо тонкой структуры блоков, фрагментов, дислокации при увеличениях до 100000х. Этот важнейший анализ определяет размеры и форму зерен, структурные составляющие, неметаллические включения и их характер (трещины, пористость и т. д.), качество термической, обработки. Зная микроструктуру, можно объяснить причины изменения свойств металла.
С помощью рентгеновского анализа изучают атомную структуру металлов, типы и параметры кристаллических решеток, а также дефекты, лежащие в глубине. Этот анализ, основанный на дифракции (отражении) рентгеновских лучей рядами атомов кристаллической решетки, позволяет обнаружить дефекты (пористость, трещины, газовые пузыри, шлаковые включения и т. д.), не разрушая металла. В местах дефектов рентгеновские лучи поглощаются меньше, чем в сплошном металле, и поэтому на фотопленке такие лучи образуют темные пятна, соответствующие форме дефекта.
Для исследования структуры металла и дефектов изделий широко применяют гамма-лучи, которые проникают в изделие на большую глубину, чем рентгеновские.
Магнитным методом исследуют дефекты в магнитных металлах (сталь, никель и др.) на глубине до 2 мм (трещины различного происхождения, неметаллические включения и т. д.). Для этого испытуемое изделие намагничивают, покрывают его поверхность порошком железа, осматривают поверхность и размагничивают изделие. Вокруг дефекта образуется неоднородное поле, вследствие чего магнитный порошок повторяет очертания дефекта. Другой метод - магнитный индукционный - часто используют для оценки полноты структурных превращений в сплавах (изделиях) после их термической обработки.
Ультразвуковым методом осуществляется эффективный контроль качества металла изделий и заготовок практически любых размеров. В импульсных ультразвуковых дефектоскопах ультразвуковая волна от щупа - излучателя распространяется в контролируемом изделии и при встрече с каким-либо дефектом отражается от него. При этом отраженные волны принимаются, усиливаются и передаются на показывающий индикатор. Ультразвук используют для контроля качества роторов, рельсов, поковок, проката и других изделий при необходимости сохранения целостности изделий.
Физические и химические свойства
Физические свойства. К физическим свойствам металлов относят цвет, плотность, температуру плавления, теплопроводность, тепловое расширение, теплоемкость, электропроводность, магнитные свойства и др.
Цветом называют способность металлов отражать световое излучение с определенной длиной волны. Например, медь имеет розово-красный цвет, алюминий - серебристо-белый.
Плотность металла характеризуется его массой, заключенной в единице объема. По плотности все металлы делят на легкие (менее 4500 кг/м3) и тяжелые. Плотность имеет большое значение при создании различных изделий. Например, в самолето- и ракетостроении стремятся использовать более легкие металлы и сплавы (алюминиевые, магниевые, титановые), что способствует снижению массы изделий.
Температурой плавления называют температуру, при которой металл переходит из твердого состояния в жидкое. По температуре плавления различают тугоплавкие металлы (вольфрам 3416° С, тантал 2950°С, титан 1725°С. и др.) и легкоплавкие (олово 232°С, свинец 327°С, цинк 419,5°С, алюминий 660°С). Температура плавления имеет большое значение при выборе металлов для изготовления литых изделий, сварных и паяных соединений, термоэлектрических приборов и других изделий. В единицах СИ температуру плавления выражают в градусах Кельвина (К).
Теплопроводностью называют, способность металлов передавать тепло от более нагретых к менее нагретым участкам тела. Серебро. медь, алюминий обладают большой теплопроводностью. Железо имеет теплопроводность примерно в три раза меньше, чем алюминий, и в пять раз меньше, чем медь. Теплопроводность имеет большое значение при выборе материала для деталей. Например, если металл плохо проводит тепло, то при нагреве и быстром охлаждении (термическая обработка, сварка) в нем образуются трещины. Некоторые детали машин (поршни двигателей, лопатки турбин) должны быть изготовлены из материалов с хорошей тeплопpoводностью. В единицах СИ теплопроводность имеет размерность Вт/ (м*К).
Тепловым расширением называют способность металлов увеличиваться в размерах при нагревании и уменьшаться при охлаждении. Тепловое расширение характеризуется коэффициентом линейного расширения б = (l2 -l 1)/ [l 1 (t 2 - t 1)], где l 1 и l 2 длины тела при температурах t 1 и t 2. Коэффициент объемного расширения равен 3 б. Тепловые расширения должны учитываться при сварке, ковке и горячей объемной штамповке, изготовлении литейных форм, штампов, прокатных валков, калибров, выполнении точных соединений и сборке приборов, при строительстве мостовых ферм, укладке железнодорожных рельс.
Теплоемкостью называют способность металла при нагревании поглощать определенное количество тепла. В единицах СИ имеет размерность Дж/К. Теплоемкость различных металлов сравнивают по величине удельной теплоемкости - количеству тепла, выраженному в больших калориях, которое требуется для повышения температуры 1 кг металла на 1°С (в единицах СИ - Дж/(кг.К).
Электрическая проводимость оценивается в системе СИ в сименсах (См), удельная электропроводность - в См/м.
Электросопротивление выражают в Омах (Ом), а удельное электросопротивление - в Ом/м.
Хорошая электропроводность необходима, например, для токоведущих проводов (медь, алюминий). При изготовлении электронагревателей приборов и печей необходимы сплавы с высоким электросопротивлением (нихром, константан, манганин). С повышением температуры металла его электропроводность уменьшается, а с понижением - увеличивается.
Магнитные свойства характеризуются абсолютной магнитной проницаемостью или магнитной постоянной, т. е. способностью металлов намагничиваться. В единицах СИ магнитная постоянная имеет размерность Гн/м. Высокими магнитными свойствами обладают железо, никель, кобальт и их сплавы, называемые ферромагнитными. Материалы с магнитными свойствами применяют в электротехнической аппаратуре и для изготовления магнитов.
Химические свойства. Химические свойства характеризуют способность металлов и сплавов сопротивляться окислению или вступать в соединение с различными веществами: кислородом воздуха, растворами кислот, щелочей и др. Чем легче металл вступает в соединение с другими элементами, тем быстрее он разрушается. Химическое разрушение металлов под действием на их поверхность внешней агрессивной среды называют коррозией.
Металлы, стойкие к окислению при сильном нагреве, называют жаростойкими или окалиностойкими. Такие металлы применяют для изготовления деталей, которые эксплуатируются в зоне высоких температур.
Сопротивление металлов коррозии, окалине-образованию и растворению определяют по изменению массы испытуемых образцов на единицу поверхности за единицу времени.
Химические свойства металлов обязательно учитываются при изготовлении тех или иных изделий. Особенно это относится к изделиям или деталям, работающим в химически агрессивных средах.
Механические свойства
Способность металла сопротивляться воздействию внешних сил характеризуется механическими свойствами. Поэтому при выборе материала для изготовления деталей машин необходимо прежде всего учитывать его механические свойства: прочность, упругость, пластичность, ударную вязкость, твердость и выносливость. Эти свойства определяют по результатам механических испытаний, при которых металлы подвергают воздействию внешних сил (нагрузок). Внешние силы могут быть статическими, динамическими или циклическими (повторно-переменными). Нагрузка вызывает в твердом теле напряжение и деформацию.
Напряжение - величина нагрузки, отнесенная к единице площади поперечного сечения испытуемого образца. Деформация - изменение формы и размеров твердого тела под влиянием приложенных внешних сил. Различают деформации растяжения (сжатия), изгиба, кручения, среза (рис. 8).
В действительности материал может подвергаться одному или нескольким видам деформации одновременно.
Для определения прочности, упругости и пластичности металлы в виде образцов круглой или плоской формы испытывают на статическое растяжение. Испытания проводят на разрывных машинах. В результате испытаний получают диаграмму растяжения. По оси абсцисс этой диаграммы откладывают значения деформации, а по оси ординат - нагрузки, приложенные к образцу.
Прочность - способность материала сопротивляться разрушению под действием нагрузок оценивается пределом прочности и пределом текучести. Важным показателем прочности материала является также удельная прочность - отношение предела прочности материала к его плотности. Предел прочности у в (временное сопротивление) - это условное напряжение в Па (Н/м2). соответствующее наибольшей нагрузке, предшествующей разрушению образца: у в = P max / F о, где Рmах - наибольшая нагрузка, Н; Fо - начальная площадь поперечного сечения рабочей части образца, м2.
Истинное сопротивление разрыву S к - это напряжение, определяемое отношением нагрузки Рк в момент разрыва к площади минимального поперечного сечения образца после разрыва F к (S к = Р к/ F к).
Предел текучести (физический) у т - это наименьшее напряжение (в МПа), при котором образец деформируется без заметного увеличения нагрузки:
у т = Р т F о, где Р т - нагрузка, при которой наблюдается площадка текучести, Н.
Площадку текучести имеют в основном только малоуглеродистая сталь и латуни. Другие сплавы площадки текучести не имеют. Для таких материалов определяют предел текучести (условный), при котором остаточное удлинение достигает 0,2 % от расчетной длины образца: у 0,2 = P 0,2 / F 0.
Упругость - способность материала восстанавливать первоначальную форму и размеры после прекращения действия нагрузки Р уп оценивают пределом пропорциональности у пц и пределом упругости у ун.
Предел пропорциональности у пц - напряжение (МПа), выше которого нарушается пропорциональность между прилагаемым напряжением и деформацией образца у пц = Р пц / Р 0.
Предел упругости (условный) у 0,05 - это условное напряжение в Мпа, соответствующее нагрузке, при которой остаточная деформация впервые достигает 0,05 %, от расчетной длины образца lo: у 0,05 = P 0,05 / F 0, где P 0,05 - нагрузка предела упругости, Н.
Пластичность, т.е. способность материала принимать новую форму и размеры под действием внешних сил не разрушаясь, характеризуется относительным удлинением и относительным сужением.
Относительное удлинение (после разрыва) д - это отношение приращения (l k - lo) расчетной длины образца после разрыва к его первоначальной расчетной длине lo, выраженное в процентах: д = ((1к -1о)/1о] 100 %.
Относительное сужение (после разрыва) Ш - это отношение разности начальной и минимальной площадей (Fo - Fк) поперечного сечения образца после разрыва к начальной площади Fo поперечного сечения, выраженное в про центах: Ш = [( F 0 - F k) / Fо] 100%.
yaneuch.ru
Аллотропия металлов — реферат
Чем больше значения относительного удлинения и сужения для материала, тем он более пластичен. У хрупких материалов эти значения близки к нулю. Хрупкость конструкционного материала является отрицательным свойством.
Ударная вязкость, т. е. способность материала сопротивляться динамическим нагрузкам, определяется как отношение затраченной на излом образца работы W (в МДж) к площади его поперечного сечения F (в м2) в месте надреза KC=W/F.
Для испытания изготовляют специальные стандартные образцы, имеющие форму квадратных брусочков с надрезом. Испытывают образец на маятниковых копрах. Свободно падающий маятник копра ударяет по образцу со стороны, противоположной надрезу. При этом фиксируется работа.
Определение ударной вязкости особенно важно для некоторых металлов, работающих при минусовых температурах и проявляющих склонность к хладноломкости. Чем ниже порог хладноломкости, т. е. температура, при которой вязкое разрушение материала переходит в хрупкое, и больше запас вязкости материала, тем больше ударная вязкость материала. Хладноломкость-снижение ударной вязкости при низких температурах.
Циклическая вязкость - это способность материалов поглощать энергию при повторно-переменных нагрузках. Материалы с высокой циклической вязкостью быстро гасят вибрации, которые часто являются причиной преждевременного разрушения. Например, чугун, имеющий высокую циклическую вязкость, в некоторых случаях (для станин и других корпусных деталей) является более ценным материалом, чем углеродистая сталь.
Твердостью называют способность материала сопротивляться проникновению в него другого, более твердого тела. Высокой твердостью должны обладать металлорежущие инструменты: резцы, сверла, фрезы, а также поверхностно-упрочненные детали. Твердость металла определяют способами Бринелля, Роквелла и Виккерса (рис. 10).
Способ Бринелля основан на том, что в плоскую поверхность металла вдавливают под постоянной нагрузкой стальной закаленный шарик. Диаметр шарика и величину нагрузки устанавливают в зависимости от твердости и толщины испытываемого металла. Твердость по Бринеллю определяют на твердомере ТШ (твердомер шариковый). Испытание проводят следующим образом. На поверхности образца, твердость которого нужно измерить, напильником или абразивным кругом зачищают площадку размером 3 -5 см2. Образец ставят на столик прибора и поднимают до соприкосновения со стальным шариком, который укреплен в шпинделе прибора. Груз опускается и вдавливает шарик в испытываемый образец. На поверхности металла образуется отпечаток. Чем больше отпечаток, тем металл мягче.
За меру твердости НВ принимают отношение нагрузки к площади поверхности отпечатка диаметром d и глубиной t, который образуется при вдавливании силой Р шарика диаметра D (см. рис. 10,а).
Числовое значение твердости определяют так: измеряют диаметр отпечатка с помощью оптической лупы (с делениями) и по полученному значению находят в таблице, приложенной к ГОСТу, соответствующее число твердости.
Преимущество способа Бринелля заключается в простоте испытания и точности получаемых результатов. Способом Бринелля не рекомендуется измерять твердость материалов с НВ>450, например закаленной стали, так как при измерении шарик деформируется и показания искажаются.
Для испытания твердых материалов применяют способ Роквелла. В образец вдавливают алмазный конус с углом при вершине 120° или стальной закаленный шарик диаметром 1,59 мм. Твердость по Роквеллу измеряется в условных единицах. Условная величина единицы твердости соответствует осевому перемещению наконечника на 0,002 мм. Испытание проводят на приборе ТК. Значение твердости определяется по глубине отпечатка h и отсчитывают по циферблату индикатора, установленному на приборе. Во всех случаях предварительная нагрузка Ро равна 100 H.
При испытании металлов с высокой твердостью применяют, алмазный конус и общую нагрузку P = Po + P 1= 1500 H. Твердость отсчитывают по шкале «С» и обозначают HRC.
Если при испытании берется стальной шарик и общая нагрузка 1000 H, то твердость отсчитывается по шкале «В» и обозначается HRB.
При испытании очень твердых или тонких изделий используют алмазный конус и общую нагрузку 600 Н. Твердость отсчитывается по шкале «А» и обозначается HRA. Пример обозначения твердости по Роквеллу: HRC 50 - твердость 50 по шкале «С».
При определении твердости способом Виккерса (ГОСТ 2999 -75) в качестве вдавливаемого в материал наконечника используют четырехгранную алмазную пирамиду с углом при вершине 136°. При испытаниях применяют нагрузки от 50 до 1000 Н (меньшие значения нагрузки для определения твердости тонких изделий и твердых, упрочненных поверхностных слоев металла). Числовое значение твердости определяют так: замеряют длины обеих диагоналей отпечатка после снятия нагрузки и с помощью микроскопа и по полученному среднему арифметическому значению длины диагонали находят в таблице соответствующее число твердости. Пример обозначения твердости по Виккерсу - HV 500.
Для оценки твердости металлов в малых объемах, например, на зернах металла или его структурных составляющих применяют способ определения микротвердости. Наконечник (индентор) прибора представляет собой алмазную четырехгранную пирамиду (с углом при вершине 136о, таким же как и у пирамиды при испытании по Виккерсу). Нагрузка на индентор невелика и составляет 0,05 -5 Н, а размер отпечатка 5 -30 мкм. Испытание проводят на оптическом микроскопе ПМТ-3, снабженном механизмом нагружения. Микротвердость оценивают по величине диагонали отпечатка.
Усталостью называют процесс постепенного накопления повреждений материала под действием повторно-переменных напряжений, приводящий к образованию трещин и разрушению. Усталость металла обусловлена концентрацией напряжений в отдельных его объемах, в которых имеются неметаллические включения, газовые пузыри, различные местные дефекты и т. д. Характерным является усталостный излом, образующийся после разрушения образца в результате многократного нагружения и состоящий из двух разных по внешнему виду частей. Одна часть 1 излома с ровной (затертой) поверхностью образуется вследствие трения поверхностей в области трещин, возникших от действия повторно-переменных нагрузок, другая часть 2 с зернистым изломом возникает в момент разрушения образца.
Испытания на усталость проводят на специальных машинах. Наиболее распространены машины для повторно-переменного изгибания вращающегося образца, закрепленного одним или обоими концами, а также машины для испытаний на растяжение - сжатие и на повторно-переменное кручение. В результате испытаний определяют предел выносливости, характеризующий сопротивление усталости.
Выносливость - свойство материала противостоять усталости. Предел выносливости - это максимальное напряжение, которое может выдержать металл без разрушения заданное число циклов нагружения. Между пределом выносливости и пределом прочности существует приближенная зависимость:
у -1 ?0,43 у в; у -1р ? 0,36 у в, где у -1 и у -1р - соответственно пределы выносливости при изгибе и растяжении - сжатии.
Технологические и эксплуатационные свойства
Эти свойства характеризуют способность металлов подвергаться обработке в холодном и горячем состояниях. Технологические свойства определяют при технологических пробах, которые дают качественную оценку пригодности металлов к тем или иным способам обработки. Образец, подвергнутый технологической пробе осматривают. Признаком того, что образец выдержал испытание, является отсутствие трещин, надрывов, расслоения или излома. К основным технологическими свойствам относят: обрабатываемость резанием, свариваемость, ковкость, литейные свойства и др.
Обрабатываемость резанием - одна из важнейших технологических свойств, потому что подавляющее большинство заготовок, а так же деталей сварных узлов и конструкций подвергается механической обработке. Одни металлы обрабатываются хорошо до получения чистой и гладкой поверхности, другие же, имеющие высокую твердость, плохо. Очень вязкие металлы с низкой твердостью также плохо обрабатываются: поверхность получается шероховатой, с задирами. Улучшить обрабатываемость, например, стали можно термической обработкой, понижая или повышая ее твердость.
Свариваемость - способность металлов образовывать сварное соединение, свойства которого близки к свойствам основного металла. Ее определяют пробой сваренного образца на загиб или растяжение.
Ковкость - способность металла обрабатываться давлением в холодном или горячем состоянии без признаков разрушения. Ее определяют кузнечной пробой на осадку до заданной степени деформации. Высота образца для осадки равна обычно двум его диаметрам. Если на боковой поверхности образца трещина не образуется, то и такой образец считается выдержавшим пробу; а испытуемый металл - пригодным для обработки давлением.
Литейные свойства металлов характеризуют способность их образовывать отливки, без трещин, раковин и других дефектов. Основными литейными свойствами являются, жидкотекучесть, усадка и ликвация.
Жидкотекучесть - способность расплавленного металла хорошо заполнять полость литейной формы.
yaneuch.ru
Аллотропия
аллотропия это, аллотропия деген неАллотро́пия (от др.-греч. αλλος — «другой», τροπος — «поворот, свойство») — существование двух и более простых веществ одного и того же химического элемента, различных по строению и свойствам — так называемых аллотропных (или аллотропических) модификаций или форм.Явление аллотропии обусловлено либо различным составом молекул простого вещества (аллотропия состава), либо способом размещения атомов или молекул в кристаллической решётке (аллотропия формы).
Содержание
- 1 История
- 2 Примеры аллотропии
- 2.1 Неметаллы
- 2.2 Полуметаллы
- 2.3 Металлы
- 3 Энантиотропные и монотропные переходы
- 4 Примечания
- 5 См. также
- 6 Литература
- 7 Ссылки
История
Понятие аллотропии введено в науку Й. Берцелиусом в 1841 году для обозначения разных форм существования элементов; одновременно он предполагал, по-видимому, применить его и к изомерии соединений. После принятия гипотезы А. Авогадро в 1860 году стало понятно, что элементы могут существовать в виде многоатомных молекул, например, О2 — кислород и О3 — озон.
В начале XX века было признано, что различия в кристаллической структуре простых веществ (например, углерода или фосфора) также являются причиной аллотропии. В 1912 году В. Оствальд отметил, что аллотропия элементов является просто частным случаем полиморфизма кристаллов, и предложил от него отказаться. Однако, по настоящее время они используются параллельно. Аллотропия относится только к простым веществам, независимо от их агрегатного состояния; полиморфизм — только к твёрдому состоянию независимо от того, простое это вещество или сложное. Таким образом, эти термины совпадают для простых твёрдых веществ (кристаллическая сера, фосфор, железо и др.).
Примеры аллотропии
Аллотропные модификации фосфора (белый, красный, жёлтый, чёрный фосфор)В настоящее время известно более 400 разновидностей простых веществ. Способность элемента к образованию аллотропных форм обусловлена строением атома, которое определяет тип химической связи, строение молекул и кристаллов.
Как правило, большее число аллотропных форм образуют элементы, имеющие переменные значения координационного числа или степени окисления (олово, фосфор). Другим важным фактором является катенация — способность атомов элемента образовывать гомоцепные структуры (например, сера). Склонность к аллотропии более выражена у неметаллов, за исключением галогенов и благородных газов, и полуметаллов.
Принято обозначать различные аллотропические формы одного и того же элемента строчными буквами греческого алфавита; причём форму, существующую при самых низких температурах, обозначают буквой α, следующую — β и т. д.
Неметаллы
| Водород: | Водород может существовать в виде орто- и пара-водорода. В молекуле орто-водорода o-h3 (т. пл. −259,10 °C, т. кип. −252,56 °C) ядерные спины параллельны, а у пара-водорода p-h3 (т. пл. −259,32 °C, т. кип. −252,89 °C) — антипараллельны. |
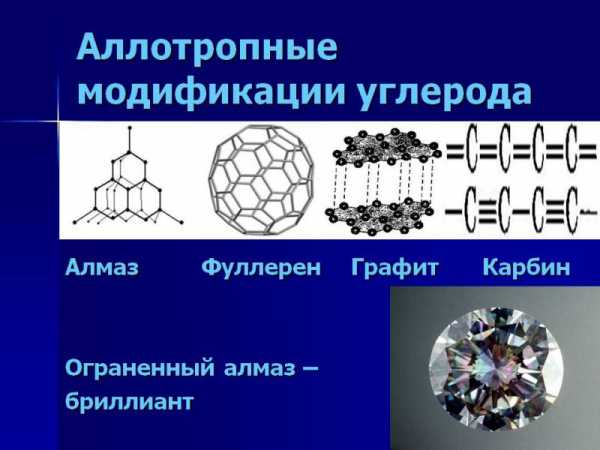
| Углерод: | Множество модификаций: алмаз, графит, фуллерен, карбин, графен, углеродные нанотрубки, лонсдейлит и др. Точное число модификаций указать затруднительно вследствие разнообразия форм связывания атомов углерода между собой. Наиболее многочисленны молекулярные структуры фуллеренов и нанотрубок. |
| Фосфор: | Известно 11 аллотропных модификаций фосфора. Основные модификации: белый, красный и чёрный фосфор. Белый фосфор ядовит, светится в темноте, способен самовоспламеняться, красный фосфор не ядовит, не светится в темноте, сам по себе не воспламеняется. |
| Кислород: | Две аллотропные модификации: О2 — кислород и О3 — озон. Кислород бесцветен, не имеет запаха; озон имеет выраженный запах, имеет бледно-фиолетовый цвет, он более бактерициден. |
| Сера: | Большое число аллотропных модификаций, второе место после углерода. Основные модификации: ромбическая, моноклинная и пластическая сера. |
| Селен: | Красный цикло-Se8, серый полимер Se и чёрный селен. |
Полуметаллы
| Бор: | Бор существует в аморфном и кристаллическом видах. Аморфный бор — порошок бурого цвета. Обладает большей реакционной способностью, чем кристаллический бор. Кристаллический бор — вещество чёрного цвета. Известно более 10 аллотропных модификаций бора, которые кристаллизуются в ромбической и тетрагональной сингониях. Наиболее устойчивая модификация — β-ромбический бор — состоит из икосаэдров B12, которые образуют слои, объединенные в бесконечную структуру. |
| Кремний: | Различают две основные аллотропные модификации кремния — аморфную и кристаллическую. Решётка кристаллической модификации кремния — атомная, алмазоподобная. Также выделяют поликристаллический и монокристаллический кремний. |
| Мышьяк: | Три основные аллотропные модификации: жёлтый мышьяк (неметалл, состоящий из молекул As4 — структура, аналогичная белому фосфору), серый мышьяк (полуметаллический полимер), чёрный мышьяк (неметаллическая молекулярная структура, аналогичная красному фосфору). |
| Германий: | Две аллотропные модификации: α-Ge — полуметалл с алмазоподобной кристаллической решёткой и β-Ge — с металлической структурой, аналогичной β-Sn. |
| Сурьма: | Известны четыре металлических аллотропных модификаций сурьмы, существующих при различных давлениях, и три аморфные модификации (взрывчатая, чёрная и жёлтая сурьма), из которых наиболее устойчива металлическая форма серебристо-белого цвета с синеватым оттенком |
| Полоний: | Полоний существует в двух аллотропных металлических модификациях. Кристаллы одной из них — низкотемпературной — имеют кубическую решетку (α-Po), а другой — высокотемпературной — ромбическую (β-Po). Фазовый переход из одной формы в другую происходит при 36 °C, однако при обычных условиях полоний находится в высокотемпературной форме вследствие разогрева собственным радиоактивным излучением. |
Металлы
Среди металлов, которые встречаются в природе в больших количествах (до U, без Tc и Pm), 28 имеют аллотропные формы при атмосферном давлении: Li, Be, Na, Ca, Sc, Ti, Mn, Fe, Co, Sr, Y, Zr, Sn, La, Ce, Pr, Nd, Sm, Gd, Tb, Dy, Yb, Hf, Tl, Th, Pa, U. Также важны аллотропные формы ряда металлов, образующиеся при их технологической обработке: Ti при 882˚C, Fe при 912˚C и 1394˚C, Co при 422˚C, Zr при 863˚C, Sn при 13˚C и U при 668˚C и 776˚C.
| Олово: | Олово существует в трех аллотропных модификациях. Серое олово (α-Sn) мелкокристаллический порошок, полупроводник, имеющий алмазоподобную кристаллическую решётку, существует при температуре ниже 13,2 °С. Белое олово (β-Sn) — пластичный серебристый металл, устойчивый в интервале температур 13,2—161 °С. Высокотемпературное гамма-олово (γ-Sn), имеющее ромбическую структуру, отличается высокой плотностью и хрупкостью, устойчиво между 161 и 232 °С (температура плавления чистого олова). |
| Железо: | Для железа известны четыре кристаллические модификации: до 769 °C (точка Кюри) существует α-Fe (феррит) с объёмноцентрированной кубической решёткой и свойствами ферромагнетика; в температурном интервале 769—917 °C существует β-Fe, который отличается от α-Fe только параметрами объёмноцентрированной кубической решётки и магнитными свойствами парамагнетика; в температурном интервале 917—1394 °C существует γ-Fe (аустенит) с гранецентрированной кубической решёткой; выше 1394 °C устойчиво δ-Fe с объёмоцентрированной кубической решёткой |
| Лантаноиды: | Церий, самарий, тербий, диспрозий и иттербий имеют по три аллотропических модификации; празеодим, неодим, гадолиний и тербий — по две. |
| Актиниды: | Для всех актиноидов, кроме актиния, характерен полиморфизм. Кристаллические структуры протактиния, урана, нептуния и плутония по своей сложности не имеют аналогов среди лантаноидов и более похожи на структуры 3d-переходных металлов. Плутоний имеет семь полиморфных модификаций (в том числе, при обычном давлении — 6), а уран, прометий, нептуний, америций, берклий и калифорний — три. Лёгкие актиниды в точке плавления имеют объёмно-центрированную решётку, а начиная с плутония — гранецентрированную. |
Энантиотропные и монотропные переходы
Серое и белое оловоПереход одной аллотропной модификации в другую происходит при изменении температуры или давления (или одновременном воздействии обоих факторов) и связан со скачкообразным изменением свойств вещества. Этот процесс бывает обратимым (энантиотропным) и необратимым (монотропным).
Примером энантиотропного перехода может служить превращение ромбической серы в моноклинную α-S (ромб.) ↔ β-S (монокл.) при 95,6 °C. При обычной температуре стабильной является ромбическая модификация серы, которая при нагревании до 95,6 °С при нормальном давлении переходит в моноклинную форму. Последняя при охлаждении ниже 95,6 °С вновь переходит в ромбическую форму. Таким образом, переход одной формы серы в другую происходит при одной и той же температуре, и сами формы называются энантиотропными.
К монотропному переходу относится превращение белого фосфора P4 под давлением 1,25 ГПа и температуре 200 °C в более стабильную модификацию — чёрный фосфор. При возвращении к обычным условиям обратный переход не происходит. Переход из нестабильной формы в стабильную в принципе возможен при любой температуре, а обратный — нет, то есть определенная точка перехода отсутствует. Ещё один пример — превращение графита в алмаз при давлении 6 ГПа и температуре 1500 °C в присутствии катализатора (никель, хром, железо и другие металлы), то есть при условиях термодинамической устойчивости алмаза. Тогда как алмаз легко и быстро переходит в графит при температурах выше 1000 °С. В обоих случаях давление способствует превращению, поскольку образуется вещества с более высокой плотностью, чем исходные.
Три известные модификации олова переходят друг в друга различным образом. При обычных условиях устойчиво β-Sn (пластичное белое олово) с тетрагональной кристаллической решеткой. Выше 173 °С β-Sn энантиотропно превращается в хрупкую модификацию γ-Sn, а ниже 13,2 °C β-Sn переходит монотропно в порошкообразное α-Sn (серое олово) с кубической решёткой типа алмаза. Этот полиморфный переход происходит с малой скоростью, но резко ускоряется в контакте с серым оловом — плотные куски белого олова рассыпаются в пыль («оловянная чума»). Обратный процесс возможен только путем переплавки.
Примечания
- ↑ Угай Я. А. Общая и неорганическая химия: Учеб. для студентов вузов, обучающихся по направлению и спец. «Химия». — М.: Высш. шк., 1997. — 524 с.: ил.
- ↑ Химическая энциклопедия: в 5 т. / Редкол.:Кнунянц И. Л. (гл. ред.). — Москва: Советская энциклопедия, 1992. — Т. 3. — С. 382. — 639 с. — 50 000 экз. — ISBN 5-85270-039-8
См. также
- Изомерия
- Полиморфизм кристаллов
- Кристаллическая решётка
Литература
- Эддисон У. Аллотропия химических элементов. — М.: Мир, 1966. — 207 с.
Ссылки
- Аллотропия // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
аллотропия деген не, аллотропия кислорода, аллотропия серы, аллотропия углерода, аллотропия фосфора, аллотропия это
Аллотропия Информацию О
Аллотропия Комментарии
АллотропияАллотропия Аллотропия Вы просматриваете субъект
Аллотропия что, Аллотропия кто, Аллотропия описание
There are excerpts from wikipedia on this article and video
www.turkaramamotoru.com
| Опубликовать | скачать Реферат на тему: План:
ВведениеАллотро́пия (от др.-греч. αλλος — «другой», τροπος — «поворот, свойство») — существование одного и того же химического элемента в виде двух и более простых веществ, различных по строению и свойствам: так называемых аллотропических модификаций или аллотропических форм. 1. Примеры
2. ПричиныАллотропия может быть результатом образования молекул с различным числом атомов (например, атомарный кислород O, молекулярный кислород O2 и озон O3) или образования различных кристаллических форм (например, графит и алмаз) — в этом случае аллотропия — частный случай полиморфизма). ПримечанияскачатьДанный реферат составлен на основе статьи из русской Википедии. Синхронизация выполнена 12.07.11 15:47:53Похожие рефераты: Аллотропия углерода.Категории: Аллотропия. Текст доступен по лицензии Creative Commons Attribution-ShareAlike. |
wreferat.baza-referat.ru
Читать реферат по химии: "Аллотропные модификации"
(Назад) (Cкачать работу)
Функция "чтения" служит для ознакомления с работой. Разметка, таблицы и картинки документа могут отображаться неверно или не в полном объёме!
Министерство образования и науки Российской Федерации федеральное государственное бюджетное образовательное учреждение высшего профессионального образовании «Оренбургский государственный педагогический университет»
Институт естествознания и экономики
Кафедра химии и методика преподавания химии
Реферат
по дисциплине: Основы общей химии
АЛЛОТРОПНЫЕ МОДИФИКАЦИИ
Выполнил:
Тукаева Г.Р.
Оренбург
СодержаниеВведение
Глава 1
.1 Аллотропные модификации
.2 История аллотропной модификации
.3 Переход аллотропной модификации
Глава 2
.1 Аллотропия углерода
.1.1 Алмаз
.1.1.1 Свойства алмаза
.1.2 Графит
.1.2.1 Свойства графита
Глава 3
.1 Аллотропия состава
.1.1 Кислород
.1.2 Озон
Заключение
Список использованной литературы Введение Аллотропия - это существование по крайней мере двух форм одного и того же элемента в твердом кристаллическом состоянии, которые отличаются пространственным расположением атомов. Поскольку взаимные превращения аллотропных форм связаны с изменением уравнения состояния вещества, его энергии, термин “аллотропия” следует использовать исключительно в термодинамическом смысле. Понятие полиморфизма имеет в большей мере кристаллографическое значение, так как включает структурные и морфологические изменения. А частный случай одномерного полиморфизма, который характерен для некоторых плотноупакованных и слоистых структур, представляет собой политипизм. Это способность вещества кристаллизоваться в виде нескольких модификаций, каждая из которых при двух идентичных параметрах элементарной ячейки отличается лишь третьим, зависимым чаще всего от расстояния между соседними слоями.
Политипизм нередко проявляется в структурах, эквивалентных кубической и гексагональной плотной упаковке атомов. В политипных модификациях ближайшее атомное окружение одинаково, а различия обусловлены характером вторых (или даже более удаленных) координационных сфер. Поэтому величины энергии их кристаллических решеток почти равны и, следовательно, очень похожи их физические свойства. Глава 1.1 Явление аллотропии Сочетание атомов одного и того же элемента - есть простое вещество. В зависимости от типа химической связи, между атомами простые вещества могут быть металлами и неметаллами. Для металлов характерна металлическая связь, а для неметаллов - ковалентная. Резкого различия между металлическими и неметаллическими простыми веществами нет. К металлам примыкают металлоподобные простые вещества, а к неметаллам - неметаллоподобные.
Один и тот же элемент может образовывать несколько разных типов простых веществ, называемых аллотропными модификациями. Известно свыше 400 разновидностей простых веществ. Явление аллотропии может быть обусловлено либо различным составом молекул простого вещества данного элемента (аллотропия состава), либо способом размещения молекул и атомов в кристаллах (аллотропия формы). Способность элемента к образованию соответствующих аллотропных модификаций обусловлена строением атома, которое определяет тип химической связи, строение молекул, строение кристаллов.
Как правило, большее число аллотропных форм образуют элементы, которые имеют переменные значения координационного числа или степени окисления (олово, фосфор). Также другим важным фактором является катенация - способность атомов элемента образовывать гомоцепные структуры (например, сера). Склонность к аллотропии более выражена у неметаллов, за исключением галогенов и благородных газов, а также полуметаллов.
Принято обозначать различные аллотропические формы одного и того же элемента строчными буквами греческого алфавита; а форму, существующую при самых низких температурах - буквой α, следующую - β и т. д. .2 История аллотропной модификации Понятие аллотропии введено в науку Й. Берцелиусом в 1841 году для обозначения различных форм существования элементов. Одновременно он предполагал применить его и к изомерии соединений. После принятия гипотезы А. Авогадро в 1860 году, стало понятно, что элементы могут существовать в виде многоатомных молекул (например, О2 - кислород, О3 - озон. В начале ХХ века было признано, что различия в кристаллической структуре простых веществ также являются причиной аллотропии. В 1912 году В. Оствальд отметил, что аллотропия элементов является просто частным случаем полиморфизма кристаллов, после чего предложил от него отказаться. Аллотропия относится только к простым веществам, независимо от их агрегатного состояния. Полиморфизм - только к твердому состоянию независимо от того, простое это вещество или сложное..3 Переход аллотропной модификации Переход одной аллотропной модификации в другую происходит при изменении температуры или давления (или же при одновременном воздействии обоих факторов) и связан со скачкообразным изменением свойств вещества. Этот процесс бывает обратимым (энантиотропным) и необратимым (монотропным).
Примером энантиотропного перехода может служить превращение ромбической серы в моноклинную α-S (ромб.) ↔ β-S (монокл.) при 95,6 °C. При обычной температуре стабильной является ромбическая модификация серы, которая при нагревании до 95,6 °С при нормальной давлении переходит в моноклинную форму. Последняя при охлаждении ниже 95,6 °С вновь переходит в ромбическую форму. Таким образом, переход одной формы серы в другую происходит при одной и той же температуре, и сами формы называются энантиотропными.
К монотропному переходу относится превращение белого фосфора P4 под давлением 1,25 ГПа и температуре 200 °C в более стабильную модификацию - чёрный фосфор. При возвращении к обычным условиям обратный переход не происходит. Переход из нестабильной формы в стабильную в принципе возможен при любой температуре, а обратный - нет, то есть определенная точка перехода отсутствует. Еще один пример - превращение графита в алмаз при давлении 6 ГПа и температуре 1500 °C в присутствии катализатора (никель, хром, железо и другие металлы), то есть при условиях термодинамической устойчивости алмаза. Тогда как алмаз легко и быстро переходит в графит при температурах выше 1000 °С. В обоих случаях давление способствует превращению, поскольку образуется вещества с более высокой плотностью, чем исходные.
Три известные модификации олова переходят друг в друга различным образом. При обычных условиях устойчиво β-Sn (плаcтичное белое олово) с тетрагональной кристаллической решеткой [2]. Выше 173 °С β-Sn энантиотропно превращается в хрупкую модификацию γ-Sn, а ниже 13,2 °C β-Sn переходит монотропно в порошкообразное α-Sn (серое олово) с кубической решёткой типа алмаза. Этот полиморфный переход происходит с малой скоростью, но резко ускоряется в контакте с серым оловом - плотные куски белого олова рассыпаются в пыль («оловянная чума»). Обратный процесс возможен только путем переплавки. Глава 2 .1 Аллотропия углерода В свободном состоянии углерод известен в виде алмаза, кристаллизующего в кубической системе, а также графита, принадлежащего к гексагональной системе. Такие его формы, как древесный уголь, кокс, сажа - имеют неупорядоченную структуру. Синтетически получены карбин и поликумилен - разновидности углерода, состоящие из линейных цепных полимеров типа...-С=С-С=С-... или...=С=С=С=.... Карбин обладает полупроводниковыми свойствами. При сильном нагревании и без доступа воздуха он превращается в графит..1.1 Алмаз
Алмаз - бесцветное, прозрачное вещество, чрезвычайно сильно преломляющее лучи света. Он кристаллизуется в кубической гранецентрированной решетке. При этом одна половина атомов располагается в вершинах и центрах граней одного куба, а другая - в вершинах и центрах граней другого, смещенного относительно в первом в направлении его пространственной диагонали. Атомы углерода в алмазе находятся в состоянии sp^3 гибридизации, образуют трехмерную тетраэдрическую сетку, в которой они связаны друг с другом ковалентными связями. Расстояние между атомами в тетраэдрах равно 0,154 нм.
Из всех простых веществ алмаз имеет максимальное число атомов, приходящихся на единицу объема, атомы углерода "упакованы" в алмазе очень плотно. С этим, а также с большой прочностью связи в углеродных тетраэдрах
referat.co
Реферат По дисциплине: Биология На тему: Аллотропия металлов.
1.1. Аморфные и кристаллические тела
В твердых телах атомы могут размещаться в пространстве двумя способами:
Беспорядочное расположение атомов, когда они не занимают определенного места друг относительно друга. Такие тела называются аморфными.
Аморфные вещества обладают формальными признаками твердых тел, т.е. они способны сохранять постоянный объем и форму. Однако они не имеют определенной температуры плавления или кристаллизации.
Упорядоченное расположение атомов, когда атомы занимают в пространстве вполне определенные места, Такие вещества называются кристаллическими.
Атомы совершают относительно своего среднего положения колебания с частотой около 1013 Гц. Амплитуда этих колебаний пропорциональна температуре.
Благодаря упорядоченному расположению атомов в пространстве, их центры можно соединить воображаемыми прямыми линиями. Совокупность таких пересекающихся линий представляет пространственную решетку, которую называют кристаллической решеткой.
Внешние электронные орбиты атомов соприкасаются, так что плотность упаковки атомов в кристаллической решетке весьма велика.
Кристаллические твердые тела состоят из кристаллических зерен – кристаллитов. В соседних зернах кристаллические решетки повернуты относительно друг друга на некоторый угол.
В кристаллитах соблюдаются ближний и дальний порядки. Это означает наличие упорядоченного расположения и стабильности как окружающих данный атом ближайших его соседей (ближний порядок), так и атомов, находящихся от него на значительных расстояниях вплоть до границ зерен
Вследствие диффузии отдельные атомы могут покидать свои места в узлах кристаллической решетки, однако при этом упорядоченность кристаллического строения в целом не нарушается.
1.2. Основные типы кристаллических решеток
Все металлы являются кристаллическими телами, имеющими определенный тип кристаллической решетки, состоящей из малоподвижных положительно заряженных ионов, между которыми движутся свободные электроны (так называемый электронный газ). Такой тип структуры называется металлической связью.
Тип решетки определяется формой элементарного геометрического тела, многократное повторение которого по трем пространственным осям образует решетку данного кристаллического тела.
Металлы имеют относительно сложные типы кубических решеток – объемно центрированная (ОЦК) и гранецентрированная (ГЦК) кубические решетки.
Основу ОЦК-решетки составляет элементарная кубическая ячейка в которой положительно заряженные ионы металла находятся в вершинах куба, и еще один атом в центре его объема, т. е. на пересечении его диагоналей. Такой тип решетки в определенных диапазонах температур имеют железо, хром, ванадий, вольфрам, молибден и др. металлы.
У ГЦК-решетки элементарной ячейкой служит куб с центрированными гранями. Подобную решетку имеют железо, алюминий, медь, никель, свинец и др. металлы.
Третьей распространенной разновидностью плотноупакованных решеток является гексагональная плотноупакованная (ГПУ,). ГПУ-ячейка состоит из отстоящих друг от друга на параметр с параллельных центрированных гексагональных оснований. Три иона (атома) находятся на средней плоскости между основаниями.
У гексагональных решеток отношение параметра с/а всегда больше единицы. Такую решетку имеют магний, цинк, кадмий, берилий, титан и др.
Компактность кристаллической решетки или степень заполненности ее объема атомами является важной характеристикой. Она определяется такими показателями как параметр решетки, число атомов в каждой элементарной ячейке, координационное число и плотность упаковки.
Параметр решетки – это расстояние между атомами по ребру элементарной ячейки. Параметры решетки измеряется в нанометрах (1 нм = 10-9 м = 10 Å). Параметры кубических решеток характеризуются длиной ребра куба и обозначаются буквой а.
Для характеристики гексагональной решетки принимают два параметра – сторону шестигранника а и высоту призмы с. Когда отношение с/а = 1,633, то атомы упакованы наиболее плотно, и решетка называется гексагональной плотноупакованной . Некоторые металлы имеют гексагональную решетку с менее плотной упаковкой атомов (с/а > 1,633). Например, для цинка с/а = 1,86, для кадмия с/а = 1,88.
Параметры а кубических решеток металлов находятся в пределах от 0,286 до 0,607 нм. Для металлов с гексагональной решеткой а лежит в пределах 0,228-0,398 нм, а с в пределах 0,357- 0,652 нм.
Параметры кристаллических решеток металлов могут быть измерены с помощью рентгеноструктурного анализа.
При подсчете числа атомов в каждой элементарной ячейке следует иметь в виду, что каждый атом входит одновременно в несколько ячеек. Например, для ГЦК-решетки, каждый атом, находящийся в вершине куба, принадлежит 8 ячейкам, а атом, центрирующий грань, двум. И лишь атом, находящийся в центре куба, полностью принадлежит данной ячейке.
Таким образом, ОЦК- и ГЦК-ячейки содержат соответственно 2 и 4 атома.
Под координационным числом понимается количество ближайших соседей данного атома.
В ОЦК решетке атом А (в центре) находится на наиболее близком равном расстоянии от восьми атомов, расположенных в вершинах куба, т. е. координационное число этой решетки равно 8 (К8).
В ГЦК решетке атом А (на грани куба) находится на наиболее близком равном расстоянии от четырех атомов /, 2, 3, 4, расположенных в вершинах куба, от четырех атомов 5, 6, 7, 8, расположенных на гранях куба, и, кроме того, от четырех атомов 9, 10, 11, 12, принадлежащих расположенной рядом кристаллической ячейке. Атомы 9, 10, 11, 12 симметричны атомам 5, 6, 7, 8. Таким образом, ГЦК решетки координационное число равно 12 (К12).
В ГПУ решетке при с/а = 1,633 (рис. 1.3, в) атом А в центре шестигранного основания призмы находится на наиболее близком равном расстоянии от шести атомов /, 2, 3, 4, 5, 6, размещенных в вершинах шестигранника, и от трех атомов 7, 8, 9, расположенных в средней плоскости призмы. Кроме того, атом А оказывается на таком же расстоянии еще от трех атомов 10, 11, 12, принадлежащих кристаллической ячейке, лежащей ниже основания. Атомы 10, 11, 12 симметричны атомам 7, 8, 9.
Следовательно, для ГПУ решетки координационное число равно 12 (Г12).
Плотность упаковки представляет собой отношение суммарного объема, занимаемого собственно атомами в кристаллической решетке, к ее полному объему. Различные типы кристаллических решеток имеют разную плотность упаковки атомов. В ГЦК решетке атомы занимают 74 % всего объема кристаллической решетки, а межатомные промежутки («поры») 26 %. В ОЦК решетке атомы занимают 68 % всего объема, а «поры» 32 %. Компактность решетки зависит от особенностей электронной структуры металлов и характера связи между их атомами.
От типа кристаллической решетки сильно зависят свойства металла.
Упорядоченность кристаллического строения в пространственной решетке позволяет выделить отдельные кристаллографические направления и плоскости.
Кристаллографические направления – это характерные прямые линии, выходящие из точки отсчета, вдоль которых в кристаллической решетке располагаются атомы. Точками отсчета, могут служить вершины куба, а кристаллографическими направлениями – его ребра и диагонали, а также диагонали граней
Кристаллографические направления и плоскости в кристаллической решетке: а) – основные направления и их обозначение; Кристаллографическими плоскостями являются, например, плоскости граней кубов , а также их различные диагональные плоскости вместе с находящимися на них атомами. Для ГПУ-решеток кристаллографическими плоскостями могут быть плоскости оснований.
Для определения индекса какого-либо направления необходимо найти индекс ближайшего к данной точке отсчета атома, находящегося на данном направлении. Например, индекс ближайшего атома вдоль оси ОХ обозначается цифрами 100. Эти цифры представляют собой координаты упомянутого атома относительно точки О, выраженные через количество параметров вдоль осей OX, OY и OZ соответственно.
Индексы направления ОХ и параллельных ему направлений обозначаются [100]. Соответственно направления OY и OZ обозначаются [010] и [001]. Кристаллографические направления вдоль диагоналей граней XOZ, XOY и YOZ обозначают [101], [110] и [011]. Пользуясь указанной методикой, можно определить индекс любого направления. Например, индекс направления вдоль диагонали куба выразится так: [111].
Для определения индекса кристаллографической плоскости необходимо вначале найти координаты ближайших точек ее пересечения с осями координат, проведенными из точки отсчета О. Затем взять обратные им величины и записать их в круглых скобках в обычной последовательности. Например, координатами точек пересечения с осями координат ближайшей плоскости, параллельной плоскости XOY, выраженными через параметры решеток, являются числа Ґ, Ґ, 1. Поэтому индекс этой плоскости можно записать в виде (001).
Индексами плоскостей, параллельных плоскостям XOZ и YOZ, окажутся выражения (010) и (100. Индекс вертикальной диагональной плоскости куба выразится через (110), а индекс наклонной плоскости, пересекающейся со всеми тремя осями координат на удалении одного параметра, примет вид (111).
1.4. Анизотропия в кристаллах
Под анизотропией понимается неодинаковость механических и других свойств в кристаллических телах вдоль различных кристаллографических направлений. Она является естественным следствием кристаллического строения, так как на различных кристаллографических плоскостях и вдоль различных направлений плотность атомов различна.
Например, в кубических решетках по направлениям вдоль ребер насчитывается меньше атомов, чем вдоль диагоналей куба в ОЦК-решетке или диагоналей граней в ГЦК-решетке. На плоскостях, проходящих через грани ОЦК- и ГЦК-решеток, находится меньше атомов, чем на диагональных плоскостях.
Поскольку механические, физические и химические свойства вдоль различных направлений зависят от плотности находящихся на них атомов, то перечисленные свойства вдоль различных направлений в кристаллических телах должны быть неодинаковыми.
Анизотропия проявляется только в пределах одного монокристалла или зерна-кристаллита. В поликристаллических телах она не наблюдается из-за усреднения свойств по каждому направлению для огромного количества произвольно ориентированных друг относительно друга зерен. Поэтому реальные металлы являются квазиизотропными телами, т. е. псевдоизотропными.
Рис. 1.5. Элементарная ячейка решетки ОЦК
Сдвиг в кристалле происходит наиболее легко вдоль атомных плоскостей с наиболее плотной упаковкой атомов. Рассмотрим объемно-центрическую кубическую решетку (ОЦК
1.5. Аллотропия металлов
Некоторые металлы, например, железо, титан, олово и др. способны по достижении определенных температур изменять кристаллическое строение, т. е. изменять тип элементарной ячейки своей кристаллической решетки. Это явление получило название аллотропии или полиморфизма, а сами переходы от одного кристаллического строения к другому называются аллотропическими или полиморфными.
В интервале температур 911-1392оC железо имеет решетку ГЦК, так как при этом его свободная энергия меньше. При t<911°С и t>1392°С, у него должна быть решетка ОЦК, обладающая меньшей свободной энергией.
Разные аллотропические формы металлов обозначаются буквами греческого алфавита, при этом низкотемпературные модификации обозначаются буквой a, а последующие в порядке роста температур – буквами b, g ,d и т. д. Аллотропическими формами железа являются: до 911°С – альфа-железо (a-Fe), имеющее ОЦК-решетку, от 911°С до 1392 °С -гамма-железо (g -Fe) с решеткой ГЦК и от 1392°С до 1539 °С т. е. до температуры плавления – снова a-Fe с решеткой OЦK, однако, чтобы отличить его от низкотемпературной модификации, его принято называть дельта-железом (d -Fе).
Известное в практике так называемое немагнитное бета-железо (b -Fe) самостоятельной аллотропической формой не является, так как имеет такую же, как у a-Fe ОЦК-решетку и отличается от него только отсутствием магнитных свойств, которые оно теряет при 768°С (точка Кюри).
1.6. Дефекты кристаллической решетки металла
Кристаллическая решетка, в которой отсутствуют нарушения сплошности и все узлы заполнены однородными атомами называется идеальной кристаллической решеткой металла.
В решетке реального металла могут находиться различные дефекты.
Все дефекты кристаллической решетки принято делить на точечные, линейные, поверхностные и объемные.
Точечные дефекты соизмеримы с размерами атомов. К ним относятся вакансии, т. е. незаполненные узлы решетки, межузельные атомы данного металла (рис 1.8), примесные атомы замещения, т. е. атомы, по диаметру соизмеримые с атомами данного металла и примесные атомы внедрения, имеющие очень малые размеры и поэтому находящиеся в междоузлиях. Влияние этих дефектов на прочность металла может быть различным в зависимости от их количества в единице объема и характера.
Линейные дефекты имеют длину, значительно превышающую их поперечные размеры. К ним относятся дислокации, т. е. дефекты, образующиеся в решетке в результате смещений кристаллографических плоскостей.
Дислокации бывают двух видов.
Наиболее характерной является краевая дислокация. Она образуется в результате возникновения в решетке так называемой полуплоскости или экстраплоскости.
В винтовой дислокации, так же как в краевой, существенные искажения кристаллической решетки наблюдаются только вблизи оси, поэтому такой дефект может быть отнесен к линейным.
Дислокации обладают высокой подвижностью, поэтому существенно уменьшают прочность металла, так как облегчают образование сдвигов в зернах-кристаллитах под действием приложенных напряжений.
Дислокационный механизм сдвиговой пластической деформации внутри кристаллов может привести к разрушению изделия. Таким образом, дислокации непосредственно влияют на прочностные характеристики металла.
Для оценки этого влияния используется плотность дислокаций, под которой принято понимать отношение суммарной длины дислокаций к объему содержащего их металла. Плотности дислокаций измеряется в см-2 или м-2.
Виде кривой ABC схематически показана зависимость прочности металла от плотности дислокаций. Точка А соответствует теоретической прочности металла, обусловленной необходимостью одновременного разрыва всех межатомных связей, проходящих через плоскость сдвига, в случае отсутствия дислокаций.
При увеличении количества дислокаций (см. участок АВ) прочность резко снижается, так как на несколько порядков уменьшаются усилия, необходимые для осуществления сдвигов в зернах металла при его деформировании и разрушении.
При плотности дислокаций 106-107 см-2 (точка В на кривой), прочности минимальна, и на участке ВС происходит ее рост. Это объясняется тем, что с ростом плотности дислокаций их передвижение происходит не только по параллельным, но и по пересекающимся плоскостям, что существенно затрудняет процесс деформирования зерен.
Поэтому начиная с точки В прочность металла возрастает.
Максимальная плотность дислокаций, может составить 1013 см-2. При дальнейшем росте плотности дислокаций происходит разрушение металла.
Поверхностные дефекты включают в себя главным образом границы зерен. На границах кристаллическая решетка сильно искажена. В них скапливаются перемещающиеся изнутри зерен дислокации.
Из практики известно, что мелкозернистый металл прочнее крупнозернистого. Так как у последнего меньше суммарная протяженность (площадь) границ. То можно сделать вывод, что поверхностные дефекты способствуют повышению прочности металла. Поэтому создано несколько технологических способов получения мелкозернистых сплавов.
Объемные дефекты кристаллической решетки включают трещины и поры. Наличие данных дефектов, уменьшая плотность металла, снижает его прочность.
Кроме того, трещины являются сильными концентраторами напряжений, в десятки и более раз повышающими напряжения создаваемые в металле рабочими нагрузками. Последнее обстоятельство наиболее существенно влияет на прочность металла.
kursak.net
аллотропия / Поиск по тегам / Кампусята Дальневосточного Федерального Университета
10 мар 2012. Характерные свойства металлов обусловлены их строением.… формах носит название полиморфизма или аллотропии. Различные. Аллотропия металлов Наука и мистика.. 08.02.2013, 18:31, Автор темы. Изменения, которые происходят в строении металла, находящегося в. 10 мар 2012. Характерные свойства металлов обусловлены их строением.… формах носит название полиморфизма или аллотропии. Различные. Фазовые переходы и поверхностные свойства аллотропных металлов и… научных журналах, рекомендуемых ВАК; более 20 тезисов докладов и 3. Скачать Презентация по химии 8 класс на тему металлы. на тему Доклад с. Аллотропия. Аллотропия металлов Наука и мистика.. 08.02.2013, 18:31, Автор темы. Изменения, которые происходят в строении металла, находящегося в. 21 апр 2014. Презентация по химии на тему «Аллотропия. Простые и. Фуллерены применяются для синтеза металлов и сплавов с новыми. Тема выпускной работы: Взаимодействие отходящих газов, содержащих диоксид серы с. диоксида серы и соединений щелочноземельных металлов. Описание: Сборник подготовлен по материалам докладов и тезисов участников IV… Взаимодействие серы с кислородом, аллотропные модификации.Свойства аллотропных модификаций химического элемента кислорода: простых. Рассмотрите этимологию названий отдельных благородных металлов.. Сайт Xvatit.com является порталом, в котором не предусмотрены темы. Алмаз и графит — аллотропические формы углерода, отличающиеся… Pa, U. Также важны аллотропные формы ряда металлов, образующиеся при их. Аллотропия металов.. применение свойств металов и сплавов.. Гигантский проект на юго-западе Баку: скоростная дорога К тому же, углерод проявляется во многих своих формах — аллотропных. равной 13,2°С, и существовать в виде белого металла достаточно долго. 11 окт 2012. Аллотропическое превращение как процесс перехода из одной кристаллической формы в другую. Исследование строения металлов. Поэтому в газообразном состоянии большинство металлов состоит из одноатомных. Таким образом, металлическая связь между атомами металлов. Читать доклад online по теме 'Аллотропные видоизменения углерода: графит и алмаз'. Раздел: История техники, Наука и техника, Загружено:. Алмаз и графит — аллотропические формы углерода, отличающиеся… Pa, U. Также важны аллотропные формы ряда металлов, образующиеся при их. Аллотропия металлов Наука и мистика.. 08.02.2013, 18:31, Автор темы. Изменения, которые происходят в строении металла, находящегося в. Аллотропия металлов Наука и мистика.. 08.02.2013, 18:31, Автор темы. Изменения, которые происходят в строении металла, находящегося в.
xn--80aa2ajpmhg3i.xn--p1ai











