Содержание
Кристаллическое строение металлов. Кристаллическая решетка металлов
Одним из самых распространенных материалов, с которым всегда предпочитали работать люди, был металл. В каждую эпоху предпочтение отдавалось разным видам этих удивительных веществ. Так, IV-III тысячелетия до нашей эры считаются веком хальколита, или медным. Позже его сменяет бронзовый, а затем в силу вступает тот, что и по сей день является актуальным — железный.
Сегодня вообще сложно представить, что когда-то можно было обходиться без металлических изделий, ведь практически все, начиная от предметов быта, медицинских инструментов и заканчивая тяжелой и легкой техникой, состоит из этого материала или включает в свой состав отдельные части из него. Почему же металлы сумели завоевать такую популярность? В чем проявляются особенности и как это заложено в их строении, попробуем разобраться далее.
Общее понятие о металлах
«Химия. 9 класс» — это учебник, по которому проходят обучение школьники. Именно в нем подробно изучаются металлы. Рассмотрению их физических и химических свойств отведена большая глава, ведь разнообразие их чрезвычайно велико.
Именно в нем подробно изучаются металлы. Рассмотрению их физических и химических свойств отведена большая глава, ведь разнообразие их чрезвычайно велико.
Именно с этого возраста рекомендуют давать детям представление о данных атомах и их свойствах, ведь подростки уже вполне могут оценить значение подобных знаний. Они прекрасно видят, что окружающее их разнообразие предметов, машин и прочих вещей имеет в своей основе как раз металлическую природу.
Что же такое металл? С точки зрения химии, к данным атомам принято относить те, что имеют:
- малое число электронов на внешнем уровне;
- проявляют сильные восстановительные свойства;
- имеют большой атомный радиус;
- как простые вещества обладают рядом специфических физических свойств.
Основу знаний об этих веществах можно получить, если рассмотреть атомно-кристаллическое строение металлов. Именно оно объясняет все особенности и свойства данных соединений.
В периодической системе для металлов отводится большая часть всей таблицы, ведь они образуют все побочные подгруппы и главные с первой по третью группу.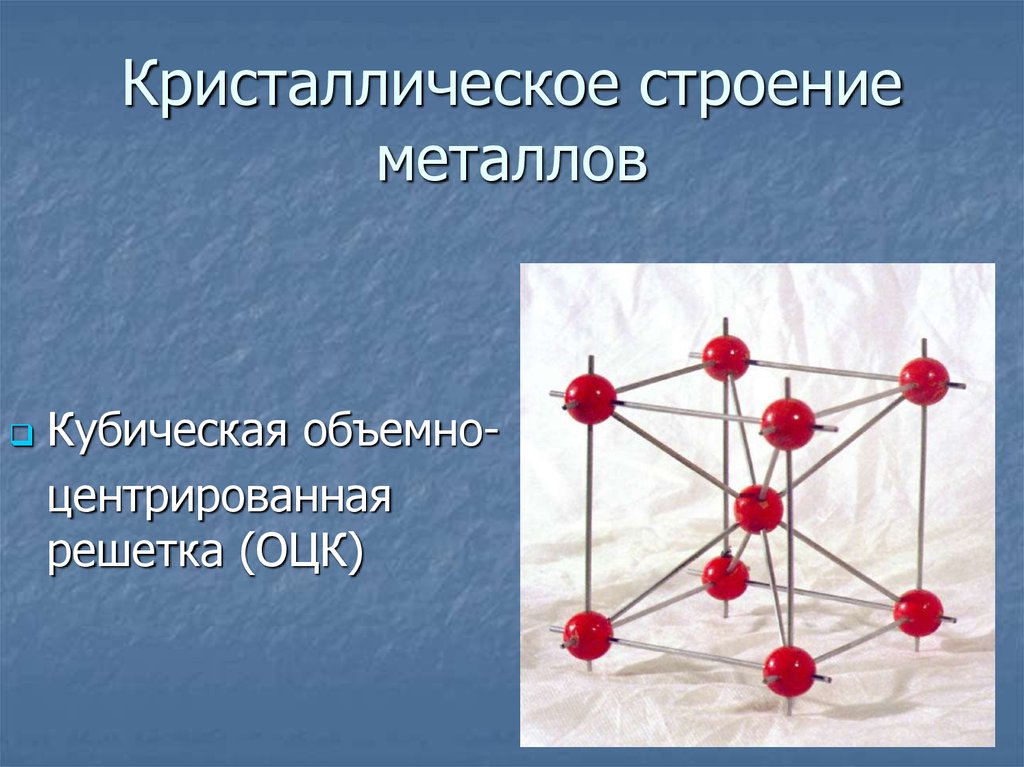 Поэтому их численное превосходство очевидно. Самыми распространенными являются:
Поэтому их численное превосходство очевидно. Самыми распространенными являются:
- кальций;
- натрий;
- титан;
- железо;
- магний;
- алюминий;
- калий.
Все металлы имеют ряд свойств, которые позволяют объединять их в одну большую группу веществ. В свою очередь, эти свойства объясняет именно кристаллическое строение металлов.
Свойства металлов
К специфическим свойствам рассматриваемых веществ относят следующие.
- Металлический блеск. Все представители простых веществ им обладают, причем большинство одинаковым серебристо-белым цветом. Лишь некоторые (золото, медь, сплавы) отличаются.
- Ковкость и пластичность — способность деформироваться и восстанавливаться достаточно легко. У разных представителей выражена в неодинаковой мере.
- Электропроводность и теплопроводность — одно из основных свойств, которое определяет области применения металла и его сплавов.
Кристаллическое строение металлов и сплавов объясняет причину каждого из обозначенных свойств и говорит о выраженности их у каждого конкретного представителя.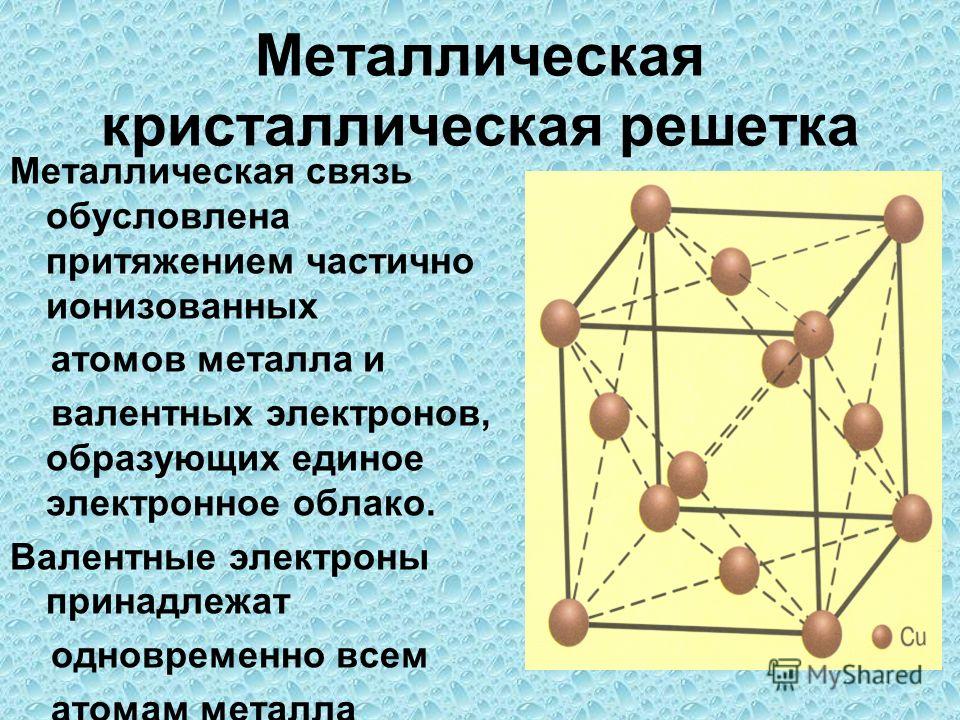 Если знать особенности такого строения, то можно влиять на свойства образца и подстраивать его под нужные параметры, что и делают люди уже многие десятилетия.
Если знать особенности такого строения, то можно влиять на свойства образца и подстраивать его под нужные параметры, что и делают люди уже многие десятилетия.
Атомно-кристаллическое строение металлов
В чем же заключается такое строение, чем характеризуется? Само название говорит о том, что все металлы представляют собой кристаллы в твердом состоянии, то есть при обычных условиях (кроме ртути, которая является жидкостью). А что такое кристалл?
Это условное графическое изображение, построенное путем пересечения воображаемых линий через атомы, которые выстраивают тело. Другими словами, каждый металл состоит из атомов. Они располагаются в нем не хаотично, а очень правильно и последовательно. Так вот, если мысленно соединить все эти частицы в одну структуру, то получится красивое изображение в виде правильного геометрического тела какой-либо формы.
Это и принято называть кристаллической решеткой металла. Она очень сложная и пространственно объемная, поэтому для упрощения показывают не всю ее, а лишь часть, элементарную ячейку.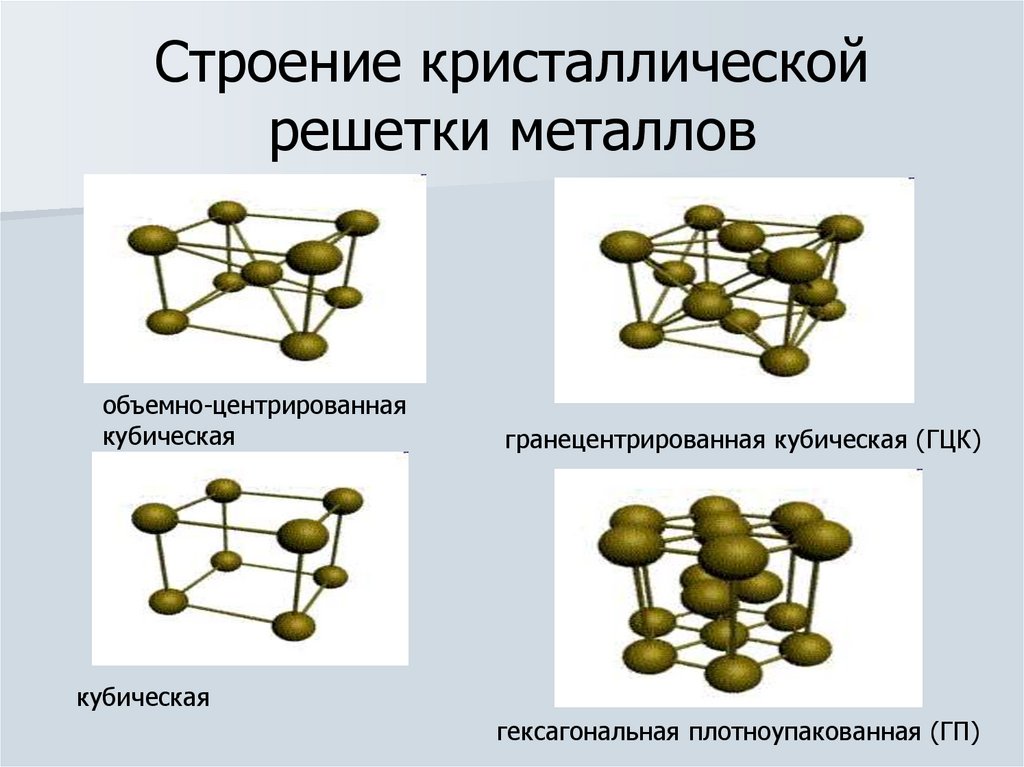 Совокупность таких ячеек, собранная вместе и отраженная в трехмерном пространстве, и образует кристаллические решетки. Химия, физика и металловедение — это науки, которые занимаются изучением особенностей строения таких структур.
Совокупность таких ячеек, собранная вместе и отраженная в трехмерном пространстве, и образует кристаллические решетки. Химия, физика и металловедение — это науки, которые занимаются изучением особенностей строения таких структур.
Сама элементарная ячейка — это набор атомов, которые располагаются на определенном расстоянии друг от друга и координируют вокруг себя строго фиксированное число других частиц. Она характеризуется плотностью упаковки, расстоянием между составными структурами, координационным числом. В целом все эти параметры являются характеристикой и всего кристалла, а значит, отражают и проявляемые металлом свойства.
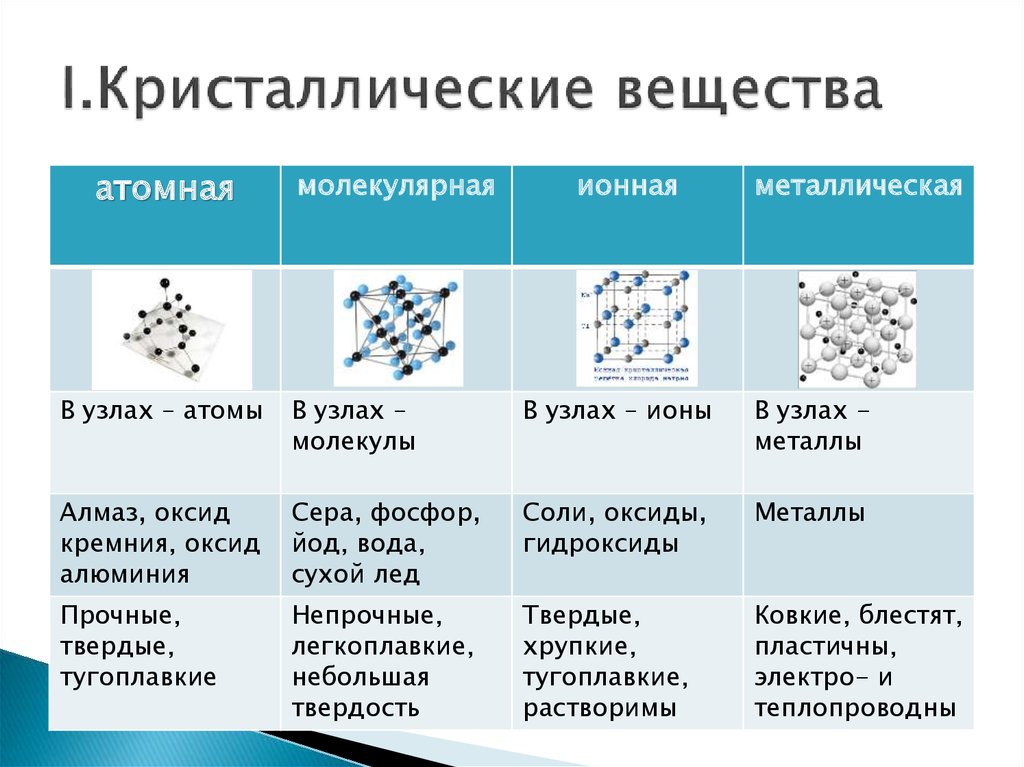
Существует несколько разновидностей кристаллических решеток. Объединяет их все одна особенность — в узлах находятся атомы, а внутри располагается облако электронного газа, которое формируется путем свободного передвижения электронов внутри кристалла.
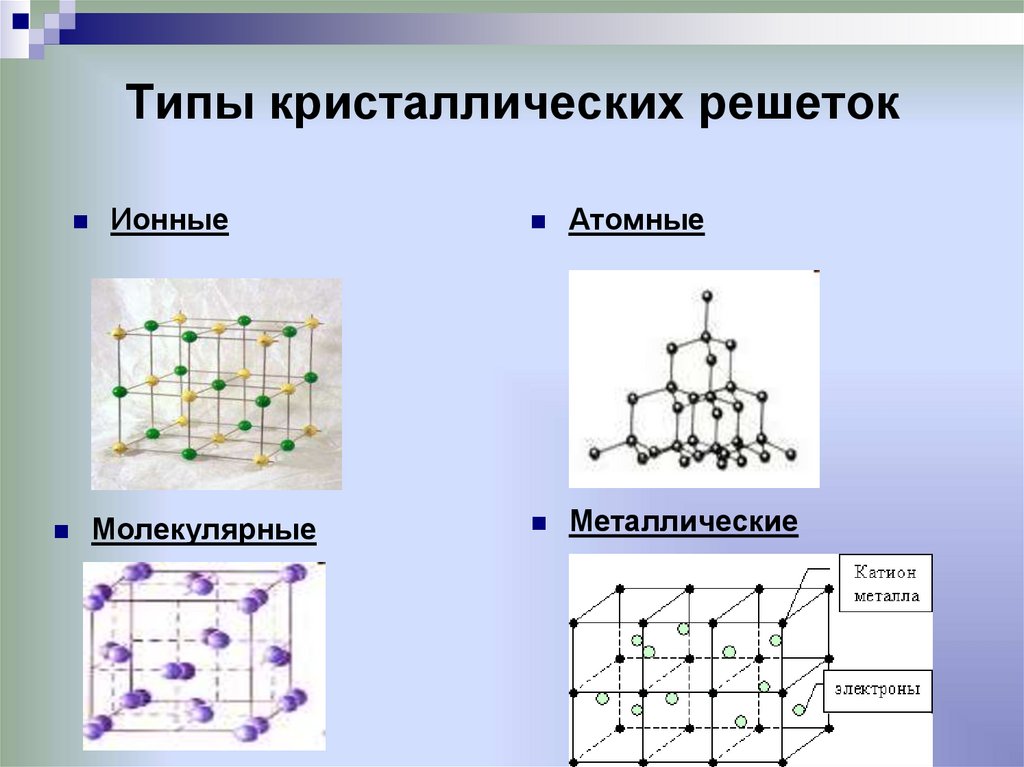
Типы кристаллических решеток
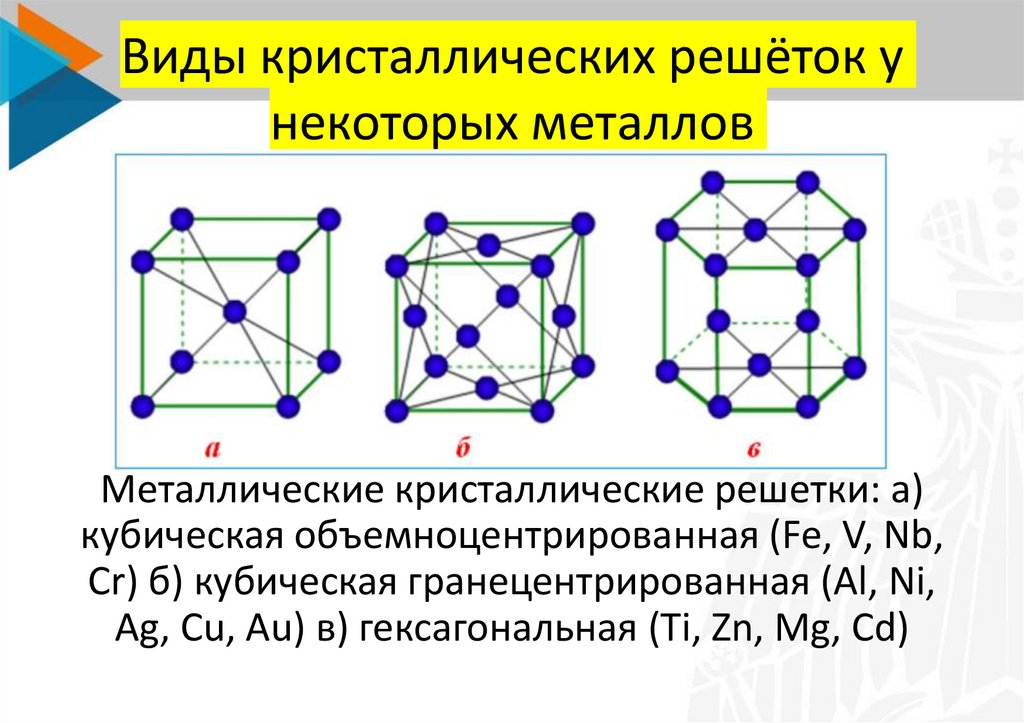
Четырнадцать вариантов строения решетки принято объединять в три основных типа. Они следующие:
Они следующие:
- Объемно-центрированная кубическая.
- Гексагональная плотноупакованная.
- Гранецентрированная кубическая.
Кристаллическое строение металлов было изучено только благодаря электронной микроскопии, когда стало возможным получать большие увеличения изображений. А классификацию типов решеток впервые привел французский ученый Браве, по фамилии которого их иногда называют.
Объемно-центрированная решетка
Строение кристаллической решетки металлов данного типа представляет собой следующую структуру. Это куб, в узлах которого находится восемь атомов. Еще один располагается в центре свободного внутреннего пространства ячейки, что и объясняет название «объемно-центрированная».
Это один из вариантов наиболее простого строения элементарной ячейки, а значит, и всей решетки в целом. Такой тип имеют следующие металлы:
- молибден;
- ванадий;
- хром;
- марганец;
- альфа-железо;
- бетта-железо и другие.

Основные свойства таких представителей — высокая степень ковкости и пластичности, твердость и прочность.
Гранецентрированная решетка
Кристаллическое строение металлов, имеющих гранецентрированную кубическую решетку, представляет собой следующую структуру. Это куб, который включает в свой состав четырнадцать атомов. Восемь из них формируют узлы решетки, а еще шесть расположены по одному на каждой грани.
Подобную структуру имеют:
- алюминий;
- никель;
- свинец;
- гамма-железо;
- медь.
Основные отличительные свойства — блеск разного цвета, легкость, прочность, ковкость, повышенная устойчивость к коррозии.
Гексагональная решетка
Кристаллическое строение металлов, обладающих данным типом решетки, следующее. В основе элементарной ячейки лежит шестигранная призма. В ее узлах располагается 12 атомов, еще два по основаниям и три атома свободно лежат внутри пространства в центре структуры. Всего семнадцать атомов.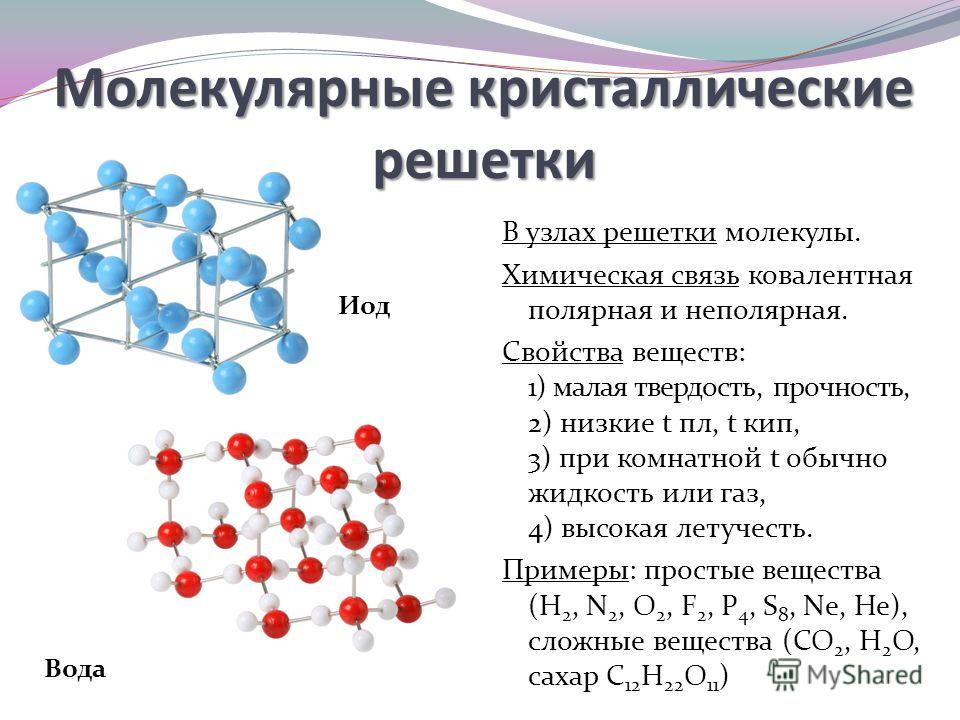
Подобную сложную конфигурацию имеют такие металлы, как:
- альфа-титан;
- магний;
- альфа-кобальт;
- цинк.
Основные свойства — высокая степень прочности, сильный серебристый блеск.
Дефекты кристаллического строения металлов
Однако все рассмотренные типы ячеек могут иметь и естественные недостатки, или так называемые дефекты. Это может быть связано с разными причинами: посторонними атомами и примесями в металлах, внешними воздействиями и прочим.
Поэтому существует классификация, отражающая дефекты, которые могут иметь кристаллические решетки. Химия как наука изучает каждый из них с целью выявления причины и способа устранения, чтобы свойства материала не были изменены. Итак, дефекты следующие.
- Точечные. Они бывают трех основных видов: вакансии, примеси или дислоцированные атомы. Приводят к ухудшению магнитных свойств металла, электро- и теплопроводности его.
- Линейные, или дислокационные. Выделяют краевые и винтовые.
 Ухудшают прочность и качество материала.
Ухудшают прочность и качество материала. - Поверхностные дефекты. Влияют на внешний вид и структуру металлов.
В настоящее время разработаны методики устранения дефектов и получения чистых кристаллов. Однако совсем искоренить их не удается, идеальной кристаллической решетки не существует.
Значение знаний о кристаллическом строении металлов
Из вышеизложенного материала очевидно, что знания о тонкой структуре и строении позволяют спрогнозировать свойства материала и повлиять на них. И это позволяет делать наука химия. 9 класс общеобразовательной школы делает в процессе обучения упор на то, чтобы сформировать у учащихся четкое понятие о важном значении основополагающей логической цепочки: состав — строение — свойства — применение.
Сведения о кристаллическом строении металлов очень четко иллюстрирует эту зависимость и позволяет учителю наглядно объяснить и показать детям, насколько важно знать тонкую структуру, чтобы правильно и грамотно использовать все свойства.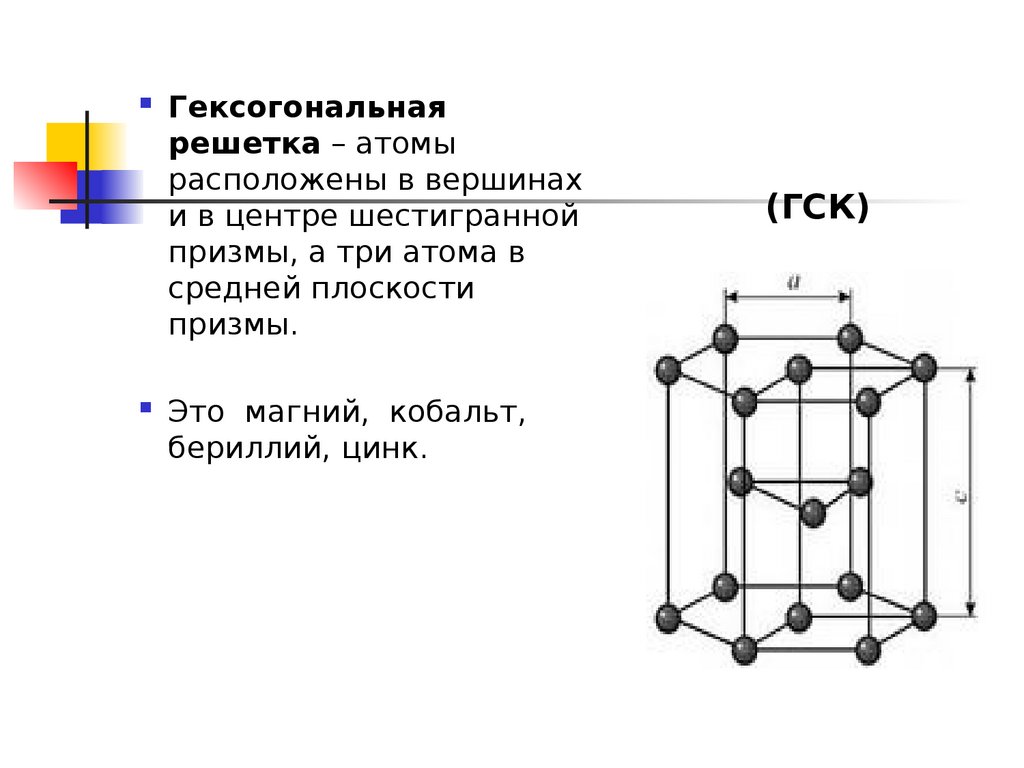
Особенность — строение — кристаллическая решетка
Cтраница 1
Особенности строения кристаллической решетки играют существенную роль для характеристики качества диоксида марганца как активного вещества источника тока, катализатора, абсорбента, твердого электролита.
[1]
| Рентгенограммы двуокиси марганца.
[2] |
Особенности строения кристаллической решетки играют — существенную роль для характеристики качества двуокиси марганца как активного вещества источников тока. Строение кристаллов определяют рентгенографическим способом. Расстояние между плоскостями в кристалле ( межплоскостные расстояния), измеряемые в ангстремах А, позволяют отнести образец к той или иной модификации. Расстояния между плоскостями в кристалле соответствуют промежутку между линиями на рентгенограмме.
[3]
Основные типы кристаллических решеток металлов.
[4] |
Особенность строения кристаллической решетки металлов заключается в том, что одни ее узлы заняты атомами, а другие положительными ионами. В промежутках между узлами перемещаются свободные электроны, образующие как бы электронный газ. Нахождение свободных электронов в металлических кристаллах обусловливают общие свойства металлов, их электро — и теплопроводность. Они же объясняют способность металлов к механической деформации.
[5]
Особенности строения кристаллических решеток графита и алмаза приводят к заметному различию их физических и химических свойств.
[6]
Ионная проводимость некоторых кристаллических тел — твердых электролитов — связана с особенностями строения кристаллической решетки и в отдельных случаях — с присутствием в ней чужеродных ионов.
[7]
Кристаллическая структура графита. а — модель графита.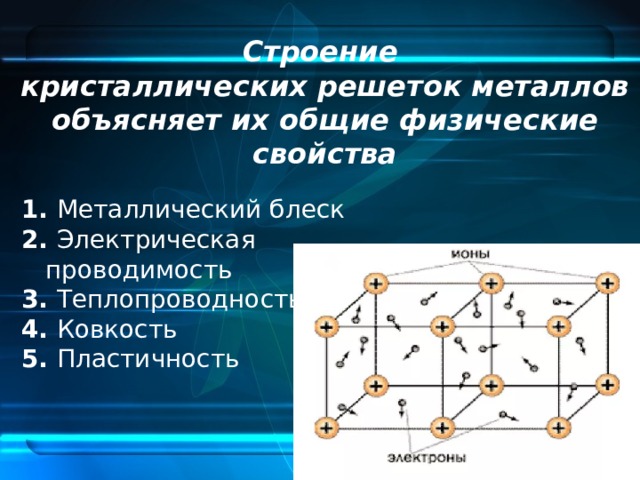 б — взаимное расположение слоев. б — взаимное расположение слоев.
[8] |
В настоящее время авторы многочисленных работ подтвердили, что все реакции углерода обусловлены особенностями строения кристаллической решетки графита.
[9]
Высокая вязкость рассматриваемых сталей и сплавов и их значительное упрочнение в процессе обработки обусловлены особенностями строения кристаллической решетки жаропрочных материалов. Детали следует обрабатывать на мощных и жестких станках, с жестким закреплением детали и инструмента. Инструмент должен хорошо затачиваться. Нельзя применять чрезмерно малые подачи при обработке, так как из-за наклепа поверхностных слоев стойкость инструмента при малых подачах резко падает. Глубину резания также рекомендуется брать не ниже 0 3 — 0 5 мм.
[10]
В [9] предложен механизм, связывающий изомеризацию АВК и юс реакции обмена с р-дикетонами и АВТ с особенностями строения кристаллической решетки.
[11]
Поэтому можно предположить, что повышенная температура плавления га-хлоранилина но сравнению с температурой плавления тг-бромани-лина связана с особенностью строения кристаллической решетки последнего.
[12]
Следует отметить, что наряду с конструкционной анизотропией композита существуют технологическая анизотропия, возникающая при пластической деформации изотропных материалов, и физическая анизотропия, присущая, например, кристаллам и связанная с особенностями строения кристаллической решетки.
[13]
Диэлектрическая проницаемость углей зависит от степени их метаморфизма и имеет минимальное значение, что объясняется ростом электропроводимости у слабометаморфизованных углей за счет наличия в них полярных функциональных групп, а в антрацитах — за счет особенностей строения кристаллической решетки. Диэлектрическая проницаемость возрастает с повышением влажности.
[14]
В минералах группы монтмориллонита связь между кремне-кислородными и гиббситовыми пакетами проходит по кислородным поверхностям и поэтому относительно слаба, она определяется ван-дер-ваальсовыми силами. Такая особенность строения кристаллической решетки позволяет молекулам воды и полярным органическим молекулам легко входить в межпакетное пространство, изменяя его размеры и вызывая набухание породы.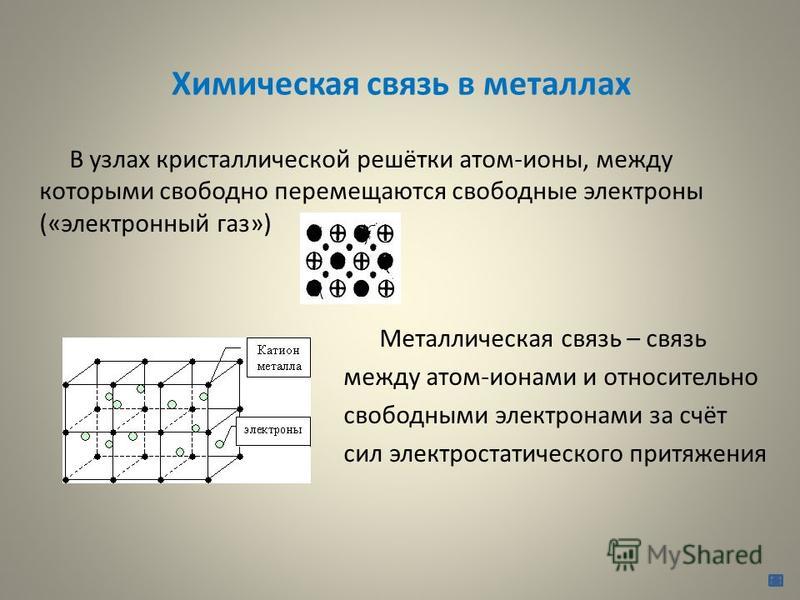 Эти минералы характеризуются выраженными катионообменными свойствами, что проявляется в способности глины связывать определенно число катионов, причем одни из них могут быть частично или полностью заменены другими в эквивалентных количествах. Обменная емкость монтмориллонита — более 50Х Х10 — 5 моль / кг. Минералы группы монтмориллонита встречаются в глинистых породах палеогенового, мелового, юрского, пермского и каменноугольного возраста. В более ранних породах не обнаружены.
Эти минералы характеризуются выраженными катионообменными свойствами, что проявляется в способности глины связывать определенно число катионов, причем одни из них могут быть частично или полностью заменены другими в эквивалентных количествах. Обменная емкость монтмориллонита — более 50Х Х10 — 5 моль / кг. Минералы группы монтмориллонита встречаются в глинистых породах палеогенового, мелового, юрского, пермского и каменноугольного возраста. В более ранних породах не обнаружены.
[15]
Страницы:
1
2
4.2a Металлы и металлические сплавы
Черные металлы содержат железо, ржавчину и обладают магнитными свойствами.
| Цветные металлы не содержат железа и не подвержены коррозии.
|
Металлы часто описывают как положительно заряженные ядра в море электронов. Внешние электроны ядер атомов металлов свободны и могут проходить через кристаллическую структуру. Связь вызвана притяжением между положительно заряженными ядрами металлических атомов и отрицательно заряженным облаком свободных электронов. Особое расположение атомов металла не требуется.
Металлическая связь предполагает совместное использование внешних электронов, но они более свободны и могут проходить через кристаллическую структуру. Связь вызвана притяжением между положительно заряженными ядрами атомов металла и отрицательно заряженным облаком свободных электронов и распространяется по всей решетке — «положительно заряженные ядра в море электронов».
Чистые и легированные металлы существуют в виде кристаллов. Металлы, многие виды керамики и некоторые полимеры имеют однородное геометрическое расположение атомов или ионов, которое повторяется по всему материалу, и поэтому их называют кристаллическими.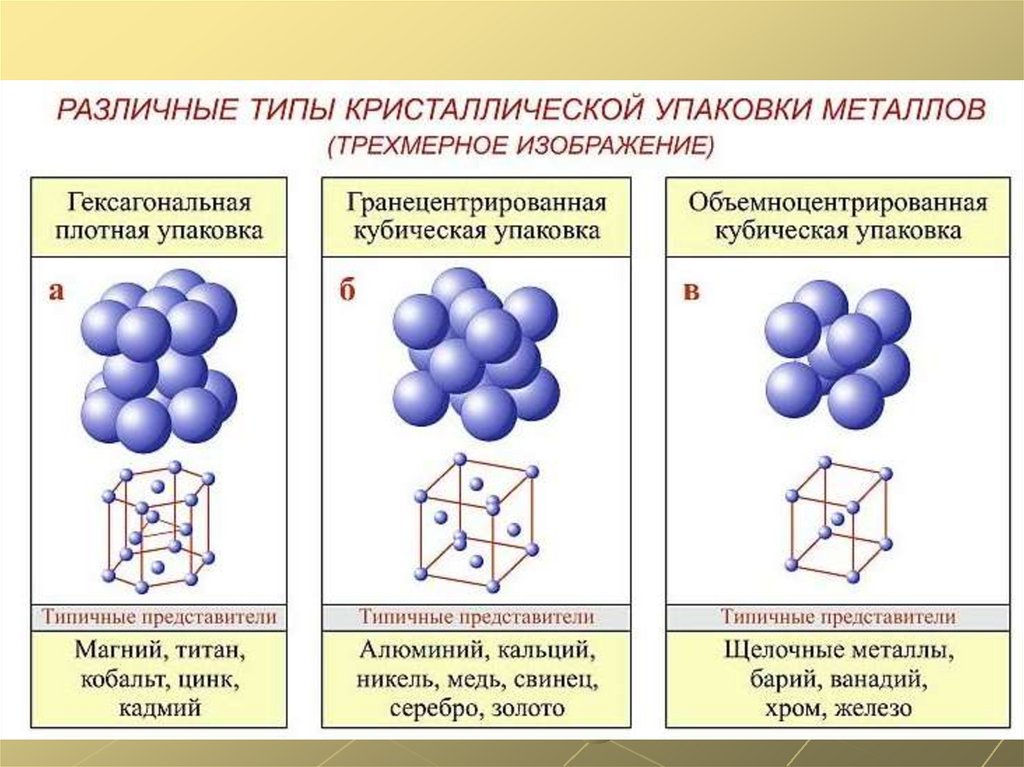 Эта регулярная трехмерная структура атомов известна как пространственная решетка, а элементарная ячейка является наименьшей единицей решетки, которая сохраняет общие характеристики решетки. Кристаллическая структура относится к размеру, форме и расположению атомов элементарной ячейки решетки и варьируется от одного вещества к другому. Кристаллы представляют собой регулярное расположение частиц (атомов, ионов или молекул).
Эта регулярная трехмерная структура атомов известна как пространственная решетка, а элементарная ячейка является наименьшей единицей решетки, которая сохраняет общие характеристики решетки. Кристаллическая структура относится к размеру, форме и расположению атомов элементарной ячейки решетки и варьируется от одного вещества к другому. Кристаллы представляют собой регулярное расположение частиц (атомов, ионов или молекул).
Решетчатая структура металлов |
Если взять в качестве примера скрепку. Типичная скрепка состоит из ок. 1 000 000 000 000 000 000 000 атомов железа. Эти атомы плотно упакованы в кристаллическую структуру (регулярное расположение атомов, которое повторяется много раз). |
Размер зерна
Затвердевание металла достигается в процессе зарождения и роста. Когда чистый расплавленный металл охлаждается чуть ниже температуры замерзания, в жидкости сначала образуются мельчайшие зародыши твердого вещества.
Структура атомов железа не является непрерывной на протяжении всей скрепки. Когда металл охлаждается и переходит из жидкого состояния в твердое, его атомы объединяются, образуя крошечные зерна или кристаллы. Хотя кристаллическая структура не продолжается от кристалла к кристаллу, кристаллы связаны друг с другом.
Затвердевание металлов состоит в том, что оно не происходит внезапно во всей жидкости. По мере затвердевания расплавленного чистого металла начинают формироваться кристаллы (зародыши), и эти кристаллы растут за счет добавления атомов с образованием дендрита, который, как можно видеть, представляет собой кристаллический скелет с остовом, от которого ветви растут в других направлениях, фиксируемых закономерностью элементарной ячейки.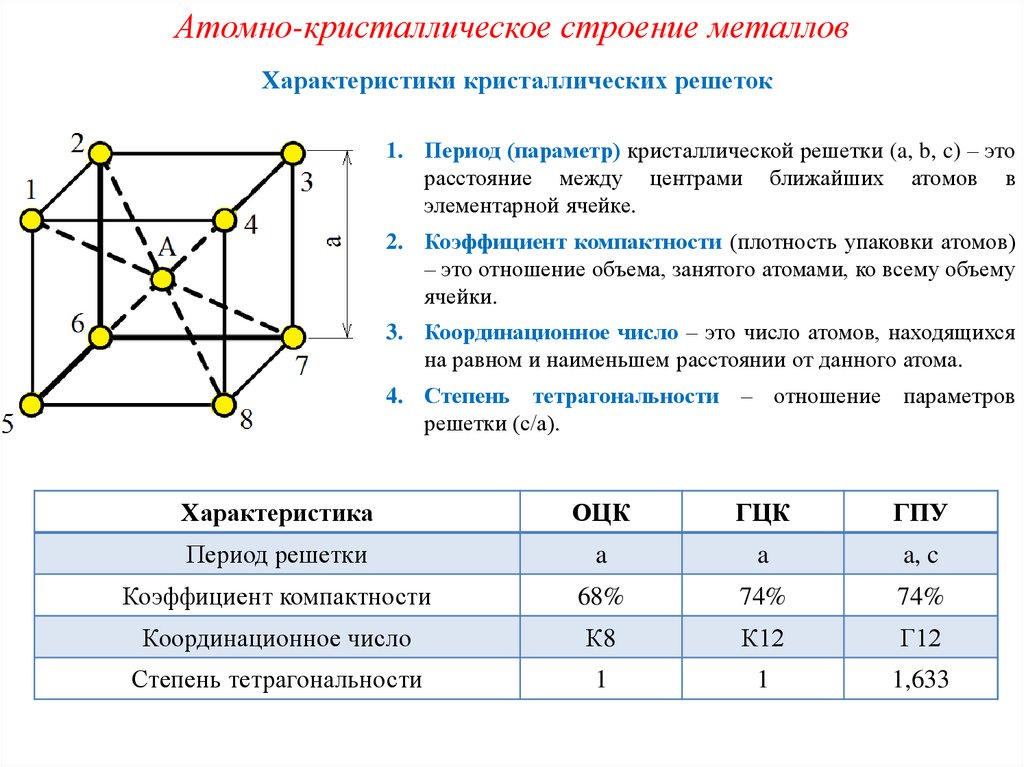
Рост дерева, начиная с его ствола и растущих ветвей и побегов, часто используется в качестве аналогии для описания роста дендритов. |
Кристаллы, обнаруженные во всех коммерческих металлах, обычно называют зернами из-за этого изменения внешней формы. Область, вдоль которой встречаются кристаллы, известная как граница зерна, представляет собой область несоответствия. Границы образованы материалами, которые не являются частью решетки, такими как примеси, которые не имеют определенного рисунка зерен. Это приводит к некристаллической (аморфной) структуре на границе зерен с неравномерно расположенными атомами. Поскольку последняя жидкость затвердевает, как правило, вдоль границ зерен, в этой области наблюдается более высокая концентрация примесных атомов.
Повторный нагрев твердого металла или сплава позволяет материалу диффундировать между соседними зернами и изменять структуру зерен. Медленное охлаждение позволяет формировать более крупные зерна; быстрое охлаждение дает более мелкие зерна. Направленные свойства в структуре могут быть достигнуты за счет избирательного охлаждения одной области твердого тела.
Медленное охлаждение позволяет формировать более крупные зерна; быстрое охлаждение дает более мелкие зерна. Направленные свойства в структуре могут быть достигнуты за счет избирательного охлаждения одной области твердого тела.
Скорость охлаждения расплавленного металла будет определять размер зерна. Постепенное охлаждение приводит к образованию лишь нескольких зародышей и, следовательно, к большому размеру зерна, тогда как быстрое охлаждение приводит к образованию большого количества зародышей и меньшего размера зерна.
http://www.ehponline.org/members/2006/114-8/innovations.html
Пластическая деформация: Остаточная деформация твердого тела, подвергаемого напряжению.
Пластическая деформация: материалы остаются деформированными после того, как нагрузка добавлена, а затем удалена.
Упругая деформация металла представляет собой небольшое изменение формы при низком напряжении, которое восстанавливается после снятия напряжения. Этот тип деформации включает растяжение металлических связей, но атомы не скользят друг относительно друга.
Этот тип деформации включает растяжение металлических связей, но атомы не скользят друг относительно друга.
Пластическая деформация возникает, когда напряжение достаточно для необратимой деформации металла. Этот тип деформации включает разрыв связей, обычно за счет движения дислокаций.
Пластическая деформация приводит к образованию большего количества дислокаций в металлической решетке. Это может привести к уменьшению подвижности этих дислокаций из-за их склонности к запутыванию или закреплению. Пластическая деформация при температурах, достаточно низких, чтобы атомы не могли перестроиться (холодная обработка) , может упрочнить металл в результате этого эффекта. Одним из побочных эффектов является то, что металл становится более хрупким. По мере использования металла трещины имеют тенденцию образовываться и расти, что в конечном итоге приводит к его поломке или разрушению.
Прочность на растяжение : Способность материала выдерживать растягивающие усилия.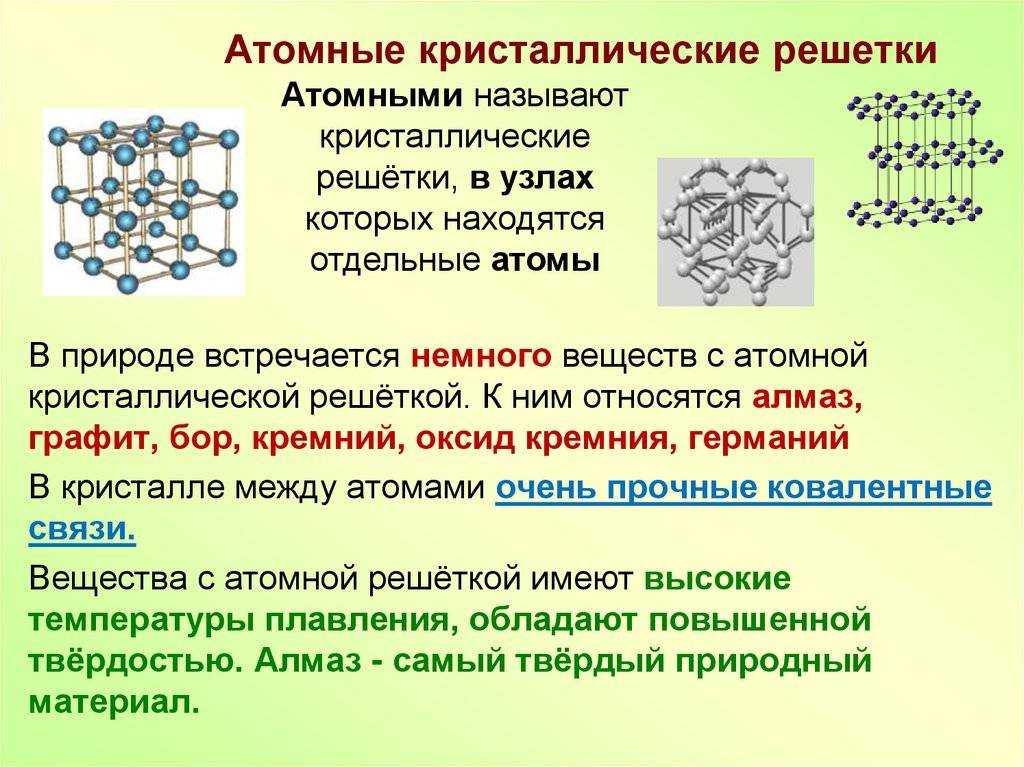
Деформационное упрочнение — увеличение твердости металлов в результате их холодной обработки. Это вызывает необратимое искажение кристаллической структуры и особенно заметно для железа, меди и алюминия и т. д., тогда как для свинца и цинка этого не происходит, поскольку эти металлы способны рекристаллизоваться при комнатной температуре. (мелкий размер зерна).
Холодная обработка:
Поскольку пластическая деформация возникает в результате движения дислокаций, металлы можно упрочнить, предотвращая это движение. Когда металл изгибается или формуется, дислокации генерируются и перемещаются. По мере увеличения количества дислокаций в кристалле они запутываются или скрепляются и не могут двигаться. Это укрепит металл, затруднит его деформацию. Этот процесс известен как холодная обработка. При более высоких температурах дислокации могут перестраиваться, поэтому упрочнение происходит незначительно.
Влияние холодной обработки на растяжение и предел текучести меди. |
Прочность на растяжение, предел текучести и твердость увеличиваются, а пластичность снижается. Твердость обычно увеличивается наиболее быстро при первых 10 % обжатия (холодная обработка), в то время как предел прочности при растяжении увеличивается более или менее линейно. Предел текучести увеличивается быстрее, чем предел прочности при растяжении, так что по мере увеличения величины пластической деформации разрыв между пределом текучести и пределом прочности при растяжении уменьшается. |
Сплав: Смесь, содержащая хотя бы один металл.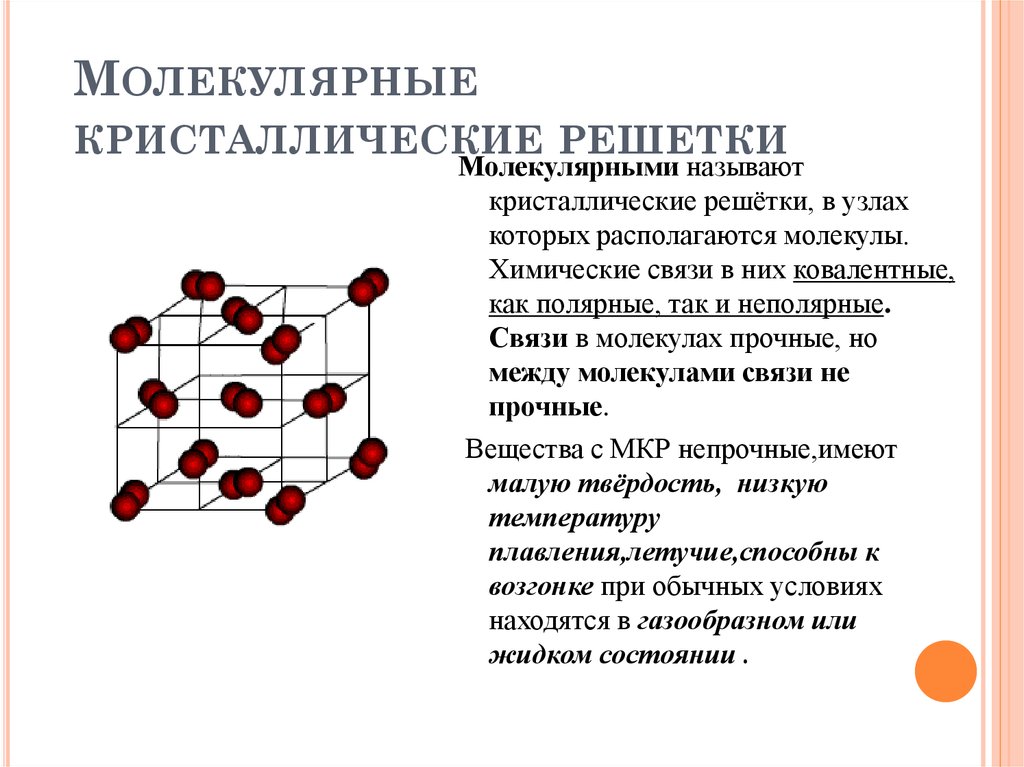 Это может быть смесь металлов или смесь металлов и неметаллов.
Это может быть смесь металлов или смесь металлов и неметаллов.
Стойкость к окислению металла или сплава в окислительной атмосфере определяется свойствами оксидного слоя — окалины, образующейся на поверхности металла. | Ползучесть — это склонность металла (или материала) к медленному перемещению или постоянной деформации из-за длительного воздействия напряжения ниже предела текучести или предела прочности металла. Ползучесть является более серьезной, когда металлы подвергаются воздействию тепла, близкого к точке плавления, в течение длительных периодов времени. | Отпуск — это метод термической обработки, применяемый к сплавам черных металлов, таким как сталь или чугун, для повышения ударной вязкости за счет снижения твердости сплава. |
Твердость металла | Zahner — Инновации и сотрудничество для достижения невероятного
РЕСУРСЫ
Твердость металла – характеристика, определяющая износостойкость поверхности и стойкость к истиранию. Способность материала сопротивляться вмятинам от удара связана с твердостью, а также с пластичностью материала. Различные степени твердости могут быть достигнуты во многих металлах путем отпуска, процесса термической обработки, используемого в холоднокатаных и холоднодеформированных металлах.
По мере того как зернистая структура металла подвергается холодной штамповке, зерна растягиваются и изменяются. Поверхность становится более твердой, сопротивляясь деформации от контакта. Закалка нагревает обрабатываемый металл до температур, при которых зерна начинают растворяться.
Доступны серии стандартных сплавов. Эти состояния и их доступность в конкретном сплаве варьируются в зависимости от природы зерен при их рекристаллизации.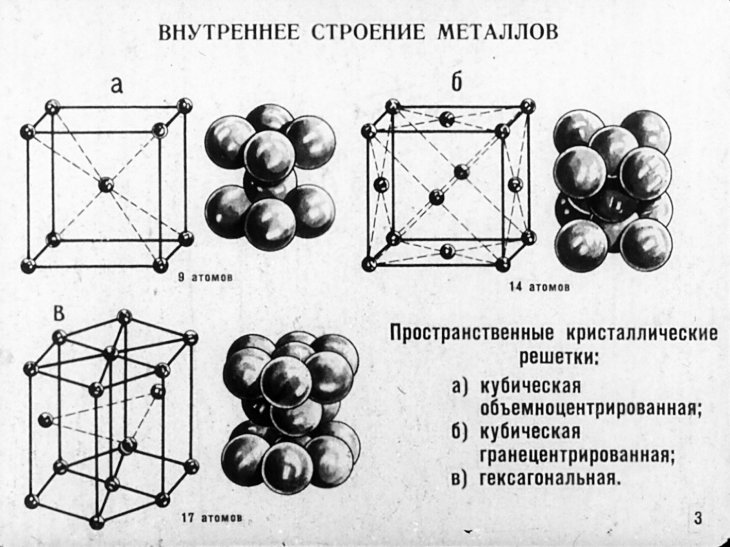 Обозначение отпуска фактически определяется размером зерна, а не пределом текучести металла.
Обозначение отпуска фактически определяется размером зерна, а не пределом текучести металла.
Таблица твердости металлов
Приведенная ниже таблица полезна для определения того, какие металлы будут невосприимчивы к царапинам и вмятинам, поскольку она относится к шкале Роквелла и пластичности. Шкала Роквелла — это шкала твердости, основанная на твердости материала при вдавливании. Испытание Роквелла определяет твердость путем измерения глубины проникновения индентора под большой нагрузкой по сравнению с проникновением, сделанным при предварительном нагружении.
Таблица твердости металла на основе шкалы Роквелла и пластичности.
ИЗОБРАЖЕНИЕ © КОМПАНИЯ A. ZAHNER.
Процессы повышения твердости металла
Существует несколько способов упрочнения архитектурного металла: на заводе или в процессе изготовления. Каждый из механизмов упрочнения вносит неровности кристаллической решетки в кристаллическую структуру металла, что затрудняет дислокацию структуры металла.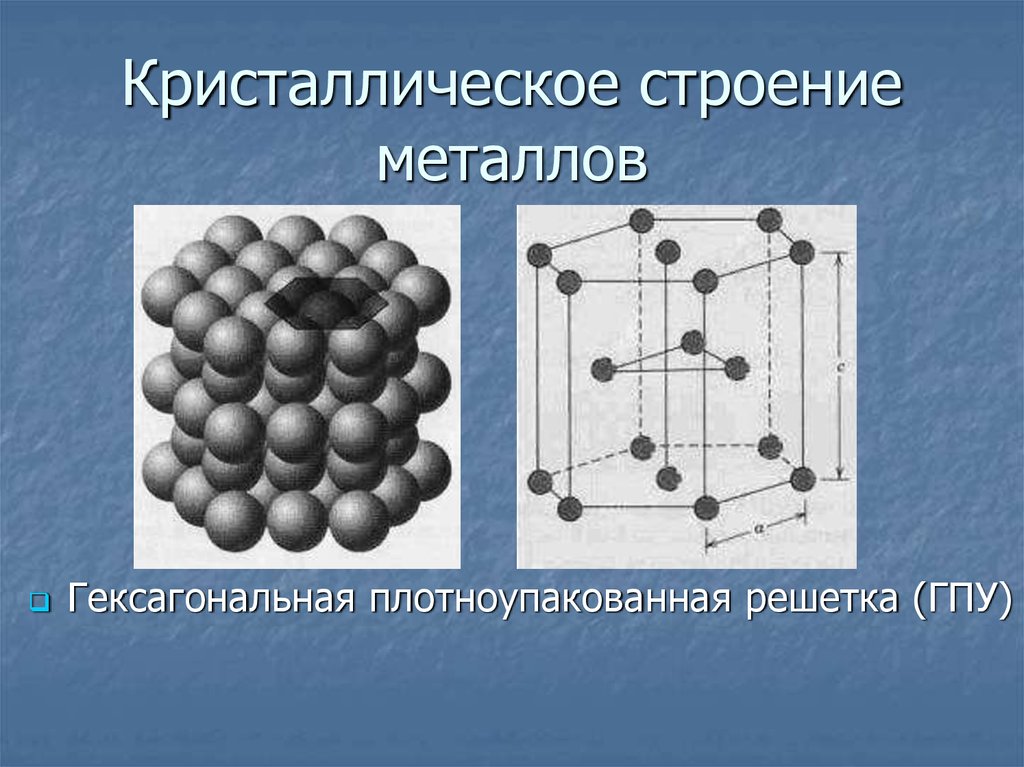 В результате получается более твердая и менее пластичная металлическая поверхность.
В результате получается более твердая и менее пластичная металлическая поверхность.
Деформационное упрочнение относится к деформации или холодному упрочнению металлической поверхности. По мере многократного изгиба или деформации металла пластичность металла снижается, он становится нагартованным и менее пластичным. Обычно относится к деформационному упрочнению металла при его обработке при комнатной температуре. Сплавы некоторых металлов, такие как никель-титан , не подвергаются деформационному упрочнению, но на самом деле имеют свойство снимать деформацию, когда возвращаются к исходной форме.
Упрочнение твердым раствором относится к металлу в процессе легирования, при котором легирующий компонент вводится в твердый материал. Один или несколько элементарных компонентов могут входить в нагретый, но твердый раствор. Затем металл быстро охлаждают, чтобы захватить элемент в твердом растворе.
Старение это процесс, который происходит быстро в первые несколько дней после отливки, а затем гораздо медленнее в течение следующих нескольких недель. Этот процесс часто называют «естественным старением». Другой искусственный вариант этого процесса может быть использован путем нагревания металла в течение короткого периода времени при высокой температуре. В результате он стабилизирует свойства, дополнительно укрепляя сплав. Этот процесс известен как «искусственное старение» или дисперсионное твердение.
Этот процесс часто называют «естественным старением». Другой искусственный вариант этого процесса может быть использован путем нагревания металла в течение короткого периода времени при высокой температуре. В результате он стабилизирует свойства, дополнительно укрепляя сплав. Этот процесс известен как «искусственное старение» или дисперсионное твердение.
Анодирование , процесс, специфичный для алюминия, имеет эффект упрочнения. Последним этапом создания анодированного алюминия является затвердевание и герметизация поверхности с помощью деионизированной кипящей воды или герметиков на основе солей металлов. Герметизация необходима для закрытия пор оксидной пленки и обеспечения однородности за исключением легирующих составляющих.
Цементация относится к процессу термической обработки поверхности, используемому для получения твердой износостойкой поверхности металла. Методы цементации включают науглероживание, цианирование, азотирование, закалку пламенем и электроиндукционную закалку.
Отпуск – это процесс термической обработки, используемый для холоднокатаных и холоднодеформированных металлов. Когда зернистая структура металла подвергается холодной штамповке, зерна растягиваются и изменяются. Поверхность становится более твердой, сопротивляясь деформации от контакта. Закалка нагревает холоднодеформированный металл до температуры, при которой зерна начинают растворяться друг в друге. Доступны серии стандартных темпераций. Эти состояния и их доступность в конкретном сплаве варьируются в зависимости от природы зерен при их рекристаллизации. Обозначение отпуска фактически определяется размером зерна, а не пределом текучести металла.
Обратная пескоструйная обработка металлическая поверхность — это способ выравнивания металла, который также значительно повышает твердость поверхности. Рекомендуется подвергнуть материал обратной струйной очистке после операций формования, потому что после пескоструйной обработки поверхности материал станет труднее обрабатывать и формировать.
 Ухудшают прочность и качество материала.
Ухудшают прочность и качество материала.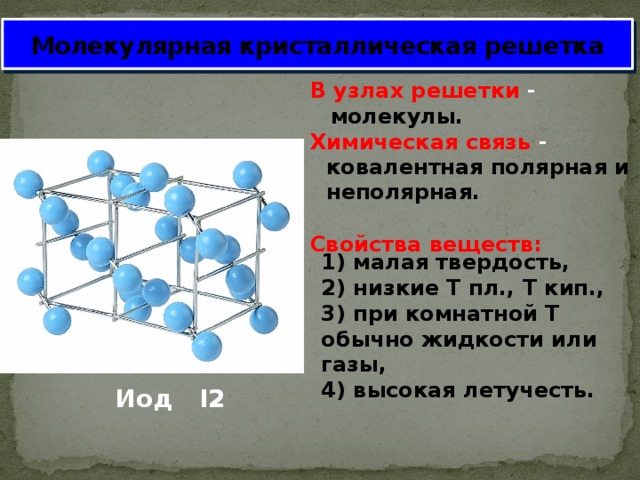 Устойчив к окрашиванию и коррозии и поэтому используется для столовых приборов и хирургических инструментов.
Устойчив к окрашиванию и коррозии и поэтому используется для столовых приборов и хирургических инструментов.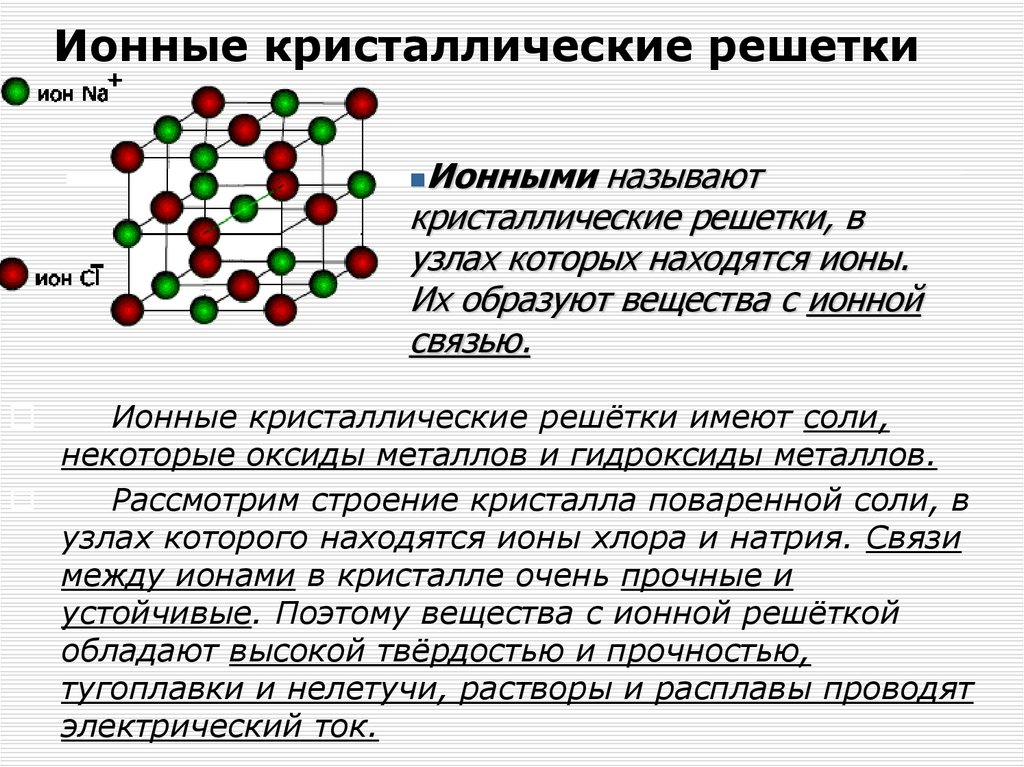 Используется в декоративных целях и в электроустановках.
Используется в декоративных целях и в электроустановках.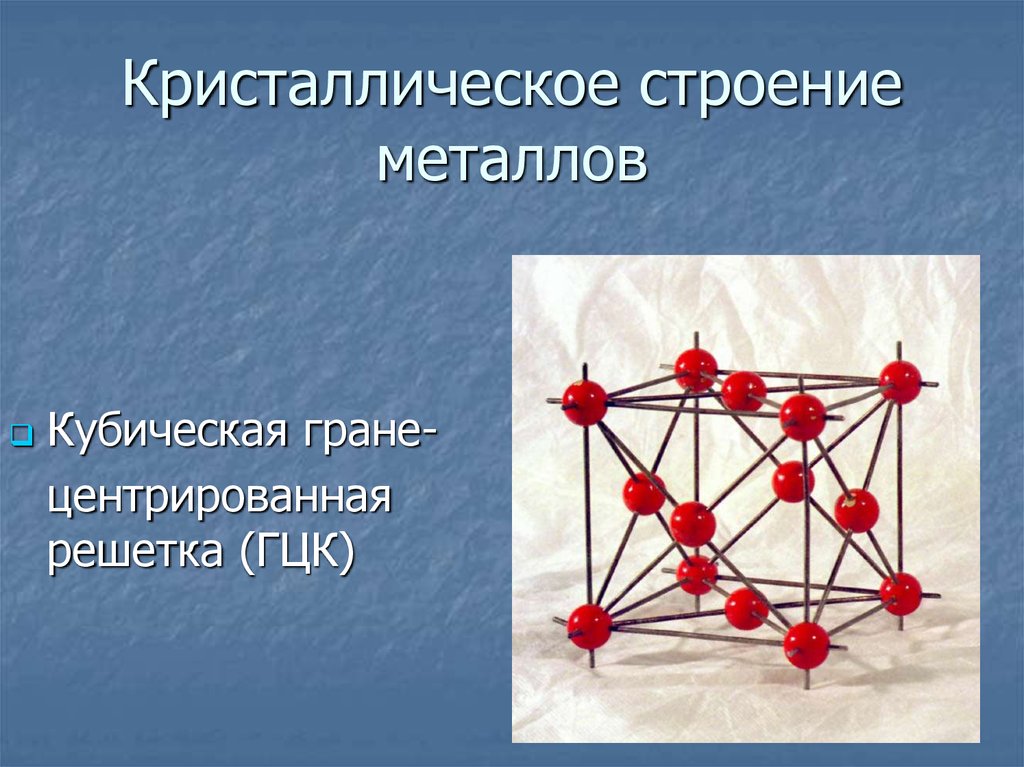
 Снижение твердости обычно сопровождается повышением пластичности, вследствие чего снижается хрупкость металла.
Снижение твердости обычно сопровождается повышением пластичности, вследствие чего снижается хрупкость металла.