Содержание
Неограниченной растворимостью системы медь — никель — Студопедия
Поделись
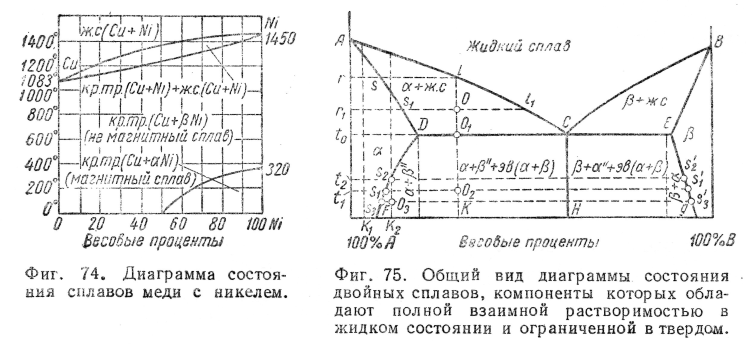
Сплав Сu–Ni относится к сплавам — твердым растворам II типа. Компоненты сплава имеют одинаковую кристаллическую решетку гранецентрированного куба и неограниченно растворимы как в жидком, так и в твердом состоянии. Взаимодействуя между собой они образуют единую кристаллическую решетку. Общий вид диаграммы состояния Сu – Ni приведен на рис. 3.6. Выпуклая линия АВ диаграммы является ликвидусом, выше которой все сплавы данной системы находятся в жидком состоянии. Вогнутая линия АВ (солидус), ниже которой сплавы с любой концентрацией представляют собой твердые растворы. Между ликвидусом и солидусом одновременно находятся две фазы: жидкий и твердый растворы.
Чтобы охарактеризовать фазовое состояние конкретного сплава при заданной температуре, необходимо определить природу фаз, находящихся в равновесии при данной температуре, их химический состав и относительное количество. Для этого используют правило отрезков, которое подробно рассмотрено выше.
Для этого используют правило отрезков, которое подробно рассмотрено выше.
| ||||||||||
| ||||||||||
| ||||||||||
| 0 20 40 60 80 100%Ni |
| 100%Cu Ni |
Рис.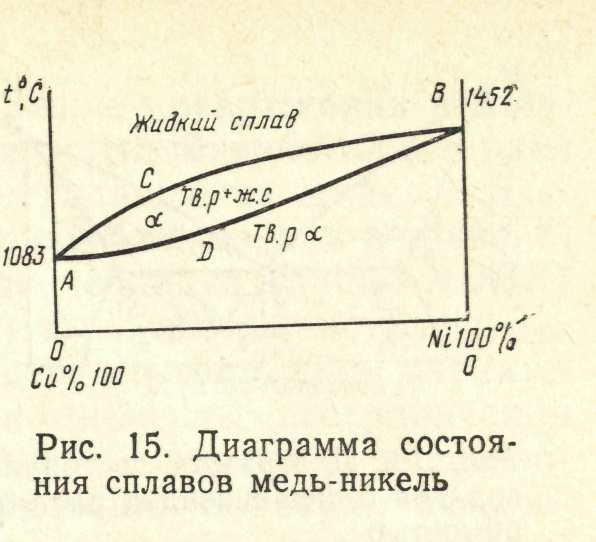 3.6. Диаграмма состояния сплава «медь—никель», образующего
3.6. Диаграмма состояния сплава «медь—никель», образующего
твердый раствор с неограниченной растворимостью
Анализ диаграммы проводим на примере изменения фазового состояния, происходящего при снижении температуры в сплаве, содержащем 72 % Ni и 28 % Сu (рис. 3.7).
Рис. 3.7. Диаграмма состояния системы «медь – никель»
Для определения фазового состава сплава в интервале кристаллизации применяют правило отрезков.
При охлаждении сплава из жидкого состояния ниже точки 1, лежащей на линии ликвидус, начинается кристаллизация, которая заканчивается при достижении температуры точки 2 на линии солидус. В двухфазной системе число степеней свободы С1-2 = 2–2+1=1. Скорость охлаждения снижается, т.к. затвердевание сплава сопровождается тепловым эффектом. Фазовые превращения выражаются уравнением α2 . После окончания кристаллизации структура сплава состоит из зерен твердого раствора α, имеющих одинаковый состав.
Однако в процессе кристаллизации концентрация компонентов постоянно изменяется: в жидком растворе – по линии ликвидус от точки 1 до точки 2′, а в растущих кристаллах твердого раствора α – по линии солидус от точки 1′ до точки 2 (показано стрелками на рис. 3.7).
3.7).
Поэтому микроструктура литого сплава (рис. 3.8, а) имеет ярко выраженную внутризёренную химическую неоднородность, называемую дендритной ликвацией. Это снижает коррозионную стойкость сплава. Для выравнивания химического состава, а, следовательно, повышения свойств, литой сплав подвергают деформированию с последующим отжигом. В результате микроструктура становится однородной (рис. 3.8, б).
а) б)
Рис. 3.8. Микроструктуры сплава Сu – Ni, содержащего 30% Ni
(Î135, травлено): а) – сплав литой; б) – сплав деформированный и
отожжённый
Применение сплавов твердых растворов:
1. Коррозионно-стойкие (нержавеющие) сплавы, свойства которых обеспечиваются однофазной структурой, устойчивой к электрохимическому воздействию (используются в атомных реакторах, подводных лодках, химической промышленности и т.п.).
2. Сплавы для резисторов, реостатных проволок (Сu – Ni, Ni – Мn), нагревательных элементов (Ni – Сr, Fе – Сr).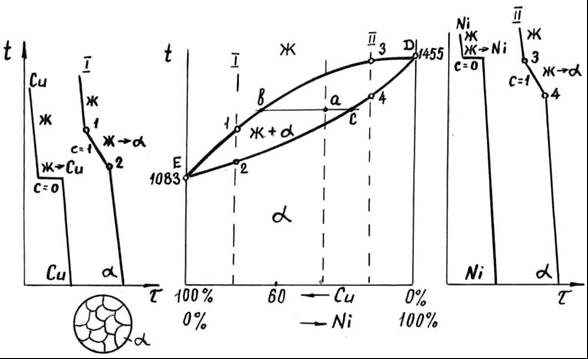 Их высокое электросопротивление обеспечивается благодаря наличию в кристаллической решетке металла-растворителя чужеродных атомов растворенного металла.
Их высокое электросопротивление обеспечивается благодаря наличию в кристаллической решетке металла-растворителя чужеродных атомов растворенного металла.
План составления отчета
1. Вычертить в масштабе диаграммы состояния Pb – Sb и Cu-Ni; используя правила фаз и отрезков, описать процессы кристаллизации и построить кривые охлаждения для сплавов заданной концентрации.
2. В промежуточной точке между линиями ликвидус и солидус определить количество сплава в жидком и твердом состоянии.
3. Зарисовать и описать схемы микроструктур.
4. Построить кривую охлаждения для сплава Pb – Sb заданной преподавателем концентрации.
Диаграмма состояния системы Cu-Ni
Диаграмма состояния
Определение 1
Диаграмма состояния – это графическое изображение состояния любого исследуемого сплава в зависимости от его температуры и химического состава (концентрации).
На диаграмме состояния показываются устойчивые, равновесные состояния, то есть обладающие минимальной свободной энергией.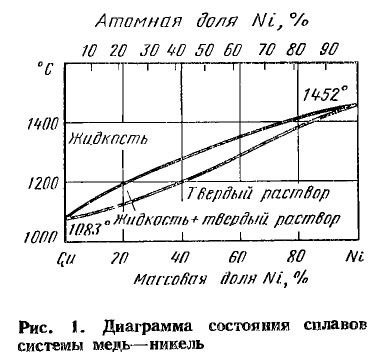 Такие диаграммы имеют большое практическое и теоретическое значение, потому что изучение сплава начинается с построения и анализа диаграммы состояния для структурных составляющих и фаз сплава. С их помощью устанавливаются возможности проведения термической обработки, определение режимов термической обработки, определения температуры литья, пластической горячей деформации и т. п.
Такие диаграммы имеют большое практическое и теоретическое значение, потому что изучение сплава начинается с построения и анализа диаграммы состояния для структурных составляющих и фаз сплава. С их помощью устанавливаются возможности проведения термической обработки, определение режимов термической обработки, определения температуры литья, пластической горячей деформации и т. п.
В абсолютно любой системе количество фаз, которые находятся в равновесии, зависит от внешних и внутренних условий. Закономерность изменений, которые происходят в системе, подчиняются закону Гиббса (правило фаз). Данным законом выражается зависимость между вариантностью (число степеней свободы), количеством фаз системы, а также к числом компонентов системы, находящихся в равновесии.
Определение 2
Вариантность – это количество внутренних и внешних факторов, которые можно изменять без изменения количества фаз в системе.
Построение диаграммы состояния может осуществляться различными методами. В большинстве случаев используется термический анализ, заключающийся в отборе сплавов исследуемой системы с разным соотношением масс, которые входят в состав компонентов. Для этого взяты сплавы помещаются в огнеупорные тигли и подвергаются нагреву в печи. После расплавления тигли охлаждаются, скорость охлаждения фиксируется. По полученным результатам строятся кривые охлаждения в координатах время-температура.
В большинстве случаев используется термический анализ, заключающийся в отборе сплавов исследуемой системы с разным соотношением масс, которые входят в состав компонентов. Для этого взяты сплавы помещаются в огнеупорные тигли и подвергаются нагреву в печи. После расплавления тигли охлаждаются, скорость охлаждения фиксируется. По полученным результатам строятся кривые охлаждения в координатах время-температура.
Температуры, которые соответствуют фазовым превращениям, — это критические точки. Точки начала процесса кристаллизации – это точки ликвидуса, а конца кристаллизации — точки солидуса. По критическим точкам различных сплавов строится диаграмма состояния, в ней:
- ось абсцисс – это концентрация компонентов,
- ось ординат – это температура.
Диаграмма состояния системы Cu-Ni
Сплав меди и никеля является твердым раствором второго типа. Компоненты этого сплава имеют одинаковую кристаллическую решетку в виде гранецентрированного куба, а также неограниченно растворимы в твердом и жидком состоянии. Взаимодействуя с друг другом они образовывают единую кристаллическую решетку. Пример диаграммы состояния системы медь-никель представлен на рисунке ниже.
Взаимодействуя с друг другом они образовывают единую кристаллическую решетку. Пример диаграммы состояния системы медь-никель представлен на рисунке ниже.
Рисунок 1. Диаграмма состояния системы медь-никель. Автор24 — интернет-биржа студенческих работ
Линия АВ является ликвидусом, то есть линией выше которой все сплавы системы находятся в жидком состоянии. Вогнутая линия АВ является солидусом, то есть линией ниже которой сплавы с любым химическим составом являются твердыми растворами. Между линиями солидуса и ликвидуса находятся одновременно твердый и жидкий растворы. Для того, чтобы дать характеристику определенного сплава при установленной температуре, сначала необходимо определить природу фаз, которые находятся в равновесии при этой температуре, их концентрацию (химический состав), а также относительное количество. Для этого используется правило отрезков. Проведем анализ диаграммы состояния медь-никель на примере изменения фазового состояния, которое происходит при снижении температуры в сплаве, состоящим из 28 % меди и 72 % никеля.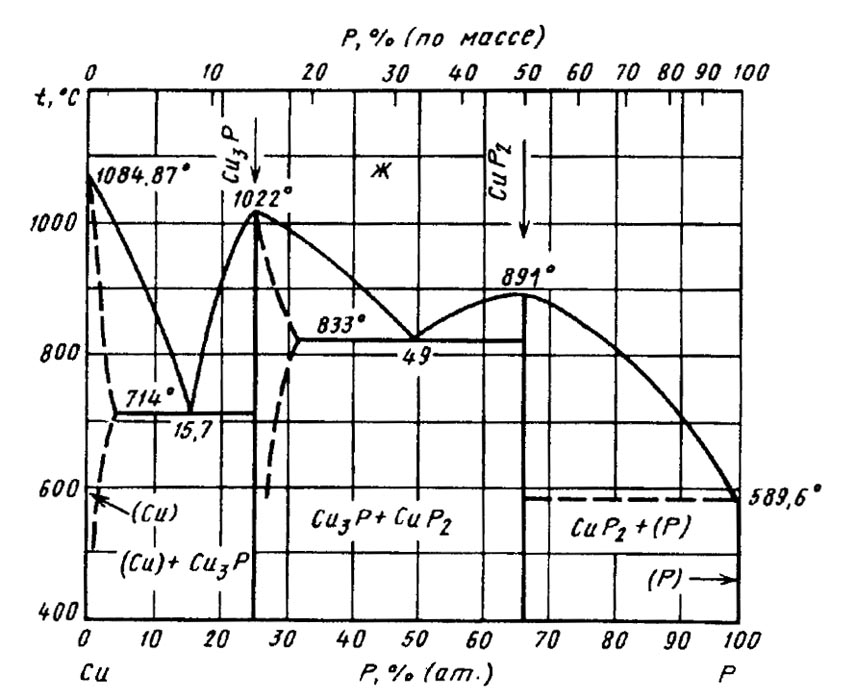 При охлаждении рассматриваемого сплава из жидкого состояния ниже точки 1, которая лежит на точке линии ликвидуса, начинается процесс кристаллизации, заканчивающийся при достижении температуры в точке 2 на линии солидуса. В системе двух фаз количество степеней свободы может быть рассчитано по следующей формуле:
При охлаждении рассматриваемого сплава из жидкого состояния ниже точки 1, которая лежит на точке линии ликвидуса, начинается процесс кристаллизации, заканчивающийся при достижении температуры в точке 2 на линии солидуса. В системе двух фаз количество степеней свободы может быть рассчитано по следующей формуле:
$С_{1-2} = 2-2+1=1$
Скорость охлаждения становится меньше, потому что процесс затвердевания сплава сопровождается тепловым эффектом, фазовые превращения могут быть выражены уравнением:
$Ж(t1-t2)=>a2.$
После окончания кристаллизации в состав структуры сплава входят зерна раствора а, с одинаковым составом. Однако, в процессе кристаллизации химический состав компонентов систем медь-никель постоянно изменяется. В жидком состоянии в растворе — по линии ликвидус от точки 1 до точки 2’. а в растущих кристаллах твердого состава а — по линии солидуса от точки 1’ до точки 2, как показано на рисунке ниже.
Рисунок 2. Диаграмма. Автор24 — интернет-биржа студенческих работ
По этой причине микроструктура литого сплава (представленного на рисунке ниже) имеет выраженную внутризеренную химическую неоднородность, которая называется дендритной ликвацией.
Рисунок 3. Микроструктура литого сплава. Автор24 — интернет-биржа студенческих работ
Это способствует снижению коррозионной стойкости исследуемого сплава. Чтобы выровнять химический состав, для увеличения полезных свойств, литой сплав может быть подвержен процесс деформирования с последующим отжигом. В результате данной операции микроструктура становится более однородной.
Свойства сплава медь-никель обеспечиваются благодаря однофазной структуре, которая устойчива электрохимическому воздействию, поэтому нашел применение в химической промышленности. Также сплав используется для производства реостатных проволок и резисторов. Высокое электрическое сопротивление обеспечивается наличием в кристаллической решетке металла-растворителя.
nglos324 — фазовая диаграмма
nglos324 — фазовая диаграмма
| ||||||||||
| А фазовая диаграмма показывает диапазон существования фаз в материалах с более одного компонента.  Бинарная фазовая диаграмма, показанная для медно-никелевого Бинарная фазовая диаграмма, показанная для медно-никелевогоуказывает на то, что эти материалы могут образовывать как жидкие, так и твердые растворы. во всем диапазоне составов от Cu до Ni. Выше 1728 К плавление точки чистого никеля сплавы находятся в жидкой фазе. Между 1728 К и 1357 К (температура плавления Cu) сплавы могут быть как твердыми, так и жидкими или существуют в виде двух равновесных фаз. Ниже 1357 К все системы сплавов являются твердыми телами. Линии ликвидуса и солидуса ограничивают двухфазную зону. В этой области при данной температуре составы твердого и жидкость, находящаяся в термодинамическом равновесии, определяется составом в точке пересечения изотермы с солидусом и ликвидусом линии соответственно. | ||||||||||
| От: Ньюи и Уивер, «Принципы и практика использования материалов», Баттерворт (1990) | ||||||||||
материалов —
материалов —
| ||||||||||||||||
Материалы | ||||||||||||||||
Медь | ||||||||||||||||
От: | ||||||||||||||||
Для любого | ||||||||||||||||

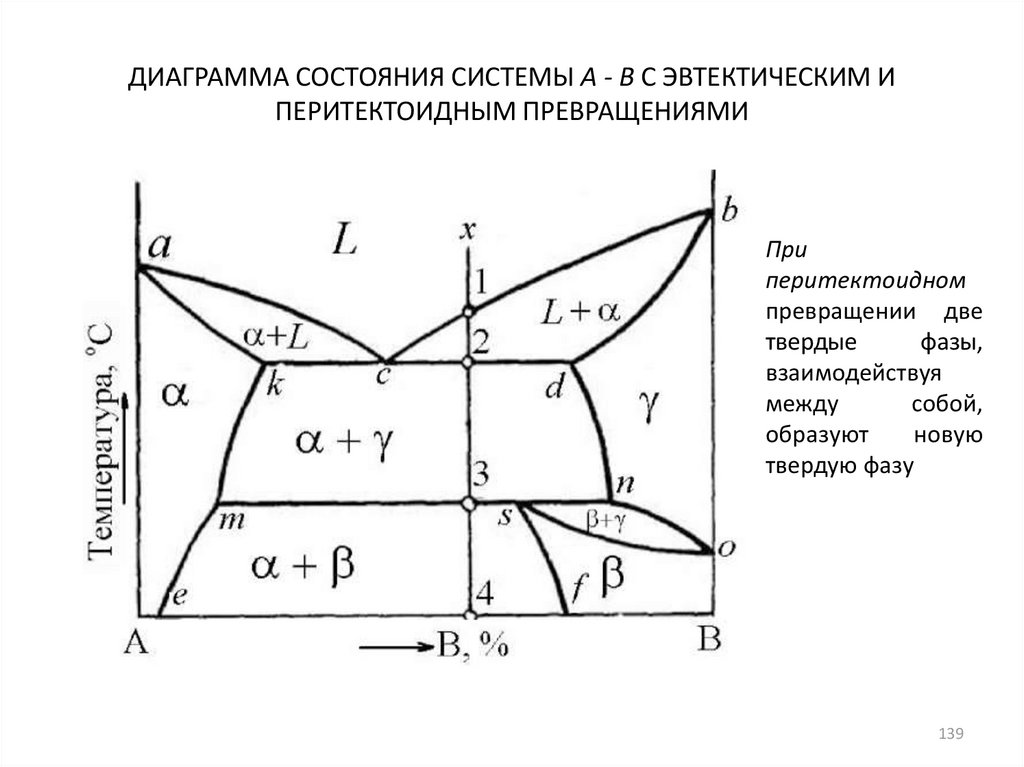 Равновесная «фазовая диаграмма»
Равновесная «фазовая диаграмма»