Технологический процесс хромирования. Хромирование электролизом
Технологический процесс хромирования
Технологические операции при ремонте (восстановлении) деталей хромированием выполняют в следующей последовательности.
Механическая обработка. Поверхности деталей, подлежащие хромированию, шлифуют до выведения следов износа и получения необходимой геометрической формы.
Промывка деталей в органических растворителях и протирка ветошью. В качестве растворителей применяют бензин, керосин, трихлорэтан, бензол и др.
Монтаж деталей на подвеску. Необходимо следить, чтобы детали одинаково отстояли от поверхности анода. Ванну следует загружать однородными деталями, укрепленными на одинаковых подвесках. Подвески и контакты должны быть изготовлены из одинаковых материалов. Контактные крючки рекомендуется изготавливать из бронзы и меди. В качестве материала для подвесок, применяют сталь, сечения подвесок рассчитывают, исходя из плотности тока 0,7… 1,0 А/мм2. Ежедневно аноды очищают от окислов и налета электролита.
Обезжиривание. Рекомендуется применять электролитическое обезжиривание в растворе следующего состава: едкий натр (NaOH)—30… 50 г/л; кальцинированная сода (iNa2C03)—25…30 г/л и жидкое стекло (Na2Si03) — 10 … 20 г/л.
Температура электролита — 60… 70°, плотность тока — 5….15 А/дм2. Время выдержки на катоде — 2… 3 мин, а на аноде — 1…2 мин. После обезжиривания детали сначала промывают горячей водой (60… 80°), а затем холодной. Обезжиривание считается законченным, если после промывки вода равномерно смачивает поверхность. После обезжиривания производится изоляция1 поверхностей, не подлежащих хромированию. Для изоляции можно применять перхлорвиниловый лак, лак АК-20, целлулоид,, винипласт, плексиглас, хлорвиниловые трубки или хлорвиниловую» изоляционную ленту.
Декапирование — это процесс обработки деталей в хромовом* электролите, состоящем из 100 г хромового ангидрида (СгОз) и 2…3 г серной кислоты (H&SO4) на 1 л воды.
Декапирование (травление) стальных деталей проводят в течение 30… 90 с при плотности тока 25… 40 А/дм2. А для деталей из серого чугуна лучшие результаты, в смысле прочности сцепления, достигаются при плотности тока 20… 25 А/дм2 и продолжителыюсти декапирования 25… 30 сек. Температура электролита во всех случаях должна быть 55… 60 °С.
Процесс хромирования. После анодного декапирования детали загружают в ванну хромирования и прогревают их при выключенном токе в течение 5… 6 мин, а затем дают полный ток согласно режиму хромирования. При хромировании чугунных деталей вначале в течение 3… 5 мин дают «толчок тока» при плотности, в 2…2,5 раза превышающей выбранную по режиму. Колебания температуры электролита могут быть в пределах ±1 °С. Не допускаются перерывы тока в процессе электролиза, так как они вызывают отслаивание хромового покрытия. Продолжить процесс после перерыва тока можно, если хромируемую поверхность подвергнуть анодному травлению при плотности тока 25… 30 А/дм2 в течение 30… 40 с, а затем изменить направление тока. В этом случае осаждение хрома следует начинать при катодной плотности тока 20… 25 А/дм2 и постепенно увеличивать до нормальной.
Аноды для хромирования изготавливают из чистого свинца или сплава, состоящего из 92…93% свинца и 7… 8% сурьмы. Аноды из чистого свинца в большей степени покрываются нерастворимой и непроводящей пленкой хромовокислого свинца, чем аноды из сплава свинца и сурьмы. В большинстве случаев аноды изготавливают плоскими и цилиндрическими. При хромировании деталей сложной конфигурации очертания анода определяются формой катода. Расстояние между анодами и деталями рекомендуется делать 30… 35 мм, но не более 50 мм. Расстояние деталей от днища ванны должно составлять не менее 100… 150 мм, а от верхнего уровня электролита — не менее 50… 80 мм. Уровень электролита должен быть ниже верхних кромок ванны на 100…150 мм. При завешивании деталей в ванну необходимо, чтобы все участки анодов были одинаково удалены от противоположных участков катода. При этом толщина слоя хрома откладывается равномерно по всей поверхности детали.
Глубина погружения анодов и деталей (катодов) в ванну должна быть одинаковой, так как при различной глубине на краях хромируемых деталей образуются утолщения, искажающие форму. Скорость осаждения слоя хрома при плотности тока 40… 100 А/дм2 составляет 0,03… 0,06 мм/ч.
По окончании процесса хромирования детали выгружают из ванны и вместе с подвесками промывают в холодной воде (в сборнике электролита) 15… 20 с. Окончательно детали моют в холодной проточной воде.
Обработка после покрытия. Промытые и очищенные от изоляции детали иногда подвергают термической обработке при температуре 150—200°С в течение 2…3 ч, а затем механической.
Для шлифования применяют круги мягкие или средней твердости с размером зерна от 60 до 120. Шлифование ведут при интенсивном охлаждении жидкостью и при скорости круга 20…30.м/с и выше. Скорость вращения детали—12…20 м/мин.
Режимы электролиза. Процесс осаждения хрома и свойства хромовых покрытий зависят от режима, при котором осаждается хром на поверхности металла, т. е. от катодной плотности тока и температуры электролита. Наиболее ясное представление о примерных границах режимов электролиза, обеспечивающих получение серого, блестящего и молочного осадков хрома, дает диаграмма плотности тока и температуры (DK—t), изображенная на рисунке 19.
Серый осадок хрома появляется на катоде при низких температурах электролиза (35…50 °С) и широком диапазоне плотностей тока. Осадки блестящего* хрома обладают высокой твердостью (6000… 9000 Н/мм2), высокой износостойкостью и меньшей хрупкостью.
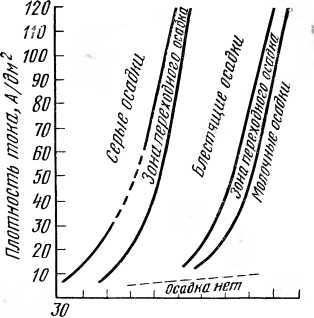 Рис. 19. Зоны хромовых осадков.
Рис. 19. Зоны хромовых осадков. Молочный хром получается при более высоких температурах, электролита (выше 70 °С) и широком интервале плотностей тока. Молочные осадки отличаются пониженной твердостью (4400..-6000 Н/мм2), пластичностью и повышенной коррозионной стойкостью.
Пористое хромирование. Пористое хромирование применяется при ремонте деталей, работающих на трение в паре с различными металлами и сплавами при высоких удельных давлениях и окружных скоростях или при повышенных температурах. К таким деталям относятся гильзы цилиндров двигателей внутреннего сгорания, коленчатые валы и др.
Пористые хромовые покрытия можно получать механическим,, химическим и электрохимическим способами.
При механическом способе на поверхность детали до хромирования наносят углубления в виде пор или каналов. Такую подготовку обеспечивают накаткой специальным роликом, дробеструйной обработкой и другими способами. После хромирования воспроизводятся неровности, полученные при подготовке.
Химическим способом получают пористость путем травления поверхности в соляной кислоте.
Наибольшее распространение получил электрохимический способ получения пористого хрома. Этот способ заключается в анодной обработке хромированных деталей в электролите того же состава. В зависимости от режимов хромирования пористость хромовых покрытий бывает двух типов — канальчатая и точечная.. При ремонте гильз цилиндров, втулок, коленчатых валов и подобных им деталей применяется канальчатый тип пористости. Такук> пористость и наименьший износ в условиях трения можно получить при хромировании в электролите, состоящем из 250 г Сг03 и 2,5 г h3S04 на 1 л воды, при температуре электролита ¦60+1 °С и катодной плотности тока 55… 60 А/дм2. Травление ведут при плотности анодного тока 35 …45 А/дм2 в течение 8 мин в том же электролите.
Точечная пористость образуется при хромировании в универсальном электролите при плотности тока 45… 55 А/дм2 и температуре 50… 55 °С. Анодную обработку проводят так же, как и при канальчатой пористости, т. е. при плотности тока 35… 45 А/дм2 в течение 8 мин.
Хромирование в саморегулирующемся электролите. В последнее время разработан новый хромовый электролит, называемый скоростным саморегулирующимся, его состав: хромовый’ ангидрид — 225… 300 г/л, кремнефтористый калий — 20 г/л и сернокислый стронций — 6 г/л.
В таком электролите выход по току при хромировании составляет 17… 22%. Саморегулирующимся он назван потому, что при электролизе в нем автоматически поддерживается необходимая концентрация анионов, вводимых в хромовый электролит. Это происходит в результате избыточного количества труднорастворимых солей кремнефтористого калия и сернокислого стронция, растворимость которых изменяется в зависимости от концентрации хромового ангидрида и температуры электролита.
Чтобы получить износостойкое покрытие в саморегулирующемся электролите, рекомендуют соблюдать следующие режимы хромирования: плотность тока 50… 100 А/дм2, температура электролита 45… 55°С. Молочные осадки можно получить при температуре электролита 55… 70 °С и плотности тока 20… 35 А/дм2. Микротвердость покрытий из саморегулирующегося электролита составляет 3000… 13 000 Н/мм2.
Недостаток такого электролита — сильное взаимодействие его со сталью и другими металлами, в результате чего происходит растравливание обрабатываемых поверхностей. Поэтому загружать детали в ванну необходимо только при включенном токе. Аноды для хромирования в саморегулирующемся электролите рекомендуется применять из сплава: 90% свинца и 10% гост олово. Чтобы приготовить саморегулирующийся электролит, в ванне хромирования растворяют нужное количество хромового ангидрида и доливают воду до рабочего уровня. Предварительно хромовый ангидрид подвергают анализу на содержание серной кислоты, которую удаляют из электролита путем добавления в него углекислого бария или стронция. На 1 г серной кислоты вводят 2,2… 2,3 г углекислого бария или 1,53 г углекислого стронция. После осаждения серной кислоты в электролит вводят нужное количество сернокислого стронция и кремнефтористого калия и нагревают до температуры 50…60°С. Нагревание длится 15… 16ч при периодическом перемешивании через каждые 2… 3 ч. После этого электролит готов к эксплуатации.
Корректируют электролит путем систематического добавления хромового ангидрида. Вместе с хромовым ангидридом вводят углекислый стронций. Кремнефторид калия и сернокислый стронций в количестве 1 г/л добавляют, когда поверхность отхромированных деталей приближается к 1 м2.
Контроль хромовых покрытий. В производственных условиях качество покрытий следует проверять внешним осмотром и замером размеров хромированных поверхностей. При внешнем осмотре необходимо обращать внимание на блеск, отслоение и плотность осадка, равномерность и отсутствие шелушения и другие видимые дефекты. Дефекты покрытий получаются в результате неисправностей в работе ванн хромирования, например отслаивание покрытия возникает в результате недостаточного обезжиривания и декапирования, а также при наличии перерывов тока в процессе хромирования. Шелушение осадков появляется при недостаточном контакте детали с подвеской или при повышенной плотности тока. Неравномерное покрытие может быть при образовании пленки хроматов свинца на анодах, недостатке серной кислоты, избытке трехвалентного хрома. Во избежание перечисленных выше дефектов, необходимо откорректировать электролит и устранить другие неполадки в работе ванн хромирования.
Оборудование. Схема расположения оборудования участка восстановления деталей хромированием приведена на рисунке 20.
Источники тока — выпрямители с напряжением 12 В ВАКГ-12/6-3000, ВАГГ-12/600М, ВАС-600/300 и другие, а также низковольтные генераторы АНД 500/250, 750/375, 1000/500, 1500/750. Ванны для гальванического участка изготавливают из листовой стали толщиной 4… 5 мм. Облицовка для ванн промывки и обезжиривания не требуется. Внутреннюю поверхность ванны хромирования облицовывают свинцом.
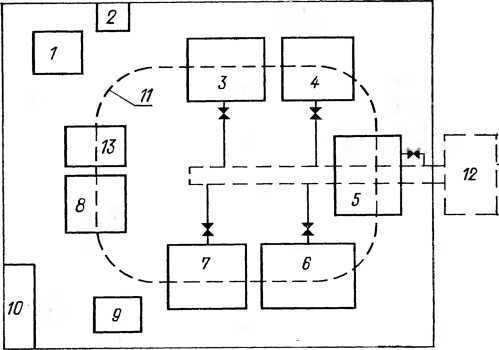 Рис. 20. Расположение оборудования на участке восстановления деталей хромированием:1 — выпрямитель; 2 — электрощитг; 3 — ванна для электрохимического обезжиривания; 4 — ванна для горячей промывки; 5 — ванна для холодной промывки; 6 — ванна для декапирования; 7 — ванна для хромирования; 8 — ванна для улавливания электролита; 9 — шкаф сушильный; 10— стеллаж ремфонда; 11 — электротельфер; 12 — сборник-нейтрализатор; 13 — стол для монтажа и демонтажа.
Рис. 20. Расположение оборудования на участке восстановления деталей хромированием:1 — выпрямитель; 2 — электрощитг; 3 — ванна для электрохимического обезжиривания; 4 — ванна для горячей промывки; 5 — ванна для холодной промывки; 6 — ванна для декапирования; 7 — ванна для хромирования; 8 — ванна для улавливания электролита; 9 — шкаф сушильный; 10— стеллаж ремфонда; 11 — электротельфер; 12 — сборник-нейтрализатор; 13 — стол для монтажа и демонтажа. Себестоимость восстановления 1 дм2 поверхности хромированием в универсальном электролите при толщине покрытия 0,1 мм ориентировочно составляет 44,8 коп., 0,2 мм — 52,0 коп., 0,3 мм—-58,6 коп.
Электролитическое железо имеет светло-серый цвет, обладает достаточно высокой твердостью и износостойкостью. Химический состав электролитического железа зависит от состава исходных материалов, используемых при электролизе.
При обычном осаждении с применением стальных растворимых анодов содержание примесей в покрытиях находится в пределах: 0,035 …0,06% С; 0,03 …0,05% S; 0,05 …0,01% Р, 0,0009… 0,023% Si; до 0,01% Мп.
В электролитических осадках железа имеются также примеси таких металлов, как Mg, Со, Ni и другие, обусловленные содержанием этих металлов в анодах и электролитах. Кроме этого, электролитическое железо содержит значительное количество водорода, выделяющегося на катоде вместе с железом. Атомный вес железа 55,85 г. Электрохимический эквивалент 1,042 г/А-ч.
Составы электролитов. На ремонтных предприятиях наибольшее распространение для железнения получили горячие хлористые электролиты, состоящие из двух компонентов: хлористого железа и соляной кислоты. В ремонтной практике чаще всего применяют четыре вида хлористых электролитов, отличающихся концентрацией железа.
Малоконцентрированный электролит содержит 200 …250 г/л хлористого железа (FeCl2-4h30). При температуре 60… 80 °С и плотности тока 30… 50 А/дм2 электролит обеспечивает получение плотных, гладких мелкозернистых осадков железа с твердостью 4500… 6500 Н/мм2, толщиной 1,0… 1,5 мм. Выход железа по току составляет 85… 95%. Скорость осаждения железа равна 0,4… 0,5 мм/ч на сторону. Электролит допускает колебание кислотности при электролизе от 0,8 до 1,5 г/л, которое незначительно отражается на механических свойствах покрытий. Недостатком этого электролита является постепенное увеличение концентрации железа в процессе электролиза в результате несоответствия между скоростью растворения анодов и скоростью осаждения железа на катоде, что вызывает затруднения при обслуживании ванны железнения.
Среднеконцентрированный электролит оптимальной концентрации содержит 300…350 г/л хлористого железа (FeCl2-4h30). Катодный выход железа из этого электролита при температуре 75 °С и плотности тока 40 А/дм2 составляет 96%. В этом электролите анодные и катодные выходы железа по току становятся примерно одинаковыми, концентрация железа остается почти неизменной и электролит длительное время по концентрации железа не требует корректировки. В настоящее время этот электролит нашел широкое применение на ремонтных предприятиях.
Среднеконцентрированный электролит содержит 400 …450 г/л хлористого железа. Электролит используется для восстановления деталей, имеющих достаточно высокие износы и сравнительно невысокую твердость. Электролит дает возможность получать гладкие плотные покрытия толщиной до 2 мм и твердостью 2500… 4500 Н/мм2. Электролит также находит применение для восстановления посадочных отверстий в корпусных, деталях.
Высококонцентрированный электролит содержит 600… 680 г/л хлористого железа. Электролит при температуре 95… 105°С и плотности тока 5…20 А/дм2 позволяет получать мягкие (120… 200 кг/мм2), вязкие покрытия толщиной 3… 5 мм..
Электролиты более высокой концентрации рекомендуется применять в случаях, когда к восстанавливаемым деталям не предъявляются повышенные требования по твердости рабочих поверхностей.
За последнее время разработаны холодные электролиты, позволяющие применять более высокие плотности тока и обеспечивающие высокую производительность процесса.
Хлористый марганец МпС12-4Н20 Аскорбиновая кислота Двухлористое железо FeCl2-4h30 Хлористый марганец МпС12-4Н20 Хлористый калий КС1 (или) NaCl Аскорбиновая кислота Двухлористое железо FeCl2*4h30 Сернокислое железо FeS04*7h30 Двухлористое железо FeCl2-4h30 Метилсульфатное железо Fe (Ch4OSO3) 2*4Н20
Хлористые электролиты без добавок, приведенные в таблице* позволяют получать качественные износостойкие покрытия толщиной 0,6… 1,0 мм и обеспечивать восстановление широкой номенклатуры изношенных деталей до нормальной работоспособности и номинальных размеров. Электролит, в состав которого» входят двухлористое железо и йодистый калий, обеспечивает по-пучение качественных осадков, железа’ при условии применения асимметричного переменного тока.
Присутствие аскорбиновой кислоты в электролитах позволяет вести электролиз в широких пределах значений pH от 1,8 до 6,0, что значительно упрощает регулирование кислотности электролита. Электролит, состоящий из двухлористого железа и метил-сульфатного железа, по сравнению с хлористым менее агрессивен и более устойчив к окислению. Покрытия, полученные из этого электролита, имеют меньшее количество трещин, обладают более равномерной структурой.
Приготовление и корректирование электролита. Для приготовления хлористого электролита используют двухлористое железо (Fe€l2-4h30).
Соляная кислота (НС1) применяется в виде водного раствора разной концентрации с плотностью от 1,14 до 1,20. Приготовление электролита производится в следующем порядке. В ванну заливают проточную или дистиллированную воду комнатной температуры и добавляют соляную кислоту из расчета 0,5 г/л воды. В подкисленную воду засыпают двухлористое железо, выдерживая требуемую концентрацию, и перемешивают до полного растворения. После растворения двухлористого железа электролит должен отстояться в течение 1 … 2 ч, пока не примет светло-зеленый цвет. Затем электролит проверяют на кислотность. Нормальная кислотность должна быть pH 0,8… 1,2. При необходимости добавляют недостающее количество кислоты в соответствии с ее плотностью, приведенной ниже.
Плотность кислоты, г/см3 1,14 1,15 1,16 1,17 1,18 1,19 1,20 Количество кислоты, г/л 20 19 18 17 16 15 14 Количество кислоты, см*/л……. 18 16,6 15,5 14,6 13,6 12,6 11,6
Приготовленный таким образом электролит следует проработать током при плотности 30 А/дм2 и соотношение поверхностей анодов и катодов Sa : SK = 2 : 1 в течение двух часов.
Удельный вес электролита (плотность) г/см8 1,12 1,15 1,17 1,20 1,23 1,26 1,29 1,32 1,35 Концентрация железа, г/л … 200 260 300 350 400 450 500 550 600. Контроль кислотности электролита можно осуществлять с помощью индикаторной бумаги «Рифан» с pH 0,3 …2,2 или потенциометров ЛПУ-01, ЛПМ-60.
sxteh.ru
6. Хромирование - Стр 2
УСЛОВИЯ ХРОМИРОВАНИЯ.
Процесс износостойкого хромирования по сравнению с защитно-декоративным обладает некоторыми особенностями: 1) Напряжение на клеммах ванны более (около 5,5 в), что является результатом применения менее концентрированных электролитов. 2) Плотности тока, применяемые при хромировании, более высокие. 3) Толщина слоя хрома несоизмеримо больше, что является причиной значительной продолжительности процесса, достигающей в отдельных случаях 24 час. 4) Режим электролиза следует поддерживать в строго установленных пределах. Отклонения от установленной величины плотности тока и температуры электролита в процессе электролиза могут вызвать дополнительные напряжения в слое осажденного хрома. 5) Хромированию подвергаются обычно стальные и чугунные детали машин без покрытия промежуточным слоем какого-либо другого металла. Режимы хромирования, обеспечивающие получение блестящих (более твердых) и молочных (сравнительно мягких и эластичных) осадков, выбираются в зависимости от назначения деталей, условий их службы и требований, предъявляемых к покрытию. Ниже приведены основные режимы хромирования для получения осадков того или другого типа: а) при осаждении блестящего хрома:
Температура электролита ……………………………54 – 56о Катодная плотность тока Dк………………………….30 – 50 а/дм2 Температура электролита…………………………….66 – 68о Катодная плотность тока Dк………………………….80 – 100 а/дм2
б) при осаждении молочного хрома:
Температура электролита ……………………………68 – 72о Катодная плотность тока Dк………………………….25 – 30 а/дм2
в) при осаждении молочно-блестящего (дымчатого) хрома:
Температура электролита ……………………………60 – 65о Катодная плотность тока Dк………………………….30 – 35 а/дм2
При выборе режима хромирования следует считаться с рельефностью детали и формой применяемого анода, определяющими степень неравномерности распределения тока между ближними и дальними участками детали. При хромировании может оказаться, что отдельные участки поверхности детали не покрываются хромом. Для предупреждения этого рекомендуются следующие меры. При покрытии хромом деталей, имеющих некоторый рельеф, или при одновременном покрытии однотипных деталей, смонтированных на нескольких подвесках, хромирование следует начинать с толчка тока. При этом плотность тока должна быть, примерно, в 1,5 раза больше заданной. Продолжительность толчка тока составляет 2-3 мин., затем плотность тока постепенно, в течение нескольких минут, снижают до установленной величины. Если по техническим причинам невозможно создание толчка тока, то хромирование следует начинать хотя бы при установленной величине плотности тока или близкой к ней. Совершенно не допускается начинать электролиз с небольшой плотности тока, а затем повышать ее до требуемой величины. Размерное хромирование. Сущность размерного хромирования состоит в том, что детали покрываются слоем хрома точно до заданного размера и направляются в производство без последующей механической обработки. Размерное хромирование создает экономию в хромовом ангидриде и расходах на механическую обработку детали. При размерном хромировании требуется осадить слой хрома совершенно одинаковой толщины и точно сохранить первоначальную форму детали, например, при хромировании цилиндрических деталей не допускается конусность или овальность. Для размерного хромирования требуется применение фигурных анодов, специальных подвесных приспособлений, позволяющих жестко монтировать детали и аноды, а также изолирующих экранов. Монтаж должен выполняться таким образом, чтобы в процессе электролиза концентрация силовых линий тока была одинаковой на всей поверхности хромируемой детали. Значение величины выхода по току и плотности тока при хромировании позволяет точно определить время, необходимое для осаждения требуемой толщины стоя хрома. Расчет производится по формуле
τ = 1314 мин.,
где τ – время в мин., δ – толщина покрытия в мк, Dk – катодная плотность тока в а/дм2, η – выход по току в %.
Однако для получения доброкачественного слоя хрома строго определенной толщины необходимо, чтобы поверхность покрытия не была шероховатой или пористой. Поэтому следует обратить внимание на чистоту поверхности детали перед покрытием (отсутствие царапин, пор и т.д.) и правильность состава электролита. Если к покрываемой детали предъявляется высокие требования в смысле чистоты поверхности и границ допуска на изготовление, то размерное хромирование пригодно только при сравнительно малых толщинах слоя хрома. Примером могут служить гладкие калибры, хромируемые на толщину слоя 10-30 мк. Сравнительно толстые покрытия возможно наносить при размерном хромировании деталей с более широкой границей допусков, например, цилиндров двигателей внутреннего сгорания. Для этих деталей допускается некоторая конусность и эллипсность, величины которых практически лежат около 0,01 мм.
ХРОМИРОВАНИЕ АЛЮМИНИЯ.
7h3O, 200 г/л NaOH) в течение 30-40 сек., затем промывают водой и производят обработку в разбавленном 1:1 растворе HNO3 в течение 5-7 сек. Деталь промывается в воде и вновь погружается в тот же цинкатный раствор на 10 сек. После промывки деталь замешивается в ванну хромирования (желательно под током) и хромируется при обычных режимах. Хорошие результаты дает также гидропескоочистка с завешиванием деталей, покрытых мокрым песком, под током в ванну хромирования.При непосредственном хромировании алюминиевых сплавов основной задачей является подготовка поверхности детали к покрытию. Для этого деталь из алюминия или алюминиевого сплава протирается тканью, смоченной бензином, и обезжиривается в течение 3-5 мин. в растворе: 50 г/л Na2CO3, 50 г/л Na3PO4, 30 г/л жидкого стекла при T = 60-65о. После промывки в горячей и холодной воде, деталь обрабатывают в цинкатном растворе (200 г/л ZnSO4
ПЕРСПЕКТИВЫ РАЗВИТИЯ ХРОМИРОВАНИЯ.
Обзор способов хромирования и областей его применения свидетельствуют о широком использовании хрома в промышленности. Однако не все возможности технологии хромирования исчерпаны. В настоящее время исследования в области хромирования производятся в различных направлениях. Однако из таких направлений имеет в виду интенсификацию и стабилизацию процесса хромирования. Этот вопрос одновременно решается различными путями. Первый путь состоит в повышении катодной плотности тока при хромировании до 200-300 а/дм2. Наряду с повышением катодной плотности тока для получения блестящих осадков хрома необходимо также увеличивать температуру электролита, т.е. придерживаться рабочего интервала хромовой ванны. При этом скорость осаждения хрома возрастает не только за счет применения более высоких плотностей тока, но также за счет увеличения выхода по току. Второй путь состоит в повышении выхода хрома по току при помощи понижения температуры хромирования и изменения состава ванны. Покрытие имеет серо-матовый цвет, но легко полируется: пористость его ниже, а пластичность выше, чем у обычных хромовых покрытий. Третий путь состоит в изыскании возможности применения растворов с низкой валентностью хрома, обеспечивающих к тому же высокий выход по току. Наряду с этим важное значение придается стабильной работе электролитов промышленного состава. Так, НИИХИММАШ предлагает саморегулирующийся электролит, имеющий состав: ромового ангидрида – 250 г/л, сернокислого стронция 5 г/л, кремнефтористоводородного натрия – 20 г/л, двухромовокислого калия – 20 г/л. В таком электролите содержание сульфат иона автоматически регулируется введением труднорастворимой соли стронция. Второе направление имее целью получение хромовых покрытий с более высокими свойствами. Сюда следует отнести работы по получению особенно твердых, износостойкиз и коррозионностойких покрытий посредством карбидизации слоя электролитического хрома в парах бензина при T = 1050о. Большой интерес представляют работы по получению хромовых покрытий, хорошо удерживающих на поверхности смазку, что достигается наложением при хромировании переменного тока на постоянный. Для получения пористого хрома высокого качества большое значение имеют работы по осаждению пористых хромовых покрытий токами переменной полярности. Таким образом, накопившихся к настоящему времени опыт по практическому применению хромирования и новые исследования в этой области создают предпосылки для совершенствования технологии процесса электролиза и дальнейшего улучшения свойств хрома.
ТЕХНИКА БЕЗОПАСНОСТИ.
При приготовлении электролита и эксплуатации ванны хромирования необходимо соблюдение правил техники безопасности. Хромовый электролит легко окисляет органические вещества, поражает кожу и слизистые оболочки дыхательных путей. Рабочие, обслуживающие хромовые ванны, должны снабжаться резиновой спецодеждой: фартуками, перчатками и сапогами. Для предохранения глаз необходимо иметь защитные очки. Ванна хромирования должна быть обеспечена безупречно действующей бортовой вентиляцией. Перед работой носовую полость необходимо смазывать мазью, состоящей из двух частей вазелина и одной части ланолина. При попадании хромовой кислоты на кожу рук, образовавшееся темное пятно следует смыть раствором, состоящим из одной части спирта, одной части соляной кислоты и двух частей воды. Хромировочный участок цеха должен быть снабжен песком и огнетушителями. Бензин, керосин, ветошь, целлулоид и т.п. горючие и легковоспламеняющиеся материалы допускается иметь на участке в количествах, необходимых лишь для текущей работы. Хранить их следует в металлических плотно закрывающихся ящиках.
8. ИСПОЛЬЗУЕМАЯ ЛИТЕРАТУРА.
1. “Хромирование и железнение” авт. М.Б. Черкез. Государственное научно-техническое издательство машиностроительной литературы. 2. “Краткий справочник гальванотехника” авт. А.М. Ямпольский и В.А. Ильин. Ленинград “Машиностроение” 1981г. 3. “Гальванические покрытия в машиностроении” Справочник. Москва “Машиностроение” 1985г.
studfiles.net
Электролиты для хромирования

Основными составляющими электролитов являются хромовый ангидрид и серная кислота. Хромовый ангидрид СгО3 - плавленая кристаллическая масса вишнево-красного цвета. Растворимость в воде при 20 °С до 625 г/л. Хромовый ангидрид, оставленный на воздухе в барабане или в кусках на полу, легко соединяется с влагой воздуха, превращаясь в хромовую кислоту, и как энергичный окислитель быстро разрушает все органические вещества, с которыми он соприкасается.
Технический хромовый ангидрид может содержать до 0,4 % SO4 в пересчете на h3SO4, что следует учитывать при приготовлении и корректировании ванн хромирования. Поэтому при зарядке сначала в ванну закладывают полностью расчетное количество хромового ангидрида, заливают водой до заданного объема и дают полностью раствориться. После перемешивания раствора отбирают пробу для анализа на содержание иона SO4- и лишь после получения результата вводят в ванну недостающее количество серной кислоты.
Серная кислота h3SO4 (ГОСТ 4204) - химически чистая, вязкая бесцветная жидкость, плотность - 1,84 г/см3. Приливание кислоты в ванну хромирования следует производить в расчетном количестве, при энергичном перемешивании.
Стандартный электролит
Ориентировочный состав стандартного электролита содержит, г/л:
хромовый ангидрид - 150-250; серная кислота - 1,5-2,5.
При наличии целого ряда ценных свойств стандартный электролит обладает и некоторыми недостатками. Так, он чувствителен к колебаниям температуры, допуская отклонения от рабочего интервала температур лишь в пределах ±2 °С в течение всего времени процесса хромирования, длящегося обычно несколько часов. Если отклонение от заданной температуры превысит норму во время осаждения, то возникнут внутренние напряжения в хромовом покрытии, которые могут привести к его отслаиванию. Аналогичное действие оказывают и колебания плотности тока.
Кроме того, поддержание правильного соотношения между концентрациями хромового ангидрида и серной кислоты, равного 100:1, связано с частыми корректированиями и с введением добавок серной кислоты. Катодный выход по току весьма низок и находится в пределах 12-13 %, вследствие чего необходимо затрачивать большое количество времени и электроэнергии для получения износостойкого слоя хрома достаточной толщины.
Саморегулирующийся электролит
Этих недостатков лишен «саморегулирующийся» электролит, который имеет следующий состав (г/л) и режим работы (ГОСТ 9.047):
хромовый ангидрид - 225-300; сернокислый стронций - 5,5-6,5; кремнефтористый калий - 18-20; хром трехвалентный - 3-10; температура, °С - 55-65; плотность тока, А/дм2 - 40-70; выход по току, % - 18.
Характерной особенностью этого электролита является, прежде всего, постоянная концентрация аниона SO2-, составляющая 2,5 г/л. Это явление связано с тем, что сернокислый стронций и кремнефтористый калий имеют весьма ограниченную растворимость в воде и в рабочем диапазоне температур поддерживают в растворе заданную концентрацию аниона SO2-. Так как в электролит вводится заведомо большее количество сернокислого стронция и кремнефтористого калия, то частично они находятся в виде осадка на дне ванны и частично - в растворе в виде ионов. По мере уноса раствора осадок растворяется и пополняет убыль аниона SO2-.
Электролит менее чувствителен к возможным колебаниям температур и плотностей тока, чем стандартный, и, следовательно, не вызывает отслаивания хрома при невольных нарушениях режима. Наконец, электролит позволяет при той же силе тока, что и в стандартном, производить осаждение хрома в 1,4—1,5 раза быстрее за счет более высокого выхода по току.
Несмотря на свои высокие достоинства, саморегулирующиеся электролиты не получили широкого применения, так как имеют весьма существенные недостатки, основным из которых является наличие агрессивного аниона F- в составе электролита. Это обстоятельство приводит к быстрому разрушению свинцовой футеровки хромовых ванн, особенно по сварочным швам. В результате, взамен рольного свинца футеровку ванн необходимо производить керамикой, винипластом, пентапластом, поливинилхлоридом и прочими материалами. По этой же причине непригодны и свинцовые аноды. Взамен им приходится применять аноды из свинцово-оловянного сплава, с содержанием олова — от 6 до 10 %.
Тетрахроматный электролит
Из электролитов, не требующих подогрева, некоторое промышленное применение получил так называемый тетрахроматный электролит, для которого рекомендуются следующий состав (г/л) и режим работы (ГОСТ 9.047):
хромовый ангидрид — 350—400; серная кислота — 2,5—3,0; едкий натр —40—60; хром трехвалентный — 10—15; температура, °С — 15—30; плотность тока, А/дм2 — 10—60; выход по току, % — 25—30.
Электролит отличается повышенной рассеивающей способностью, но хромовые покрытия имеют серый, матовый вид и в 2— 3 раза меньшую твердость, чем осадки из стандартного электролита. Поэтому хромовые покрытия из тетрахромового электролита применяют лишь в качестве защитного покрытия с использованием меди, никеля или цинка в качестве подслоя.
Для скорейшего образования трехвалентного хрома в необходимом количестве для правильной эксплуатации в представленный электролит вводят при приготовлении до 0,5-0,6 г/л сахара. Электролит менее агрессивен, чем стандартный, и в нем можно непосредственно хромировать детали из латуни, цинковых сплавов и других химически нестойких металлов. Так как электролит не требует подогрева, то в качестве поплавков для предохранения электролита от уноса в вентиляционные отсосы можно использовать кусочки дерева, пропитанные парафином. В связи с тем, что плотности тока при хромировании весьма велики, электролит может перегреваться выше допустимых температур (23-24 °С).
Электролит для реверсирования
При электроосаждении периодическое изменение направления постоянного тока существенно изменяет некоторые свойства покрытий. Одна из характерных особенностей хромирования с применением реверсирования тока - возможность получения покрытия толщиной 800 мкм и более с малыми внутренними напряжениями. Хромирование проводят при следующем составе (г/л) и режимах:
хромовый ангидрида - 200-250; серная кислота - 2-2,5; температура электролита, °С - 50-60; катодная плотность тока, А/дм2 - 120 длительность катодного периода, мин - 1-5; длительность анодного периода, с - 5-25.
Реверсирование позволяет ускорить процесс осаждения хрома в 1,5-2 раза по сравнению с обычными электролитами.
При покрытии деталей хромом в проточном электролите при тех же плотностях тока возможно получить осадок высокого качества и значительной толщины. Процесс нанесения покрытия при этом ускоряется в 6-10 раз по сравнению с обычным хромированием. С увеличением скорости протекания электролита от 0 до 200 см/с микротвердость осажденного металла повышается от 7000 до 10000 МПа при ведении процесса с плотностью тока 45 А/дм2 и температуре электролита 45 °С. Равномерность осаждения и износостойкость хрома при наращивании в проточном электролите выше, чем при хромировании в непроточном электролите. Особенно эффективно применение проточного электролита для наращивания внутренних поверхностей деталей.
К типу многослойных покрытий может быть отнесено так называемое двухслойное хромовое покрытие. Последнее получают при нанесении различных осадков хрома с изменяющимися свойствами. Если необходимо защитить деталь от коррозии при одновременном увеличении ее износостойкости, наносят два слоя хрома: нижний - беспористый молочный и верхний - блестящий.
Таблица 5.2. Скорость наращивания хрома, мкм/ч.
|
Плотность тока, А/дм2 |
Катодный выход по току, % |
|||
|
12 |
14 |
16 |
18 |
|
|
20 |
11,6 |
13,5 |
15,5 |
17,5 |
|
40 |
23,2 |
27,0 |
31,0 |
35,0 |
|
60 |
34,9 |
40,6 |
46,5 |
52,5 |
|
80 |
46,5 |
54,2 |
62,0 |
70,0 |
|
100 |
58,1 |
67,7 |
77,3 |
86,9 |
Слой молочного хрома толщиной 15 мкм осаждают при температуре 70 °С и плотности тока 30 А/дм2. Затем непромытая деталь переносится в ванну с более низкой температурой электролита, где на матовый слой наносится слой блестящего износостойкого хрома толщиной 35 мкм и более. Температура электролита - 50 °С, плотность тока - 50 А/дм2. Хромирование производят в двух ваннах с электролитом одинакового состава (250 г/л хромового ангидрида и 1-5 г/л серной кислоты).
Скорость наращивания хрома ориентировочно можно определить по данным табл. 5.2.
Возможно Вас так же заинтересуют следующие статьи: comments powered by HyperCommentsecm-zink.ru
Хромирование
 Электролитическое хромирование в практических целях осуществляется исключительно из растворов электролитов на основе шестивалентной окиси хрома. Многочисленные попытки создать промышленно полезный электролит на основе соединений трехвалентного хрома, позволяющий получать хромовые покрытия, обладающие такими же технико-эксплуатационными свойствами, особенно для получения толстослойных твердых износостойких покрытий, не привели к положительным результатам.
Электролитическое хромирование в практических целях осуществляется исключительно из растворов электролитов на основе шестивалентной окиси хрома. Многочисленные попытки создать промышленно полезный электролит на основе соединений трехвалентного хрома, позволяющий получать хромовые покрытия, обладающие такими же технико-эксплуатационными свойствами, особенно для получения толстослойных твердых износостойких покрытий, не привели к положительным результатам.
Все электролиты хромирования содержат свободные кислотные радикалы, которые, действуя как не расходуемые катализаторы, способствуют осаждению хрома на катоде. Помимо этого, во всех электролитах хромирования на основе шестивалентного хрома обязательно присутствуют и ионы трехвалентного хрома. Допустимое содержание ионов трехвалентного хрома для каждого электролита хромирования, как правило, определяется в соответствии с технологическими особенностями процесса и требованиями, предъявляемыми к качеству и функциональным характеристикам хромового покрытия (блеску, твердости, износостойкости и др.). Вместе с тем, обычно рекомендуется поддерживать концентрацию трехвалентного хрома в электролите хромирования в интервале 3-5 г/л.
Электролитическое хромирование, проводимое на основе шестивалентных солей хрома, является высокотоксичным процессом, а используемые для этого электролиты являются агрессивными жидкостями, даже в разбавленных растворах. К тому же, во время электроосаждения хрома происходит усиленное газообразование и в воздух вместе с газом, в виде аэрозоля, поступает большое количество агрессивных веществ. Поэтому при работе с электролитами хромирования должны строго соблюдаться правила техники безопасности и приняты все необходимые меры предосторожности, а используемые ванны хромирования обязательно должны быть снабжены мощными отсасывающими устройствами и вентиляционными установками, очищающими воздух от вредных аэрозольных примесей.
В зависимости от условий проведения процесса электролиза различают три типа хромовых покрытий встречающихся на практике: это блестящие защитно-декоративные покрытия, отличающиеся небольшой толщиной покрытия и позволяющие получать блестящие осадки хрома, затем твердые износостойкие защитные покрытия, позволяющие получать хромовые покрытия большой толщины, с высокими значениями твердости и износостойкости, и молочные безпористые покрытия, использующиеся в основном как подслой, для улучшения коррозионной стойкости покрытий. По функциональному назначению хромовые покрытия можно разделить на защитно-декоративные, износостойкие и молочные. В данной статье мы коснемся только блестящих защитно-декоративных и молочных износостойких хромовых покрытий.
Блестящие защитно-декоративные хромовые покрытия имеют небольшую толщину, в пределах 0,2 - 0,7 мкм, наносятся обычно по подслою меди и никеля, и используются для повышения механической и коррозионной стойкости покрытия, для придания поверхности изделия улучшенных декоративных свойств. Молочные защитные хромовые покрытия осаждают на сталь, алюминий, титан и некоторые другие металлы и сплавы. Получаемые покрытия имеют большую толщину, порядка 10-100 мкм и используются для защиты рабочего инструмента, оптической аппаратуры, для покрытия валов полиграфических машин, турбинных лопаток и т.д.
Электролиты хромирования обладают самой низкой рассеивающей способностью из всех известных на сегодня электролитов. Осаждение хрома и нанесение хромового покрытия требует очень высокой токовой нагрузки в ванне, значительно более высокой, чем в других процессах гальваноосаждения. Это в свою очередь определяет выбор источника тока для хромирования или силового преобразователя, также значительно более мощного, чем для других процессов гальваноосаждения.
 Для процесса блестящего декоративного хромирования в основном используют электролиты, содержащую высокую концентрацию хромового ангидрида. К преимуществам такихэлектролитов относится их более высокая электропроводность, а следовательно, возможность проводить осаждение хрома при пониженных плотностях тока, а также меньшая чувствительность к загрязнениям, по сравнению с разбавленными электролитами, используемыми для молочного хромирования. К недостаткам концентрированных электролитов можно отнести в первую очередь его «неэкологичность» (за счет более высокой концентрации ионов шестивалентного хрома, большее количество токсичных соединений хрома, которые выносятся в сточные воды, большие проблем с очисткой сточных вод и т.д.). Преимуществами разбавленных электролитов, используемых для матового хромирования являются прежде всего, меньшие затраты для очистки сточных вод, меньшие затраты для обезвреживания отработанных электролитов, а также более высокий выход по току. Помимо этого, в разбавленных электролитах процесс хромирования проводится при значительно более высокой силе тока (до 150 А/дм2), что позволяет повысить скорость осаждения и уменьшить продолжительность процесса хромирования. К недостаткам разбавленных электролитов относится их низкая электропроводность, для чего необходимо использовать более высоковольтные, чем обычно, источники тока, что соответственно ведет к большему расходу электроэнергии.
Для процесса блестящего декоративного хромирования в основном используют электролиты, содержащую высокую концентрацию хромового ангидрида. К преимуществам такихэлектролитов относится их более высокая электропроводность, а следовательно, возможность проводить осаждение хрома при пониженных плотностях тока, а также меньшая чувствительность к загрязнениям, по сравнению с разбавленными электролитами, используемыми для молочного хромирования. К недостаткам концентрированных электролитов можно отнести в первую очередь его «неэкологичность» (за счет более высокой концентрации ионов шестивалентного хрома, большее количество токсичных соединений хрома, которые выносятся в сточные воды, большие проблем с очисткой сточных вод и т.д.). Преимуществами разбавленных электролитов, используемых для матового хромирования являются прежде всего, меньшие затраты для очистки сточных вод, меньшие затраты для обезвреживания отработанных электролитов, а также более высокий выход по току. Помимо этого, в разбавленных электролитах процесс хромирования проводится при значительно более высокой силе тока (до 150 А/дм2), что позволяет повысить скорость осаждения и уменьшить продолжительность процесса хромирования. К недостаткам разбавленных электролитов относится их низкая электропроводность, для чего необходимо использовать более высоковольтные, чем обычно, источники тока, что соответственно ведет к большему расходу электроэнергии.
Блестящие защитно-декоративные хромовые покрытия не рекомендуется осаждать непосредственно на медную, латунную или бронзовую основу, или подслой из этих металлов, или сплавов. Связано это с тем, что при эксплуатации в атмосферных условиях медь взаимодействует с атмосферными газами с образованием углекислой и других солей меди. Образующиеся соли, скапливаясь в порах, резко ухудшают внешний вид хромового покрытия. В случаях, когда хром необходимо осаждать непосредственно на детали из меди, латуни или бронзы, толщина хромового покрытия должна быть не менее 4-5 мкм. Трехслойное декоративное хромовое покрытие, в связке Cu-Ni-Cr (медь-никель-хром) обладает достаточно высокими защитными и антикоррозионными свойствами. Первый тонкий медный подслой обеспечивает прочность сцепления покрытия с основой. Второй, толстый слой меди, повышает коррозионную стойкость и защитную способность покрытия, и позволяет уменьшить толщину осадка дорогостоящего никеля, при этом сохранить необходимые коррозионные свойства всего покрытия. При этом важно, чтобы, помимо выравнивающих добавок в электролит меднения входили также эффективные блескообразующие добавки, позволяющие получать не только гладкие, но и блестящие осадки меди. На такой блестящий слой меди и осаждают блестящее никелевое покрытие из электролитов никелирования, также содержащих блескообразующие и выравнивающие добавки. Важная роль в защитно-декоративных свойствах покрытия Cu-Ni-Cr принадлежит последнему слою блестящего хрома. Так как в отличие от никеля, который со временем пассивируется и имеет желтоватый оттенок, блестящий хром не тускнеет и имеет красивый голубоватый оттенок, а само хромовое покрытие обладает более лучшими декоративными свойствами. Помимо этого, в западных странах никель вообще запрещено использовать как конечное декоративное покрытие, если с ним возможен прямой контакт человека, так, как было обнаружено, что никель является сильным аллергеном.
Самыми распространенными электролитами хромирования являются электролиты, состоящие из окиси хрома и серной кислоты. Они бывают разбавленные, стандартные и концентрированные.
| 1 | 130-175 | 1,3 - 1,75 h3SO4 | 40-70 | 15-105 | 16-18 |
| 2 | 220-250 | 2,2 - 2,5 h3SO4 | 40-70 | 15-105 | 12-14 |
| 3 | 275-300 | 2,75 - 3,0 h3SO4 | 40-70 | 15-105 | 8-10 |
У разбавленных электролитов наилучшая рассеивающая способность, но электролит не очень устойчив по составу, а хромированные осадки склонны к шероховатости. Наиболее часто используется стандартный электролит хромирования, т.к. имеет более широкий диапазон плотностей тока, а колебания по составу не значительны. Концентрированный электролит хромирования имеет самую низкую рассеивающую способность, а осадки отличаются наименьшей твердостью, но имеют высокую декоративность.
 В некоторых случаях в электролит добавляют катионы цинка. Такие электролиты используются для нанесения износостойких покрытий на деталях, работающих в условиях воздействия сред повышенной агрессивности. Для повышения рассеивающей способности электролита и улучшения физико-химических свойств хромовых покрытий, в электролит вводятся органические добавки. Недостатком органических веществ является их взаимодействие с хромовой кислотой, что приводит уже в начале процесса электролиза к накоплению излишнего количества трехвалентного хрома в электролите.
В некоторых случаях в электролит добавляют катионы цинка. Такие электролиты используются для нанесения износостойких покрытий на деталях, работающих в условиях воздействия сред повышенной агрессивности. Для повышения рассеивающей способности электролита и улучшения физико-химических свойств хромовых покрытий, в электролит вводятся органические добавки. Недостатком органических веществ является их взаимодействие с хромовой кислотой, что приводит уже в начале процесса электролиза к накоплению излишнего количества трехвалентного хрома в электролите.
Во всех технических электролитах, содержащих хромовую кислоту, для обеспечения стабильности процесса хромирования, важно поддерживать правильное соотношение между концентрациями хромовой кислоты и каталитической добавкой. Величину отношения концентрации хромовой кислоты к полной концентрации каталитических кислотных радикалов, необходимо поддерживать в пределах от 50:1 до 200:1, но лучше всего подходить пропорция 100:1 (концентрации здесь выражены в граммах СrО3, Н2SO4).
 Процесс осаждения хрома и свойства получаемого хромового покрытия во многом зависят от режима осаждения хрома, т. е. от катодной плотности тока и температуры электролита. Наиболее ясное представление о примерных граница х режимов электролиза, обеспечивающих получение серого, блестящего и молочного осадков хрома, дает диаграмма плотности тока и температуры (DK—t), изображенная на рисунке 1.
Процесс осаждения хрома и свойства получаемого хромового покрытия во многом зависят от режима осаждения хрома, т. е. от катодной плотности тока и температуры электролита. Наиболее ясное представление о примерных граница х режимов электролиза, обеспечивающих получение серого, блестящего и молочного осадков хрома, дает диаграмма плотности тока и температуры (DK—t), изображенная на рисунке 1.
Серый осадок хрома появляется на катоде при низких температурах электролиза (35...50°С) и широком диапазоне плотностей тока. Осадки блестящего хрома обладают высокой твердостью (6000... 9000 Н/мм2), высокой износостойкостью и имеют меньшую хрупкость.
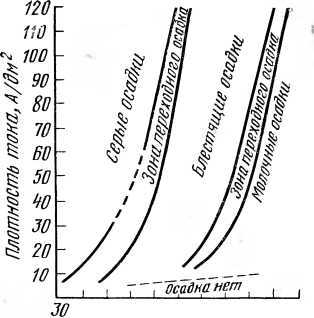 Рис. 1. Зоны хромовых осадков.
Рис. 1. Зоны хромовых осадков.
Молочный хром получается при более высокой температуре электролита (выше 70°С) и более широком широком интервале плотностей тока. Молочные осадки отличаются пониженной твердостью (4400.. 6000 Н/мм2), но обладают пластичностью и имеют повышенную коррозионную стойкость.
Сверхсульфатный электролит хромирования
Сверхсульфатный электролит хромирования рекомендуется для скоростного осаждения толстослойных, блестящих и износостойких хромовых покрытий (до 500 мкм).
Состав сверхсульфатного электролита хромирования, г/л:
Хромовый ангидрид (CrO3) 250-300 г/л
Серная кислота (h3SO4) 8-10 г/л
Хром трехвалентный (в пересчете на Сг203) 20-22.
Температура электролита должна быть не ниже 500С, а плотность тока во время процесса хромирования более 55 А/дм2. Из сверхсульфатного электролита в широком интервале температур и плотностей тока (до 300 А/дм2) осаждаются износостойкие, твердые хромовые покрытия.
Рекомендуемые режимы электролиза:
Сверхсульфатный электролит хромирования имеет крайне низкую рассеивающую способность. Поэтому он рекомендуется только для нанесения хромовых покрытий на цилиндрические детали: штоки, валы, цилиндры и т.д., при использовании специальной оснастки, обеспечивающей концентрическое (коаксиальное) расположение детали и анода. Рекомендуемый состав анодов: РЬ 7986%; Sb 4-6%; Sn 10-15%
Саморегулирующийся сульфатный электролит хромирования
Саморегулирующийся сульфатный электролит подобен стандартному электролиту хромирования, т.к. в его состав входит только один анион катализатор - сульфат. Различие заключается лишь в том, что сульфаты вводятся в электролит не в виде серной кислоты, а в виде трудно растворимой соли - сульфата стронция. Содержание сульфатов в электролите регулируется благодаря ограниченной растворимости этой соли. Состав саморегулирующегося сульфатного электролита хромирования, г/л:
Хромовый ангидрид (Сг03) 250;
Сернокислый стронций (SrS04) 6-8;
Двуокись кремния (SiO;) 10-15.
Режим работы электролита:
Блестящие твердые покрытия: Плотность тока 60-95 А/дм2. Температура 60-650С.
Молочные толстослойные покрытия: Плотность тока 20-50 А/дм2.Температура 78-800С.
Саморегулирующийся сульфатно-кремнефторидный электролит хромирования
В саморегулирующемся сульфатно-кремнефторидномэлектролите анионами-катализаторами являются ионы S042- и SiF62-. Основные преимущества данного электролита по сравнению с сульфатным электролитом, заключается в большей стабильности состава, несколько более высокой рассеивающей способности, более высоком выходе по току и более широкому интервалу допустимых температур, и плотностей тока, обеспечивающих получение блестящих осадков хрома. При использовании данного электролита легче решается проблема получения прочного сцепления хрома с блестящим никелевым покрытием, нержавеющей сталью. Объясняется это тем, что фторсодержащие электролиты обладают значительно большей активирующей способностью, чем электролиты без фтора. Процесс хромирования в этих электролитах менее чувствителен к перерывам тока.
Главным недостатком саморегулирующихся кремнефторидных электролитов хромирования является их повышенная агрессивность по сравнению со стандартными электролитами, особенно по отношению к медным сплавам, стали и к свинцовым анодам. Скорость растворения металлов в саморегулирующемся электролите хромирования, а следовательно, и скорость накопления в нем ионов железа или меди выше, чем в сернокислом. При плохой рассеивающей способности электролита участки хромируемых деталей, на которых реализуется более низкая плотность тока, более медленно покрываются хромом и подвергаются, с одной стороны, травлению электролитом, а с другой - сильному наводораживанию.
Состав саморегулирующего сульфатно-кремнефторидного электролита, г/л:
хромовый ангидрид (CrO3) — 250--300:
сернокислый стронций (SrSO4)— 5,5 -6,5
кремнефтористый калий (K2SiF6) — 18- 20
Тетрахроматный электролит хромирования
Тетрахроматный электролит имеет довольно необычный для электролитов хромирования состав - наряду с хромовой и серной кислотами он содержит достаточно большое количество щелочи, которая частично нейтрализует кислоту. Несмотря на это, при электроосаждении хрома из тетрахроматного электролита сохраняются все особенности процесса, характерные для остальных электролитов хромирования. К особенностям тетрахроматного электролита относится то, что он обладает более высокой, чем у всех остальных электролитов хромирования, рассеивающей способностью. Достоинством этого электролита хромирования является то, что хром из него осаждается при комнатной температуре (18-25оС) с высоким выходом по току. При повышении температуры тетрахромат распадается и электролит теряет свои специфические свойства. Поэтому в процессе работы очень важно постоянно контролировать и поддерживать низкую температуру, при необходимости охлаждая раствор электролита.
К электролитам тетрахроматного типа относятся и электролиты, в которых вместо щелочи используют углекислый кальций. В некоторых случаях рекомендуется добавлять в электролит 0.5-10 г/л вольфраматов или солей магния, в присутствии которых осаждаются хромовые покрытия, обладающие лучшей полируемостью.
Состав тетрахроматного электролита хромирования, г/л:
Хромовый ангидрид (СrO3) -350-400
Едкий натр (NaOH) - 40-60
Серная кислота (h3SO4) - 2.5-2.7
Хром трехвалентный (на Cr2O3) - 10-15
Температура электролита -18-250С. Плотность тока -10-80 А/дм2
Тетрахроматный электролит используется исключительно для получения защитно-декоративных покрытий. Ввиду того, что электролиз ведется при комнатной температуре, осадки получаются серыми. Однако, благодаря низкой твердости и достаточно высокой пластичности, они могут быть отполированы до зеркального блеска, характерного для блестящих декоративных хромовых покрытий. Относительно высокая рассеивающая способность тетрахроматного электролита позволяет применять его для нанесения хромовых покрытий на пресс-формы, используемыех, например, для изготовления деталей из пластмасс.
Хромовые покрытия, полученные из тетрахроматного электролита, имеют значительно более низкую пористость по сравнению с хромом из сульфатных электролитов, но для получения износостойких покрытий тетрахроматные электролиты не используются. Хромовые покрытия из тетрахроматного электролита толщиной 5-10 мкм можно применять для местной защиты поверхности стальных деталей, при газовой цементации или нитроцементации.
Электролиты черного хромирования
Черное хромирование применяется для покрытия оптических систем и деталей, которые должны иметь хорошую теплоотдачу в пространство. Толщина слоя черного хрома составляет 1,5-2,0 мкм. Покрытие черного хромирования обладает хорошей термостойкостью, и в отличии черного никеля или черных оксидных покрытий, являются износостойкими.
| Хромовый ангидрид | 250 | 200 | 250-400 | 250 | 150-400 | 250 | 250 | 200 400 |
| Уксусная кислота | - | 6.5 | 5 | - | _ | 3 | . | |
| Ванадат аммония | - | 20 | - | - | _ | _ | ||
| Оксалат железа | - | - | - | - | 15-75 | - | - | - |
| Карбамид | 2.5 | |||||||
| Фторид хрома | ||||||||
| Борная кислота | - | - | - | - | 15 | _ | ||
| Нитрат натрия | 3-5 | - | - | 5 | _ | |||
| Гексафторалюминат натрия | 0.2 | - | - | - | 0.1 | - | - | - |
| Плавиковая кислота | - | - | - | - | - | - | 0.21 | |
| Кремнефторис товодородная кислота | - | - | - | 1.25 | - | - | - | |
| Хромин | 2-3 | - | - | 1.53 | - | - | - | |
| Температура,°С | 18-25 | 10-30 | 10-30 | 18-25 | 18-25 | 15-25 | 60-70 | 18-40 |
| Плотность тока, А/дм2 | 15-30 | 50-100 | 50-100 | 10-60 | 10-50 | 10-50 | 20-30 | 50-120 |
Продолжительность процесса черного хромирования составляет 4-6 минут.
Примеси в электролите хромирования.
Присутствие в электролитах хромирования посторонних примесей может приводить к ухудшению качества хромового покрытия. Причиной появления примесей часто является нарушение самой технологии хромирования. Следует подчеркнуть, что наименьшее накопление вредных примесей происходит в электролитах, используемых для блестящего декоративного хромирования. Это объясняется тем, что из-за недолгой продолжительности процесса блестящего хромирования, подвески с деталями постоянно выносят на своей поверхности электролит с примесями. А необходимость регулярно доливать или воду, или свежую порцию электролита, приводит к разбавлению раствора электролита и предотвращает накопление в нем примесей в опасных концентрациях.
Осаждение хрома на алюминий и его сплав
Хром осаждают на детали из алюминия или его сплавов в основном в тех случаях, когда необходимо повысить их износостойкость, термостойкость или улучшить антифрикционные свойства. Непосредственное хромирование алюминия и его сплавов невозможно, что объясняется наличием на поверхности алюминия инертной оксидной пленкой прочно сцепленной с основой. Эта пленка повышает антикоррозионные свойства алюминиевой поверхности, но одновременно препятствует получению необходимого сцепления с ней хромовых и любых других гальванических покрытий. Если удалить эту пленку и опустить алюминий в раствор соли, какого-либо металла, то из-за высокого электроотрицательного потенциала алюминия на его поверхности будут контактно выделяться содержащиеся в растворе более электроположительные металлы, например медь, никель, хром, олово, или кадмий и т.п. А как известно, контактное осаждение не позволяет получать удовлетворительное сцепление покрытия с основой. Поэтому, как и в случае с титаном, для электроосажления на алюминий применяются специальные технологии.
В промышленности применяются две их разновидности:
- Активация (удаление оксидной пленки с одновременным легким подтравливанием) поверхности алюминия и одновременное осаждение на его поверхности прочно сцепленного с основой тонкого слоя металла, служащего в качестве подслоя для последующего нанесения слоя покрытия;
- Анодное оксидирование алюминия с целью формирования на нем оксидной пленки определенной структуры и толщины, которые обеспечивают надежное сцепление с ней последующего покрытия.
«Цинкатная»щелочная обработка заключается в обработке алюминиевых изделий в растворе цинката, содержащего раствор щелочи и оксида цинка. Процесс осуществляется, путем опускания алюминиевой детали на несколько секунд в раствор цинката при температуре 18-25°С. При этом имеющаяся оксидная пленка вытравливается с поверхности алюминия и, одновременно на ее месте формируется тонкий слой цинка. В принципе уже на этот слой можно наносить хромовое покрытие. Однако для улучшения сцепления рекомендуют первый слой цинка удалять, растворяя его в растворе азотной кислоте (300-500 г/л). Затем, после тщательной промывки, детали опять погружают в цинкатный раствор на 10-15 сек. Такой метод называется «двойной цинкатной обработкой» или «двойным цинкатом». Для получения более плотных, компактных с лучшими антикоррозионными свойствами пленок, рекомендуют добавлять в цинкатный раствор хлорид железа и сегнетову соль.
impgold.ru
Электролитическое хромирование - Справочник химика 21
Широко применяется электролитическое хромирование для защиты от коррозии и с целью декоративной отделки поверхности изделий. Так как хромовое покрытие трудно полируется, то процесс хромирования в этом случае ведут в условиях, обеспечивающих получение блестящих осадков небольшой толщины (0,5— [c.414]Восстановление изношенных шеек вала в зависимости от степени износа осуществляется следующими способами до 0,3 мм — электролитическим хромированием от 1,5 до 2,0 мм —электролитическим железнением от 2,0 до 3,0 мм — автоматической вибродуговой наплавкой от 3,0 до 4,0 мм —ручной газовой наплавкой свыше 4,0 мм — ручной электродуговой наплавкой. [c.242]
Опыт 5. Электролитическое хромирование [c.146]
Большинство применяемых в технике металлов и сплавов могут быть подвергнуты электролитическому хромированию. Исключение составляют стали, содержащие большое количество вольфрама, кобальта, и чугун с большим содержанием углерода и кремния. [c.115]
Восстановление электролитическим хромированием, шлифовка Электрическое железнение, шлифовка Вибродуговая наплавка, шлифовка [c.213]
Отношение к перенапряжению — двойственное. С одной стороны, перенапряжение приводит к повышенному расходу электроэнергии, с другой стороны, благодаря перенапряжению удается осаждать из водных растворов многие металлы, которые-но значениям их стандартных электродных потенциалов осаждаться не должны. Это Ре, РЬ, 5п, N1, Со, 2п, Сг. Именно благодаря перенапряжению, а также влиянию концентрации раствора на электродный потенциал возможны электролитическое хромирование и никелирование железных изделий, а на ртутном электроде удается получить из водного раствора даже натрий. [c.361]
Как видно из таблицы, при электролитическом хромировании содержание водорода в покрытии (18,9 10 %) на порядок выше, чем в стапи (1,6 10 %), т.е. практически водород адсорбируется преимущественно покрытием. Для основного металла характерно заметное уменьщение содержания водорода после термообработки при 473 К в течение 3 ч. Увеличение продолжительности термообработки приводит к росту градиента концентрации водорода вблизи границы сталь — хром. В сероводородсодержащей среде разряд водорода протекает на катодном хромовом покрытии, которое не препятствует диффузии водорода в сталь. [c.65]
Высокая устойчивость свинца в растворах серной и хромовой кислот и их солей определяет область применения свинцовых покрытий для защиты оборудования и деталей из черных и цветных металлов в химической промышленности, в производстве свинцовых аккумуляторов. Электролитический свинец применяют для покрытия подводных и подземных кабелей, деталей железнодорожных конструкций в качестве антикоррозионной защиты. Медные и стальные стержни, покрытые слоем электролитического свинца значительной толшины, используют в качестве внутренних нерастворимых анодов при электролитическом хромировании. Свинец находит применение и для специальных целей, например, при защите от рентгеновского излучения, для придания поверхности антифрикционных и сверхпроводящих свойств. [c.296]
Применяемый в настоящее время эмпирический метод борьбы с явлениями схватывания - и разрушения поверхностей трения главных шатунов и пальцев прицепных шатунов путем электролитического хромирования поверхностей трения главных шатунов и омеднения поверхностей втулок главных шатунов и пальцев прицепных шатунов совершенно себя не оправдывает. [c.112]
Электролитическое хромирование без подслоя меди и никеля применяется для повышения поверхностной твердости и износостойкости при механическом, коррозионно-механическом и абразивном видах изнашивания металлов и для восстановления размеров деталей. [c.112]
Такая.реакция протекает, например, при электролитическом хромировании, когда применение растворимых анодов невозможно-. В этом случае убыль хрома в электролите компенсируется добавлением в раствор соединений этого металла. [c.212]
Электролитическое хромирование значительно повышает сопротивление срезу, причем в случае гладкого хромового покрытия сопротивление срезу больше, чем в случае пористого покрытия. Чем больше толщина слоя хрома, тем больше сопротивление срезу (и тем меньше предел выносливости) [638]. В. Котон [639] обнаружил понижение долговечности при статической усталости надрезанных образцов из пяти авиационных сталей. [c.269]
Никелевые и хромовые гальванические покрытия являются одновременно защитно-декоративными и покрытиями, повышающими поверхностную твердость металла и его стойкость к износу. К защитно-декоративным покрытиям относятся также гальванические покрытия серебром, золотом, кобальтом бронзами, латунями и другими металлами. Для восстановления размеров деталей применяют электролитическое хромирование, железнение и меднение. . - [c.134]
Металлизованный слой довольно хрупок и для тяжело нагруженных валов металлизация не применяется. При небольших изно-сах поверхность вала может быть восстановлена электролитическим хромированием. [c.22]
Предел выносливости стали после электролитического хромирования, как показывают дан[н>1е табл. 25, заметно понижается. Из Г2 серий образцов, которые подвергались хромированию, только одна серия образцов не показала снижения усталостной прочности после хромирования. Снижение предела выносливости в остальных 11 сериях [c.108]
Усталостная прочност]> хромированной стали существенно зависит от технологического режима процесса электролитического хромирования 52]. На фиг. 83 приведены кривые усталости, полученные при испыгании трех серий образцов из стали 4-5, хромированных при различных плотностях тока. [c.109]
Так как хром отличается исключительной твердостью и большой устойчивостью к химическим воздействиям, он используется для защитных покрытий металлических изделий (хромирование). Для этого хром электролитически осаждают из растворов его солей на поверхности других металлов. Электролитическое хромирование (т. е. покрытие сАоем хрома металлических изделий) сейчас широко применяется в автомобилестроении, в производстве медицинских инструментов, корпусов часов и т. п. [c.321]
Очень велики перенапряжения при выделении водорода и кислорода. Водород на катоде выделяется при потенциале гораздо более отрицательном, чем равновесный потенциал, отвечающий pH данного раствора. Это делает возможным при электролизе водных растворов разряд ионов тех металлов (N1, Сс1, Сг, 2п и др. вплоть до Мп), потенциалы которых окажутся в соответствующих условиях белее высокими, чем потенциал водородного электрода. Благодаря этому получили широкое распростра-ненпе методы электроосаждения металлов, например электролитическое хромирование, цинкование, кадмирование, никелирование, лужение. [c.259]
Проведенные нами исследования показали, что твердое электролитическое хромирование в стандартной хромовой ванне (250 г/л хромового ангидрида и 2,5 г/л серной кислоты) при температуре 60°С и катодной плотности тока 35 А/дм при толщине слоя около 0,1 мм снижает предел выносливости стали 45 на 25-30 %. В среде 3 %-ного раствора Na I условный предел коррозионной выносливости хромированной и нехромированной стали оказался примерно одинаковым. [c.181]
Аналогичным образом при электрохимическом фторировании алкан-сульфофторидов получают перфторал-кансульфофториды и перфторалкан-сульфокислоты. Последние являются сильнейшими поверхностно-активными веществами, сохраняющими свои свойства даже в среде хромового ангидрида. Использование этих продуктов в виде препарата Хромпротект на порядок снижает унос хромового ангидрида из ванн при электролитическом хромировании. [c.380]
Перед выполнением работы необходимо ознакомиться 1) с электролитическим хромированием и назначением хромовых покрытий 2) с требованиями, предъявляемыми к хромовым покрытиям в зависимости от их назначения 3) с влиянием концентрации 504 , Сг + и Ре + в электролите для хромирования на качество хромовых лакрытий 4) с взаимосвязью при хромировании между концентрацией основных комлонентов электролита, плотностью тока, температурой и качеством пок рытий 5) с методами испытания хромовых 1П01крытий. [c.133]
В конце рассказа о металлах упомянем о хроме, который часто добавляют в сплавы алюминия для улучшения их качества. Хром широко используют для электролитического хромирования основного металла нашего века — железа, тем самыл защищая его от коррозии. Хром был открыт французским химиком Луи Вокленом в 1797 г. при [c.205]
Для получения гальванических покрытий широкое распространение 1 практике нашли процессы хромирования, никелирования, меднения, цинкования, кадмирования и др. Покрытия эти чаще всего применяются для защиты от коррозии, ио иногда и для придания изделиям декоративного вида. Кроме того, электролитическое хромирование и отчасти злектролитическое никелерование широко применяются лля повышения износостойкости трущихся деталей. [c.100]
Электролитическое хромирование образцов произволилось в ванне с электролитом трех составов (таб.ч. 23). [c.104]
Г- езу.тьтаты испытаний хромированных образцов на растяжение и ударную вязкость представлены в габл. 24. В этой же таблице указаны числа твердости для образцов, прошедших электролитическое хромирование по различным режимам. Ис11Ь тания на твердость были произведены на приборе Виккерса с нагрузкой 5 кг. а измере1шя микротвердости на приборе системы Хрушева и Берковича при нагрузке 100 кг. [c.105]
Пределы пропорциональности и текучести определялись по диаграм-ной записи на ист тательной матине ЦНИИТМАШ типа ИМ-4Р. Как показывают данные табл. 24, электролитическое хромирование практически не изменяет характеристик статической прочности стали. [c.107]
Все шесть серий образцов были захромированы на одну толщину слоя, равную 0,05 мм. После электролитического хромирования образцы подвергались отпуску при температуре 200 300 450 550 и 650°. [c.109]
chem21.info
Химическая металлизация в домашних условиях
Покрытие деталей слоем металла осуществляется по разным методикам и в различных целях. Соответственно, отличаются и технологии работы. Химическая металлизация не является в исполнении сложной, поэтому и применяется более широко, особенно в домашних условиях. О том, в чем смысл данного способа, какие понадобятся реагенты и оборудование, что следует учитывать – со всем этим предметно и разберемся.
Занимаясь самостоятельной обработкой металлических образцов в быту, ориентируются, как правило, на их внешний вид, который они приобретут в результате технологической операции. Именно поэтому, когда говорят о металлизации химической в домашних условиях, априори подразумевается, что это хромирование. Вот на нем и будет сделан акцент. Именно методика покрытия тонким слоем Cr различных деталей (в основном, колесных дисков) интересует большинство автовладельцев.

Автор обращает внимание, что простота химической металлизации, что бы ни утверждалось в статьях данной тематики – кажущаяся. На практике домашнему мастеру придется столкнуться с рядом проблем. Что это за «подводные камни», можно ли их преодолеть – разберемся сначала с этим.
Особенности химической металлизации в домашних условиях
- Деталь, подвергающаяся обработке, помещается в резервуар (ванну). Вывод №1 – хромирование имеет ограничение, связанное с габаритами образца. Если емкость для тех же дисков подобрать еще можно, то металлизацию на дому, к примеру, бампера легкового авто, произвести вряд ли получится.
- В процессе работы происходит интенсивное выделение токсичных испарений. Заниматься металлизацией не рекомендуется даже на открытом воздухе, так как невозможно предугадать, когда и как изменится ветер. А если его нет вообще, полный штиль? Вывод №2 – планируя делать хромирование чего-либо в домашних условиях, необходимо позаботиться о выборе помещения, причем организовать там вентиляцию принудительную, так как естественной будет явно недостаточно.
- После завершения процесса химической металлизации остается электролит. Жидкость достаточно агрессивная. Куда ее девать? Вывод №3 – необходимо заранее определиться с утилизацией отходов производства.
 Исходя из вышесказанного, читателя, который рассчитывает проводить хромировку где-нибудь на кухне, придется разочаровать. Словосочетание «в домашних условиях» не следует понимать буквально. Подразумевается, что металлизация делается не на производстве, на специальном оборудовании, а своими силами, с помощью простейших реагентов и принадлежностей.
Исходя из вышесказанного, читателя, который рассчитывает проводить хромировку где-нибудь на кухне, придется разочаровать. Словосочетание «в домашних условиях» не следует понимать буквально. Подразумевается, что металлизация делается не на производстве, на специальном оборудовании, а своими силами, с помощью простейших реагентов и принадлежностей.
Поэтому придется переместиться в гараж, сарай или еще куда, предварительно подготовив рабочее место. Как вариант – балкон или открытая лоджия, но только при условии, что предполагается покрытие хромом сравнительно небольшой заготовки, с использованием малого количества электролита.
Что понадобится для хромирования
О помещении уже сказано. Теперь об оборудовании и материалах.
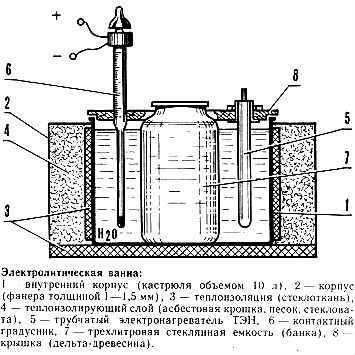
Источник постоянного напряжения
Технология металлизации предполагает использование различных электролитов и емкостей, соразмерным габаритам обрабатываемого образца. Следовательно, если речь не идет лишь о хромировании одной-единственной детали, то должна быть возможность регулировки силы тока. Простейший самодельный блок питания, использующийся в домашних условиях – трансформатор + выпрямитель + реостат.
Элементы эл/схемы
В основном это касается сечения проводов. Практика показывает, что 3-х «квадратов» при домашнем хромировании деталей вполне достаточно. Необходимо также приготовить зажимы, которыми они будут скрепляться с электродами. В продаже есть типа «крокодил». Стоимость – копеечная, а удобство работы с ними – максимальное.
Как обеспечить постоянство температуры в ванночке? Способов два. Первый и самый простой – использовать термометр, а корректировать значение силы тока вручную. Второй более сложный в реализации, так как придется устанавливать элемент автоматики – терморегулятор. Его включение в цепь избавит от необходимости контроля над процессом.
Примерное время хромирования известно, поэтому постоянное присутствие рядом с резервуаром не обязательно. Но для этого придется собирать небольшую электронную схему. Для тех, кто в этом не понимает, данный вариант неприемлем.
Ванночка
Ее материал должен быть нейтрален по отношению к жидкостям, тем более агрессивным. Поэтому лучше всего подходит стекло. Но это касается в основном малогабаритных деталей, которые смогут поместиться, скажем, в стандартной 3-литровой банке. Как вариант – емкости от промышленных аккумуляторов, с толстыми стенками. В таких любители аквариумов часто выращивают мальков. Но достать эти сосуды довольно сложно.

«Внешняя» емкость
Исходить нужно из того, что в нее будет устанавливаться выбранный стеклянный сосуд, который снаружи обкладывается утеплителем. Что можно использовать? Например, бочку, бидон, короб или ящик (даже деревянный).

Материал для теплоизоляции
Выбор большой, в зависимости от размеров емкостей – опилки, минвата, песок, стеклоткань. Задача – добиться эффекта «термоса». Поэтому необходимо изготовить крышку, которая должна полностью закрывать «внешний» резервуар. Если это ящик, то подойдет фрагмент, вырезанный из ФК, ОСВ или чего-то подобного. Нужно лишь предусмотреть гидроизоляцию крышки с внутренней стороны, если она из материала, в состав которого входит древесина. Что учесть? Из чего-бы крышка ни делалась, она не должна быть токопроводящей!
Нагревательный элемент
Чтобы упростить себе задачу, его можно приобрести. Ассортимент ТЭН достаточно большой, так что подобрать по конфигурации, размеру и мощности – не проблема.
Электроды
Могут быть пластинчатыми или стержневыми (например, из латуни, меди). В качестве «минусового» в домашних условиях обычно используется зажим, удерживающий обрабатываемый образец.

Кронштейн
Без этой «детали» не обойтись. Заготовка, которая помещается в электролит для металлизации, должна находиться в подвешенном состоянии. В противном случае та еее часть, которая будет примыкать к дну сосуда, останется необработанной. Конструкция кронштейна, способ его фиксации выбирается самостоятельно, в зависимости от условий проведения работы.
Сушильный шкаф
На последнем этапе металлизации деталь необходимо подвергнуть термообработке. Иначе не добиться характерного (и желаемого) блеска.
Порядок приготовления электролита
Методик, как и используемых реагентов, довольно много. Для хромирования в домашних условиях наиболее распространенный вариант электролита – на основе серной кислоты и хромового ангидрида. Соотношение компонентов: 2,5 г h3SO4 + 250 г CrO3 на 1 л чистой воды.
- Сначала наполняется ванночка. Вода (самая лучшая – дистиллированная) заливается примерно на ½. Ее оптимальная температура 60 – 65 ºС. В таких условиях растворение соединения хрома произойдет быстрее.
- Загрузка CrO3 и тщательное перемешивание до исчезновения всех крупиц.
- Если необходимо, доливается еще определенное количество воды (до требуемого объема), далее – серная кислота.
После перемешивания полученного раствора он подвергается «проработке». Она заключается в том, что через него пропускается постоянный ток. Его сила рассчитывается из соотношения: 1л – 6,5 А. Визуально готовность электролита можно определить по его оттенку. Он должен приобрести окрас темно-коричневый. После этого раствор отстаивается в темном и прохладном месте не менее 24 часов.
Подбирая емкость по объему, нужно ориентироваться на мощность блока питания. Соответственно, и он должен выбираться, исходя из размеров деталей, подлежащих металлизации. Это еще одна причина, по которой в домашних условиях хромирование крупногабаритных образцов нецелесообразно и затруднительно.
Подготовка детали к металлизации
Пока электролит отстаивается, самое время заняться этим.
Удаление загрязнений
Чтобы хромирование было качественным и недорогим, покрывающий деталь слой должен быть однородным и тонким. Этого можно добиться, если поверхность зачищена до самой основы. Чем удалять инородные фракции и обезжиривать, решается самостоятельно. Для образцов с ровными гранями достаточно, как правило, «шкурки». В остальных случаях придется подумать, как и чем удалить грязь и ржавчину.
Обезжиривание
Это второй подготовительный этап. Ограничиваться лишь традиционными средствами – бензином, уайт-спиритом, растворителем «666» или чем-то подобным – значит, не добиться качественной металлизации. Хромировка на такой поверхности долго не продержится.
Дополнительная обработка производится в растворе, который специально готовится для этих целей. Рецептов много, но наиболее популярный при металлизации на дому следующий:
150 (едкий натр) + 50 (кальцинированная сода) + 5 (силикатный клей).
*Из расчета г/л воды.
Предварительно обработанная заготовка погружается в этот раствор, который должен быть доведен до температуры 85 (±5) ºС. Время выдержки зависит от рельефности детали и степени ее остаточного загрязнения (от ⅓ до 1,5 часов).

Особенности процесса хромирования
Схема «установки» с полярностью включения напряжения показана на рисунке (см. выше).
- Подача тока после погружения образца в электролит производится с некоторой задержкой. Почему? Качественная металлизация произойдет, только если температуры детали и раствора выровняются. Поэтому придется немного подождать. Это время можно и сократить, если образец предварительно нагреть градусов до 40 – 50. Например, перед рефлектором.
- Рекомендуемый ток в пределах 55 ºС.
- После того, как вся деталь покроется слоем хрома, без «проплешин» (определяется визуально), ее необходимо просушить в эл/шкафу (минимум 2,5 – 3 часа).
 Прежде чем закончить статью, автор с большим сожалением должен добавить пару «ложек дегтя». Тем, кого не пугают перечисленные трудности, нужно учесть и еще ряд проблем, с которыми придется столкнуться.
Прежде чем закончить статью, автор с большим сожалением должен добавить пару «ложек дегтя». Тем, кого не пугают перечисленные трудности, нужно учесть и еще ряд проблем, с которыми придется столкнуться.
Некоторые – например, обеспечение высокого качества полировки, соблюдение абсолютной точности рецептуры, сложность определения оптимальных габаритов и формы электродов, выдержка неизменного режима по току – покажутся незначительными на фоне всего лишь одной.
Где взять ангидрид и «чистую» кислоту? Первый в продаже есть, но только для юр/лиц, с оформлением соответствующих документов. Магазинная h3SO4, которую приобретают с целью приготовления электролита для АКБ, не подходит. Она недостаточно «чистая», поэтому не обеспечит качественной хромировки.
Статья получилась достаточно полной. А заняться или нет металлизацией на дому, решать только вам, уважаемый читатель.
ismith.ru
Электролитическое хромирование — курсовая работа
Монтаж подвески. Для осаждения равномерного слоя покрытия конструкция подвески должна способствовать созданию всюду одинакового анодно-катодного расстояния, а сами детали не должны прикрывать друг друга.
При загрузке партии деталей в ванну хромирования нужно, чтобы форма и размеры деталей, а подвесных приспособлений были одинаковыми. Подвески и контакты должны изготовляться из одинаковых материалов. Поверхность контактов следует тщательно очищать от коррозии и вязкого налета электролита.
Обезжиривание. Выбор способа обезжиривания определяется природой металла детали и условиями ее работы. Стальные закаленные детали, работающие при больших удельных нагрузках, не допускается обезжиривать на катоде; в этом случае применяется анодное обезжиривание или обезжиривание химическим способом.
Детали крупного размера, а также детали, отдельные части которых легко растворяются в горячих щелочных растворах, обезжириваются известковой кашицей.
Декапирование. Перед хромированием стальные и чугунные детали подвергаются анодному декапированию в хромовом электролите при температуре, соответствующей процессу хромирования.
После анодного декапирования в хромовом электролите промывка водой не проводится.
Изделия из меди и медных сплавов анодному декапированию не подвергаются. Детали с никелевым покрытием при лежании на воздухе пассивируются и плохо хромируются. Поэтому поверхность таких деталей перед хромированием следует активировать. Для этого рекомендуется кратковременная обработка в щелочи или погружение на несколько минут в концентрированную серную кислоту.
Подвешивание деталей и анодов в ванну. Неравномерность расстояния между изделиями и анодами в ванне может привести к неоднородности покрытия по толщине, к образованию так называемого пригара на одних деталях и матовых осадков на других.
При рельефном катоде и плоском аноде уменьшение расстояния между электродами ухудшает равномерность отложения хрома на поверхности детали. Увеличение расстояния повышает равномерность покрытия, но при этом одновременно возрастает напряжение на ванне.
Завешенные в ванну детали должны находиться в вертикальном положении. При хромировании крупногабаритных деталей возникает необходимость в горизонтальном погружении их в электролит, причем деталь в процессе электролиза должна вращаться.
Электролиз. Хромируемые детали к началу электролиза должны быть прогреты до температуры электролита. Изделия прогревают 3-5 мин, что предупреждает матовых осадков и уменьшает величину внутренних напряжений в осажденном слое хрома. Стальные и чугунные детали прогреваются в хромовой ванне. Медь химически растворяется в хромовой кислоте, поэтому изделия из меди и медных сплавов прогреваются в горячей воде.
Перерывы тока в процессе хромирования не допускаются, так как при повторном наращивании возможно отслоение хрома. Если перерыв тока все же произошел, то перед повторным хромированием изделие подвергают анодному травлению в течение 20-40 сек, при плотности тока 25-30 а/дм2 и только после этого продолжают хромирование. Осаждение хрома следует начинать с относительно низких катодных плотностей тока (но не ниже 20-25 а/дм2), и постепенно увеличивать до установленной величины.
При хромировании рельефных деталей рекомендуется в начале электролиза произвести «толчок» тока. Этот прием состоит в том, что электролиз начинает при плотности тока примерно вдвое больше чем следует, а спустя 1-2 мин величину ее постепенно снижают до нормальной.
Скорость осаждения хрома
Применяемые при хромировании плотности тока лежат в пределах 10-100 а/дм2. Вместе с тем чаще рекомендуется применение более высоких плотностей тока (до 200 а/дм2 и выше), позволяющих интенсифицировать процесс осаждения хрома.
Таблица 4
Продолжительность осаждения слоя хрома толщиной 1 мкм из электролита, содержащего 250 г/л CrO3 и 2,5 г/л h3SO4.
| Катодная плотность тока, в а/дм2 | Время, в мин. |
| 10 | 9,8 |
| 15 | 6,5 |
| 20 | 4,9 |
| 25 | 3,9 |
| 30 | 3,3 |
| 40 | 2,5 |
| 50 | 2,0 |
| 60 | 1,6 |
| 80 | 1,2 |
| 100 | 1,0 |
При износостойком хромировании толщина слоя покрытия достигает значительной величины. Применение высоких плотностей тока, позволяющих сократить время хромирования, должно быть согласовано с температурой электролита.
В табл. 5 приведены примерные толщины хрома, осажденного из хромовокислого электролита обычного состава при различных плотностях тока и температурах электролита при длительности электролиза 1 час.
Таблица 5
Толщина хрома (в мкм), осажденного за 1 ч. из хромовокислого электролита с содержанием 250 г/л CrO3 и 2,5 г/л h3SO4.
| Плотность тока, в а/дм2 | Температура электролита, в оС | ||||||
| 25 | 35 | 40 | 45 | 50 | 55 | 65 | |
| 10 | 9 | 4,5 | 4,5 | 4,4 | 3,0 | - | - |
| 15 | 21 | 11,5 | 11 | 10 | 9 | 7 | 4,5 |
| 25 | 38 | 23,5 | 22 | 18 | 17 | 16 | - |
| 30 | 54 | 36 | 31 | 25,5 | 24 | 23,5 | 17,5 |
| 40 | - | 53 | 42 | 34 | 33 | 31 | - |
| 50 | 93 | 76 | 59 | 46 | 44 | 42 | 34 |
| 60 | - | 105 | 75 | 59 | 57 | 53 | 46 |
| 80 | - | - | 107 | 88 | 79 | 75 | 62 |
| 100 | - | - | - | - | 103 | 98 | 83 |
| 125 | - | - | - | - | 138 | 127 | 110 |
| 150 | - | - | - | - | - | - | 130 |
| 200 | - | - | - | - | - | - | 185 |
Электрохимические процессы протекают на границе электрод-электролит, в остальном объеме электролита никаких электрохимических превращений не происходит. При погружении электрода в электролит (вещество, подвергающееся в растворах или расплавах электролитической диссоциации и проводящая электрический ток за счет движения ионов) ионы, перешедшие в раствор, находятся вблизи поверхности электрода в виде двойного электрического слоя, за счет чего на границе металл-жидкость возникает разность потенциалов или просто потенциал. Двойной электрический слой подобен конденсатору, одна обмотка которого заряжена положительно, другая – отрицательно. При погружении металла (электродов) в раствор без подачи тока устанавливается равновесие, которому соответствует равновесный потенциал. При подаче в ванну тока от постороннего источника на аноде выделяется некоторое количество электронов, которые переходят в раствор, либо движутся к катоду.
Катодный процесс
Процесс хромирования в хромовокислых электролитах протекает в результате восстановления на катоде сложного многовалентного аниона при одновременном образовании соединений хрома промежуточной валентности. При этом на катоде совместно протекает несколько реакций.
В присутствии анионов пленка на катоде не разрыхляется, а наоборот уплотняется. При этом осаждение рома на катоде происходит за счет восстановления шестивалентных ионов хрома, входящих в состав самой пленки. В хромовокислых растворах с добавкой серной кислоты при заданном постоянном значении потенциала катодная плотность тока, имевшая в начальный момент относительно большую величину, через короткий промежуток времени, резко снижалась. Такое сильное торможение электрохимического процесса является результатом образования на поверхности катода плотной пленки из продуктов реакции. При выключении тока пленка растворялась, а после включения наблюдалось повторное явление. В растворах хромового ангидрида, не содержащих серной кислоты, величина начальной плотности тока выше, а снижение ее во времени менее резкое. Такое изменение плотности тока свидетельствует об уплотнении коллоидной пленки на катоде в присутствии серной кислоты. Образование пленки на катоде вызывается смещение потенциала катода в отрицательную область. Благодаря этому наряду с разрядом ионов водорода становится возможным восстановление шестивалентных соединений хрома до металла и трехвалентного хрома.
Установлено, что при относительно невысоких значениях потенциалов, при которых не происходит выделения металлического хрома с увеличением концентрации ионов SO42+ скорость Cr6+ до Cr3+ резко возрастает и определяется предельным током реакции Cr6+ → Cr3+. Эта реакция протекает наиболее легко и лишь при ее торможении в области отрицательных потенциалов создаются благоприятные условия для осуществления Cr6+ → Cr3+. Следует отметить положительное влияние пленки, образующейся на поверхности катода, которая несколько тормозит реакцию разряда ионов водорода. В вопросе о вреде или пользе пленки общим является мнение о том, что в процессе электролиза на поверхности катода образуется фазовая пленка из соединений высшей и низшей валентности хрома. На катоде происходит непосредственное восстановление шестивалентных ионов хрома до металла.
Анодный процесс
В электролитических ваннах для хромирования используются нерастворимые аноды. Растворимые аноды для хромирования не применяются. Металлический хром растворяется на аноде с выходом по току, в 7-8 раз превышающим выход по току на катоде. При этом концентрация ионов хрома в растворе непрерывно возрастает. Значительная часть хрома переходит в раствор в виде трехвалентных ионов, которые на растворимом аноде не могут быть окислены до шестивалентных.
При электролизе растворов хромовой кислоты на нерастворимом аноде протекают два процесса: выделение кислорода (4OH–→2e→O2+2h3O) и окисление трехвалентного хрома до шестивалентного. Часть кислорода, выделившегося в процессе электролиза, окисляет свинец с образованием темно-коричневой перекиси свинца. Хотя свинцовые аноды считаются нерастворимыми, все же с течением времени они разрушаются, так как перекись свинца частично отделяется от поверхности электрода и оседает на дне ванны. Одновременно с этим свинец, слабо взаимодействуя с хромовой кислотой, образует на поверхности анода твердую, плохо проводящую ток пленку хромовокислого свинца.
- Лайнер В.И. Защитные покрытия металлов., М. «Металлургия»., 1974г.
- Плетнев Д.В., Бруснецова В.Н. Основы технологии износостойких и антифрикционных покрытий., М: «Машиностроение»., 1968г.
- Непрерывные методы нанесения покрытий. Методические указания для самостоятельной работы по дисциплине «Теория и технология нанесения покрытий»., сост. Полякова М.А., Магнитогорск, 2001г.
- Твердые смазочные покрытия. Сборник статей. Отв.ред., д-р техн.наук Матвеевский Р.М., М: Наука, 1977г.
- Хейфнец Л.И. Электролиз никеля., М.: «Металлургия»., 1980г.
- Гун Г.С., Чукин М.В. и др. Упрочняющие и восстанавливающие покрытия., Магнитогорск, 1982г.
- Черкез М.Б. Хромирование., Ленинград, «Машиностроение», 1971г.
- Бахматов Ю.Ф., Голубчик Э.М. Конструирование технологий нанесения покрытий на изделия в метизной промышленности: Учеб. Пособие. – Магнитогорск: МГТУ им. Г.И.Носова, 1999. – 69с.
turboreferat.ru










