Содержание
Производство меди | Металлургический портал MetalSpace.ru
В рудах медь находится в виде сернистых соединений (CuFeS2 – халько-пирит, Cu2S – халькозин, CuS – ковелин), оксидов (CuO, CuO) и гидрокарбонатов [CuCO3·Cu(OH)2,2CuCO3·Cu(OH)2]
Пустая порода руд состоит из пирита (FeS2), кварца (SiO2), различных соединений содержащих Al2O3, MgO, CaO, и оксидов железа.
В рудах иногда содержится значительные количества других металлов (цинк, золото, серебро и другие).
Известны два способа получения меди из руд:
- гидрометаллургический;
- пирометаллургический.
Гидрометаллургический не нашел своего широкого применения из-за невозможности извлекать попутно с медью драгоценные металлы.
Пирометаллургический способ пригоден для переработки всех руд и включает следующие операции:
- подготовка руд к плавке;
- плавка на штейн;
- конвертирование штейна;
- рафинирование меди.

Подготовка руд к плавке
Подготовка руд заключается в проведении обогащения и обжига. Обогащение медных руд проводят методом флотации. В результате получают медный концентрат, содержащий до 35% меди и до 50% серы. Концентраты обжигают обычно в печах кипящего слоя с целью снижения содержания серы до оптимальных значений. При обжиге происходит окисление серы при температуре 750 – 800 °С, часть серы удаляется с газами. В результате получают продукт, называемый огарком.
Плавку на штейн
Плавку на штейн ведут в отражательных или электрических печах при температуре 1250 – 1300 °С. В плавку поступают обожженные концентраты медных руд, в ходе нагревания которых протекают реакции восстановления оксида меди и высших оксидов железа
6CuO + FeS = 3Cu2O + FeO + SO2
FeS + 3Fe3O4 + 5SiO2 = 5(2FeO·SiO2) + SO2
В результате взаимодействия Cu2O с FeS образуется Cu2S по реакции:
Cu2O + FeS = Cu2S + FeO
Сульфиды меди и железа, сплавляясь между собой, образуют штейн, а расплавленные силикаты железа, растворяя другие оксиды, образуют шлак. Штейн содержит 15 – 55% Cu; 15 – 50% Fe; 20 – 30% S. Шлак состоит в основном из SiO2, FeO, CaO, Al2O3.
Штейн содержит 15 – 55% Cu; 15 – 50% Fe; 20 – 30% S. Шлак состоит в основном из SiO2, FeO, CaO, Al2O3.
Штейн и шлак выпускают по мере их накопления через специальные отверстия.
Конвертирование штейна
Конвертирование штейна осуществляется в медеплавильных конвертерах (рисунок 44) путем продувки его воздухом для окисления сернистого железа, перевода железа в шлак и выделения черновой меди.
Конвертеры имеют длину 6 – 10 м и наружный диаметр 3 – 4 м. Заливку расплавленного штейна, слив продуктов плавки и удаление газов осуществляют через горловину, расположенную в средней части корпуса конвертера. Для продувки штейна подается сжатый воздух через фурмы, расположенные по образующей конвертера. В одной из торцевых стенок конвертера расположено отверстие, через которое проводится пневматическая загрузка кварцевого флюса, необходимого для удаления железа в шлак.
Процесс продувки ведут в два периода. В первый период в конвертер заливают штейн и подают кварцевый флюс. В этом периоде протекают реакции окисления сульфидов
В этом периоде протекают реакции окисления сульфидов
2FeS + 3O2 = 2Fe + 2SO2,
2Cu2S + 3O2 = 2Cu2O + 2SO2
Образующаяся закись железа взаимодействует с кварцевым флюсом и удаляется в шлак
2FeO + SiO2 = (FeO)2·SiO2
По мере накопления шлака его частично сливают и заливают в конвертер новую порцию исходного штейна, поддерживая определенный уровень штейна в конвертере. Во втором периоде закись меди взаимодействует с сульфидом меди, образуя металлическую медь
2Cu2O + Cu2S = 6Cu + SO2
Таким образом, в результате продувки получают черновую медь, содержащую 98,4 – 99,4% Cu. Полученную черновую медь разливают в плоские изложницы на ленточной разливочной машине.
Рафинирование меди.
Для получения меди необходимой чистоты черновую медь подвергают огневому и электролитическому рафинированию. При этом, помимо удаления примесей можно извлекать также благородные металлы.
При огневом рафинировании черновую медь загружают в пламенную печь и расплавляют в окислительной атмосфере. В этих условиях из меди удаляются в шлак те примеси, которые обладают большим сродством к кислороду, чем медь.
Для ускорения процесса рафинирования в ванну с расплавленной медью подают сжатый воздух. Большинство примесей в виде оксидов переходят в шлак (Fe2O3, Al2O3, SiO2), а некоторые примеси при рафинировании удаляются с газами. Благородные металлы при огневом рафинировании полностью остаются в меди. Кроме благородных металлов в меди в небольших количествах присутствуют примеси сурьмы, селена, теллура, мышьяка. После огневого рафинирования получают медь чистотой 99 – 99,5%.
Для удаления этих примесей, а также для извлечения золота и серебра медь подвергают электролитическому рафинированию.
Электролиз ведут в специальных ваннах, футерованных внутри свинцом или другим защитным материалом. Аноды изготовляют из меди огневого рафинирования, а катоды – из тонких листов чистой меди. Электролитом служит раствор сернокислой меди. При пропускании постоянного тока анод растворяется и медь переходит в раствор. На катодах разряжаются ионы меди, осаждаясь на них прочным слоем чистой меди.
Электролитом служит раствор сернокислой меди. При пропускании постоянного тока анод растворяется и медь переходит в раствор. На катодах разряжаются ионы меди, осаждаясь на них прочным слоем чистой меди.
Находящиеся в меди примеси благородных металлов выпадают на дно ванны в виде остатка (шлама). После электролитического рафинирования получают медь чистотой 99,95 – 99,99%.
ПОДЕЛИСЬ ИНТЕРЕСНОЙ ИНФОРМАЦИЕЙ
Получение и химические реакции меди
Нахождение в природе.
Медь встречается главным образом в виде сульфидных соединений. Наиболее важные минералы — медный блеск Cu2S, медный колчедан (халькопирит) CuFeS2 и борнит Cu3FeS2 входят в состав так называемых полиметаллических сульфидных руд. Реже встречаются кислородсодержащие соединения: малахит (основной карбонат меди) СuСО3 • Сu(ОН)2, азурит 2СuСО3 • Сu(ОН)2 и куприт СuO2.
Физические свойства.

Медь — металл красного цвета, плавится при температуре 1083°С, кипит при 2877°С. Чистая медь довольно мягка, легко поддается прокатке и вытягиванию. Примеси увеличивают твердость меди. Медь отличается очень высокой электро- и теплопроводностью. Примеси мышьяка и сурьмы значительно уменьшают электропроводность меди. Медь образует различные сплавы (латуни, бронзы и др.).
Химические свойства.
Медь относится к числу малоактивных металлов. На холоду она очень слабо взаимодействует с кислородом воздуха, покрываясь пленкой оксида, которая препятствует дальнейшему окислению меди. При нагревании медь окисляется полностью:
2Cu + O2 = 2СuО
Сухой хлор на холоду не взаимодействует с медью, однако в присутствии влаги реакция проходит довольно энергично:
Сu + Сl2 = СuС12.
При нагревании медь довольно энергично взаимодействует с серой:
Си + S = CuS.
Медь может растворятся только в кислотах-окислителях. В концентрированной серной кислоте она растворяется только при нагреваний, a в азотной — и на холоду:
Сu+ 2H2SO4 = CuSO4 + SO2 + 2Н2O,
ЗСu + 8HNO3(Разбавл. ) = 3Cu(NO3)2 + 2NO + 4Н2O,
) = 3Cu(NO3)2 + 2NO + 4Н2O,
Сu + 4HNO3(Конц .) = Cu(NO3)2+ 2NO + 2Н2O.
Получение.
Процесс получения меди состоит из нескольких стадий. Сначала сульфидную руду обжигают. При этом часть меди превращается в оксид:
4CuFeS2 + 13O2 = 4CuO + 2Fe203 + 8SO2.
Затем проводят плавку на штейн и получают сульфид меди (I). При этом к огарку прибавляют кокс и песок для образования шлака:
2CuO + FeS + С + SiO2 = Cu2S + FeSi03 + СО
или
CuO + FeO + CuS + С + SiO2 = Cu2S + FeSiO3+ CO.
Далее штейн подвергают конвертерной плавке:
9Cu2 S + 3O2 = 2Cu2 O + 2SO2 ,
2CuO2 + Cu2 S = 6Cu + SO2 .
Получаемая медь называется черновой.
Очищают медь рафинированием. Электролитом служит раствор сульфата меди, анодом — медные болванки ,катодом — пластинка чистой меди. При пропускании электрического тока через электролит медь анода растворяется, а на катоде выделяется чистая медь.
При пропускании электрического тока через электролит медь анода растворяется, а на катоде выделяется чистая медь.
Оксид меди
Обладает основными свойствами. Он может взаимодействовать с кислотами и кислотными оксидами:
CuO + H2SО4 = CuSО4 + Н2О,
CuO + SО3 = CuSО4.
Оксид меди не растворим в воде. При нагревании оксида меди и присутствии восстановителя довольно легко происходит его восстановление:
CuO + Н2 = Сu + Н2O,
СuО + СО = Сu + СO2.
Оксид меди получают окислением меди при нагревании или прокаливанием гидроксида меди:
2Сu + O2 = 2СuО,
Cu(OH)2 = CuO + Н2O.
Оксид меди встречается в природе в продуктах выветривания некоторых медных руд. Он используется в производстве стекла и эмалей как зеленый и синий красители (медно-рубиновое стекло), как окислитель в органическом анализе и в медицине.
Гидроксид меди
Гидроксид меди Сu(ОН)2. Выпадает в виде осадка при действии на растворы солей меди (II) растворов щелочей (но не аммиака):
CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4.
При действии аммиака на соли меди (II) сначала выпадает гидроксид меди, который очень легко растворяется в избытке аммиака с образованием аммиаката меди:
Cu(OH)2 + 4NH4OH = [Cu(NH3)4](OH)2 + 4Н2O
или
Cu(OH)2 + 4NH3 = [Cu(NH3)4](OH)2.
Аммиакат меди окрашен в интенсивный сине-фиолетовый цвет, Поэтому он позволяет обнаружить малые количества ионов меди (П) в растворе. Эта реакция применяется в аналитической химии.
Гидроксид меди обладает очень слабо выраженными амфотерными свойствами. В кислотах он растворяется легко, в концентрированных растворах щелочей — с большим трудом. В первом случае образуются соли меди, во втором — гидроксокупраты:
Сu(ОH)2 + 2NaOH = Na2[Cu(OH)4].
Гидроксид меди может восстанавливаться до гемиоксида меди при нагревании С различными не очень сильными восстановителями: альдегидами, сахарами, гидразином, гидроксиламином и др.:
2Cu(OH)2 + R—СНО → Cu2O + R—COOH + 2H2O.
Гемиоксид, или оксид меди (I)
Гемиоксид, или оксид меди (I), Си20. Обладает только основными свойствами. Часть солей меди (I) хорошо растворима, но довольно неустойчива и легко окисляется кислородом воздуха. Устойчивыми соединениями меди (I) являются, как правило, либо нерастворимые соединения (Cu2S, Cu2O, Cu2I2), либо комплексные соединения (Cu(NH3)+2 и др.). Гемиоксид меди применяется для изготовления купроксных выпрямителей переменного тока.
При растворении гемиоксида меди в кислородсодержащих кислотах, например серной, образуются соли меди (II) и медь:
Cu2O + H2SO4 = CuSO4 + Сu + Н2O,
а при растворении в галогеноводородных кислотах — соли меди (I):
Cu20 + 2НС1 = 2СuС1 + Н2O.
Многие соли меди (II) хорошо растворимы в воде, но подвержены гидролизу, поэтому в растворе всегда должен быть небольшой избыток кислоты. Нерастворимыми солями меди (II) являются сульфид CuS, карбонат (основной карбонат) СuСO3• Сu(ОН)2 • 0,5Н2О, оксалат СuС2O4 и фосфат Сu3(РO4)2.
Под действием восстановителей соли меди (II) в кислом растворе могут восстанавливаться до солей меди (I):
2CuSO4 + 4KI = 2K2SO4 + Cu2I2 + I2
Аммиачные растворы солей меди (I) могут взаимодействовать с ацетиленом, образуя ацетиленид меди;
СН≡СН + 2CuCl = Cu2C2 + 2НС1.
Литература [3]
Добыча и переработка меди: переработка медных руд
Перейти к навигации
Просмотреть PDF Загрузить PowerPoint
Оксидные и сульфидные руды подвергаются различным процессам очистки до меди с чистотой 99,99%.
Переработка меди — это сложный процесс, который начинается с добычи руды (менее 1% меди) и заканчивается получением листов меди с чистотой 99,99%, называемых катодами , которые в конечном итоге будут превращены в изделия для повседневного использования. Наиболее распространенные типы руд, оксид меди и сульфид меди подвергаются двум различным процессам, гидрометаллургии и пирометаллургии, соответственно, из-за различного химического состава руды. Оксиды меди более распространены вблизи поверхности, но считаются бедной рудой с более низкой концентрацией меди. Хотя для этого требуется добывать и перерабатывать больше руды, этот процесс дешевле, поэтому оксиды все еще можно добывать с прибылью. С другой стороны, хотя сульфидные руды меди менее распространены, они содержат больше меди. Хотя затраты на обработку выше, в конечном итоге можно извлечь больше меди. Поскольку каждый рудник уникален по своему минеральному составу, концентрации и количеству, планировщики рудника должны определить наиболее экономичную и прибыльную переработку руды. Когда это экономически целесообразно, рудник может добывать оба типа медных минералов; когда это невозможно, шахты будут перерабатывать только оксиды меди или сульфиды меди.
Когда это экономически целесообразно, рудник может добывать оба типа медных минералов; когда это невозможно, шахты будут перерабатывать только оксиды меди или сульфиды меди.
Первые этапы переработки меди одинаковы для обеих руд: добыча и транспортировка. Добыча меди обычно осуществляется открытым способом , при котором ряд ступенчатых уступов выкапывается все глубже и глубже в землю с течением времени. Для извлечения руды используется буровое оборудование, чтобы просверлить отверстия в твердой породе, а взрывчатые вещества вставляются в отверстия для взрыва и разрушения породы. Полученные валуны готовы к транспортировке; специализированные самосвалы, конвейеры, поезда и вагоны-челноки могут использоваться для перевозки руды с места взрывных работ на место переработки. Размеры оборудования, необходимого для перевозки тонн и тонн руды, огромны. Затем большая часть руды проходит через первичную дробилку, которая обычно располагается очень близко к карьеру, а иногда и в нем. Эта первичная дробилка уменьшает размер руды от валунов до камней размером с мяч для гольфа.
Эта первичная дробилка уменьшает размер руды от валунов до камней размером с мяч для гольфа.
A. Переработка оксидной руды
Оксидные руды обычно перерабатываются с использованием гидрометаллургии . В этом процессе используются водные растворы (на водной основе) для извлечения и очистки меди из руд оксида меди при обычных температурах, обычно в три этапа: кучное выщелачивание, экстракция растворителем и электролиз.
Кучное выщелачивание и извлечение растворителем из оксидной руды.
Кучное выщелачивание — это процесс использования перколяционных химических растворов для выщелачивания металлов. Кучное выщелачивание очень часто используется для руды с низким содержанием золота, которую в противном случае было бы нецелесообразно направлять на процесс измельчения. После добычи, транспортировки и дробления до размера гравия или мяча для гольфа дробленая руда складывается в кучу поверх непроницаемого слоя на небольшом уклоне. Выщелачивающий реагент (разбавленная серная кислота) разбрызгивается через разбрызгиватели на вершине отвала и просачивается вниз через отвал, где он растворяет медь из руды. Полученный «богатый» выщелачивающий раствор серной кислоты и медного купороса собирается в небольшой бассейн. Соединение меди теперь можно увидеть в концентрациях от 60 до 70%.
Полученный «богатый» выщелачивающий раствор серной кислоты и медного купороса собирается в небольшой бассейн. Соединение меди теперь можно увидеть в концентрациях от 60 до 70%.
Вторым этапом является экстракция растворителем , при которой две несмешивающиеся (несмешивающиеся) жидкости перемешиваются и разделяются, в результате чего медь переходит из одной жидкости в другую. Насыщенный выщелачивающий раствор энергично смешивают с растворителем. Медь мигрирует из выщелачивающего раствора в растворитель. Затем две жидкости разделяют по растворимости, при этом медь остается в растворе в растворителе, а примеси остаются в выщелачивающем растворе. Затем оставшийся выщелачивающий раствор рециркулируют, добавляя дополнительную кислоту и отправляя ее обратно в спринклеры в процессе кучного выщелачивания.
Электролиз — это последний этап переработки оксидной руды в медные катоды.
Последний этап называется электролизом , разновидностью электролиза. Электрический ток проходит через инертный анод (положительный электрод) и через раствор меди из предыдущего этапа, который действует как электролит . Положительно заряженные ионы меди (называемые катионами) выходят из раствора и наносятся на катод (отрицательный электрод) в виде меди чистотой 99,99%.
Электрический ток проходит через инертный анод (положительный электрод) и через раствор меди из предыдущего этапа, который действует как электролит . Положительно заряженные ионы меди (называемые катионами) выходят из раствора и наносятся на катод (отрицательный электрод) в виде меди чистотой 99,99%.
B. Переработка сульфидной руды
Сульфидные руды обычно перерабатываются с использованием пирометаллургии , извлечения и очистки металлов с помощью процессов, включающих применение тепла. В этом процессе используется ряд физических стадий и высоких температур для извлечения и очистки меди из медных сульфидных руд в четыре основных этапа: 1) пенная флотация, 2) сгущение, 3) плавка и 4) электролиз.
После добычи, транспортировки и дробления до размера гравия или мяча для гольфа измельченная руда далее перерабатывается на мельнице с использованием вторичных дробилок и измельчается до гальки и, наконец, до мелкого песка. После измельчения медной руды в нее добавляют жидкость, превращающую ее в суспензию. Шлам представляет собой смесь ценных минералов медной руды и «бесполезной» породы, называемой пустой породой (произносится «банда»). Суспензия помещается в резервуар, и процесс называется пенная флотация используется для отделения медных минералов от пустой породы. Химические реагенты, называемые «сборщиками», добавляются в суспензию и связываются с частицами меди, делая их гидрофобными или водонепроницаемыми. Трубы используются для подачи воздуха на дно резервуара для создания пузырьков, которые поднимаются на поверхность, увлекая за собой водостойкие частицы сульфида меди. Затем пена богатых медью пузырьков в верхней части резервуара снимается для дальнейшей обработки. Пустая порода опускается на дно резервуара и удаляется или утилизируется как хвостохранилище .
После измельчения медной руды в нее добавляют жидкость, превращающую ее в суспензию. Шлам представляет собой смесь ценных минералов медной руды и «бесполезной» породы, называемой пустой породой (произносится «банда»). Суспензия помещается в резервуар, и процесс называется пенная флотация используется для отделения медных минералов от пустой породы. Химические реагенты, называемые «сборщиками», добавляются в суспензию и связываются с частицами меди, делая их гидрофобными или водонепроницаемыми. Трубы используются для подачи воздуха на дно резервуара для создания пузырьков, которые поднимаются на поверхность, увлекая за собой водостойкие частицы сульфида меди. Затем пена богатых медью пузырьков в верхней части резервуара снимается для дальнейшей обработки. Пустая порода опускается на дно резервуара и удаляется или утилизируется как хвостохранилище .
Следующей стадией после пенной флотации является стадия сгущения . Пена выливается в большие резервуары, называемые сгустителями. Пузырьки лопаются, и твердые частицы пенного раствора оседают на дне резервуара. Затем твердые вещества фильтруют для удаления избыточной воды, которую можно повторно использовать при переработке дополнительных партий сульфидной руды. Конечный продукт стадии сгущения представляет собой комбинацию 30% меди и других металлов; этот медный концентрат затем направляется на плавильный завод.
Пузырьки лопаются, и твердые частицы пенного раствора оседают на дне резервуара. Затем твердые вещества фильтруют для удаления избыточной воды, которую можно повторно использовать при переработке дополнительных партий сульфидной руды. Конечный продукт стадии сгущения представляет собой комбинацию 30% меди и других металлов; этот медный концентрат затем направляется на плавильный завод.
Аноды на шахте Багдад в Аризоне. (Фото предоставлено: Фотоархив ADMMR, Геологическая служба Аризоны).
На плавильном заводе используются высокие температуры для дальнейшей очистки руды в серии стадий плавки . Медный концентрат сначала направляют в плавильную печь, где он нагревается до 2300 °F и превращается в расплавленную жидкость. Нагретую жидкость заливают в шлакоотстойную печь. На этом этапе получается комбинация штейна, смеси меди, серы и железа, и шлака, плотного стекловидного материала, состоящего из железа, кремнезема и других примесей. Медный штейн, созданный плавильной печью, содержит 58-60% меди. Затем расплавленный штейн направляется в другую печь, называемую конвертером, для сжигания оставшегося железа и серы; продукт упоминается как черновая медь, которая содержит 98% меди, и доставили в анодную плавку. Черновая медь желтая; когда кислород в меди выгорает в анодной плавке, она становится сине-зеленой. Полученный продукт, расплавленную анодную медь, заливают в формы, называемые колесами для литья анодов. Охлажденные пластины анода состоят из 99% чистой меди, теперь окрашены в медный цвет, имеют две отлитые сверху ручки, имеют толщину два дюйма, ширину три фута, высоту три с половиной фута и вес 750 фунтов.
Затем расплавленный штейн направляется в другую печь, называемую конвертером, для сжигания оставшегося железа и серы; продукт упоминается как черновая медь, которая содержит 98% меди, и доставили в анодную плавку. Черновая медь желтая; когда кислород в меди выгорает в анодной плавке, она становится сине-зеленой. Полученный продукт, расплавленную анодную медь, заливают в формы, называемые колесами для литья анодов. Охлажденные пластины анода состоят из 99% чистой меди, теперь окрашены в медный цвет, имеют две отлитые сверху ручки, имеют толщину два дюйма, ширину три фута, высоту три с половиной фута и вес 750 фунтов.
Электролиз является завершающим процессом очистки сульфидной руды в медные катоды.
Затем пластины медных анодов очищают на заключительном этапе, называемом электролизом . Анодные плиты подвешиваются в большой емкости, наполненной раствором электролита, состоящим из сульфата меди и серной кислоты. Между анодами подвешивают тонкие листы чистой меди, которые называются катодами и весят около 15 фунтов каждый. Подается электрический ток, и положительно заряженные ионы меди (называемые катионами) покидают анод (положительный электрод) и перемещаются в растворе через раствор электролита для нанесения покрытия на катод (отрицательный электрод). Другие металлы и примеси также покидают анод и падают на дно резервуара или остаются в растворе электролита. Эти примеси собираются и могут быть очищены для извлечения других металлов, таких как серебро и золото. После 14 дней электролиза аноды постепенно исчезли, а медные катоды теперь весят 375 фунтов каждый и содержат 9Медь чистотой 9,99%. Катоды вынимают из бака и промывают водой, чтобы предотвратить дальнейшую реакцию. Готовые медные катоды затем можно превратить в провода, пластины, трубки и другие медные изделия.
Подается электрический ток, и положительно заряженные ионы меди (называемые катионами) покидают анод (положительный электрод) и перемещаются в растворе через раствор электролита для нанесения покрытия на катод (отрицательный электрод). Другие металлы и примеси также покидают анод и падают на дно резервуара или остаются в растворе электролита. Эти примеси собираются и могут быть очищены для извлечения других металлов, таких как серебро и золото. После 14 дней электролиза аноды постепенно исчезли, а медные катоды теперь весят 375 фунтов каждый и содержат 9Медь чистотой 9,99%. Катоды вынимают из бака и промывают водой, чтобы предотвратить дальнейшую реакцию. Готовые медные катоды затем можно превратить в провода, пластины, трубки и другие медные изделия.
C. Переработка меди
Помимо переработки медных руд, новый и старый медный лом или медные сплавы могут быть переплавлены, повторно очищены и переработаны в новые компоненты. По оценкам, такая переработка обеспечивает 50% меди, используемой в медной промышленности (Scott, 2011). В 2010 г. было переработано 770 000 метрических тонн меди на сумму около шести миллиардов долларов (Papp, 2010).
В 2010 г. было переработано 770 000 метрических тонн меди на сумму около шести миллиардов долларов (Papp, 2010).
Инновации: Введение в медь: добыча и добыча
Применение меди в металлургии меди и медных сплавов
Вин Калькатт
Медный век | Бронзовый век | Средние века и позднее | Горное дело
Медные минералы и руды встречаются как в изверженных, так и в осадочных породах. Добыча медных руд осуществляется одним из двух способов.
- Подземная добыча полезных ископаемых осуществляется путем проходки стволов до соответствующих уровней, а затем проходки горизонтальных туннелей, называемых штольнями, для достижения руды. Однако подземная добыча относительно дорога и обычно ограничивается богатыми рудами. Эль-Теньенте в Чили — крупнейший в мире подземный медный рудник.
- Добыча открытым способом применяется, когда рудные тела обширны, имеют низкое содержание и находятся относительно близко к поверхности, где их можно добывать после удаления вскрышных пород.
 Чили также может похвастаться крупнейшим в мире (с точки зрения добычи) открытым медным рудником Escondida. Крупнейший медный рудник в Северной Америке (и крупнейший в мире рукотворный раскоп) — это рудник Бингем-Каньон недалеко от Солт-Лейк-Сити, штат Юта. Программа модернизации стоимостью 1,5 миллиарда долларов, завершенная в 1998 году, превратила Бингем-Каньон в производителя меди с самой низкой себестоимостью в Северной Америке, образец операционной эффективности и соблюдения экологических норм.
Чили также может похвастаться крупнейшим в мире (с точки зрения добычи) открытым медным рудником Escondida. Крупнейший медный рудник в Северной Америке (и крупнейший в мире рукотворный раскоп) — это рудник Бингем-Каньон недалеко от Солт-Лейк-Сити, штат Юта. Программа модернизации стоимостью 1,5 миллиарда долларов, завершенная в 1998 году, превратила Бингем-Каньон в производителя меди с самой низкой себестоимостью в Северной Америке, образец операционной эффективности и соблюдения экологических норм.
Медь содержится в земной коре и в океанах, хотя количество в последних считается незначительным и составляет не более восьми месяцев добычи при современных темпах. Считается, что верхние 10 километров земной коры содержат в среднем около 33 частей на миллион меди. Для коммерческой эксплуатации месторождения меди обычно должны содержать более 0,5% меди, а предпочтительно более 2%. Известные запасы руды более высокого качества в мире составляют почти 1 миллиард тонн меди. При нынешнем темпе добычи, который составляет около 13,9миллионов тонн (12,5 миллионов метрических тонн) в год, известные запасы меди могут быть истощены примерно через 65 лет. Однако успешная разведка новых месторождений полезных ископаемых, технологические достижения в горнодобывающей и добывающей металлургии (которые позволяют разрабатывать более бедные руды, тем самым увеличивая совокупность известных запасов) и использование меди (что позволяет более экономно использовать медь там, где использовались большие количества в прошлом) и продолжающаяся переработка металлолома, вероятно, на неопределенный срок предотвратят истощение запасов этого ценного металла.
Однако успешная разведка новых месторождений полезных ископаемых, технологические достижения в горнодобывающей и добывающей металлургии (которые позволяют разрабатывать более бедные руды, тем самым увеличивая совокупность известных запасов) и использование меди (что позволяет более экономно использовать медь там, где использовались большие количества в прошлом) и продолжающаяся переработка металлолома, вероятно, на неопределенный срок предотвратят истощение запасов этого ценного металла.
Например, по оценкам, на глубине первой мили земной коры континентов диффузно распределено 3x 10 18 метрических тонн меди. Относительно концентрированная часть этой меди составляет лишь небольшую часть от общего количества, составляющую примерно 10 10 метрических тонны в месторождениях с содержанием 0,25% или более. При текущей мировой добыче полезных ископаемых это представляет собой запас меди на миллион лет, теоретически доступный в извлекаемой части земной коры.
В таблице 4 показаны некоторые из наиболее распространенных минералов меди. Некоторые из них уже давно имеют ценность сами по себе, например, малахит, ценившийся за его необычный и приятный внешний вид и тысячелетиями использовавшийся в украшениях и украшениях.
Некоторые из них уже давно имеют ценность сами по себе, например, малахит, ценившийся за его необычный и приятный внешний вид и тысячелетиями использовавшийся в украшениях и украшениях.
| Минерал | Состав | Вес. % Медь | Цвет | Блеск |
|---|---|---|---|---|
| Самородная медь | Cu | 98+ | Медно-красный | Металлик |
| Куприт | Медь 2 0 | 88,8 | Красный | Адамантин |
| Халькоцит | Медь 2 0 | 79,9 | Темно-серый | Металлик |
| Халькопирит (Золото дураков) | Fe x Cu y S | 10 прибл. | Золото | Металлик |
| Ковеллит | CuS | 66,4 | Синий индиго | |
| Борнит (Павлинья руда) | Cu 5 FeS 4 | 63,3 | Золотисто-коричневый до медно-красного | Металлик |
| Малахит | CuCO 3 Cu(OH) 4 | 57,5 | ярко-зеленый | от шелковистого до землистого |
| Азурит | 2CuCO 3 Cu(OH) 2 | 55,3 | Синий | Стекловидное тело в адамантин |
| Антлерит | Cu 3 SO 4 (ОН) 4 | 53,7 | Зеленый | |
| Хризоколла | CuSiO 3 2H 2 O | 36,2 | Голубовато-зеленый, небесно-голубой, бирюзовый | Стекловидный в землистый |
| Халькопирит | CuFeS 2 | 34,6 | Золотисто-желтый | от металлического до непрозрачного |
Пустая порода, или пустая порода , должна быть отделена от сульфидных минералов для выплавки металлической меди из руды. Безусловно, наибольшая часть меди извлекается из сульфидов меди, железа и иногда других металлов. Такие руды образуются из серосодержащих вулканических магм, разделившихся на сульфиды металлов и кремнистые расплавы. Медь почти полностью сконцентрировалась в сульфидной фракции, и если она отделяется от кремнистого расплава, она может отлагаться в жилах или трещинах вмещающей породы в результате гидротермальной или другой геологической деятельности. Во многих рудах (и в большинстве обнаруженных на западе США) минералы меди встречаются в виде дисперсии мелких частиц. Такие руды называются порфиры . Там, где минерализованные породы обнажаются или разрушаются, сульфидные минералы подвергаются химическим изменениям под действием воздуха, грунтовых вод и тепла, что приводит к образованию другой основной разновидности медных минералов — окисленных руд.
Безусловно, наибольшая часть меди извлекается из сульфидов меди, железа и иногда других металлов. Такие руды образуются из серосодержащих вулканических магм, разделившихся на сульфиды металлов и кремнистые расплавы. Медь почти полностью сконцентрировалась в сульфидной фракции, и если она отделяется от кремнистого расплава, она может отлагаться в жилах или трещинах вмещающей породы в результате гидротермальной или другой геологической деятельности. Во многих рудах (и в большинстве обнаруженных на западе США) минералы меди встречаются в виде дисперсии мелких частиц. Такие руды называются порфиры . Там, где минерализованные породы обнажаются или разрушаются, сульфидные минералы подвергаются химическим изменениям под действием воздуха, грунтовых вод и тепла, что приводит к образованию другой основной разновидности медных минералов — окисленных руд.
Нет недостатка в медных ресурсах. Фактически, медь является одним из самых распространенных металлических элементов в земной коре. Средняя расчетная концентрация составляет от 55 до 70 мг/кг, что ниже хрома (200 мг/кг) и цинка (132), но выше олова и свинца. Во многих частях мира находятся промышленно эксплуатируемые месторождения медных руд, часто связанные с процессами горообразования. Отложения встречаются во многих местах в западных кордильерах Америки, в основном в Соединенных Штатах и Чили, а также в районах североамериканских равнин, таких как Мичиган, Онтарио, Квебек и Манитоба, на участках, связанных с докембрийским щитом. Медь также встречается во многих других странах мира. Перу, Польша, Мексика, Заир, Замбия и Папуа-Новая Гвинея исторически были в числе ведущих производителей, и хотя производство в Африке резко сократилось в последние годы из-за политических трудностей, остаются большие неиспользованные ресурсы. Кроме того, известно, что огромные количества меди существуют в виде «глубоководных конкреций», разбросанных по дну океана, хотя высокие затраты на добычу до сих пор препятствуют их коммерческой эксплуатации.
Средняя расчетная концентрация составляет от 55 до 70 мг/кг, что ниже хрома (200 мг/кг) и цинка (132), но выше олова и свинца. Во многих частях мира находятся промышленно эксплуатируемые месторождения медных руд, часто связанные с процессами горообразования. Отложения встречаются во многих местах в западных кордильерах Америки, в основном в Соединенных Штатах и Чили, а также в районах североамериканских равнин, таких как Мичиган, Онтарио, Квебек и Манитоба, на участках, связанных с докембрийским щитом. Медь также встречается во многих других странах мира. Перу, Польша, Мексика, Заир, Замбия и Папуа-Новая Гвинея исторически были в числе ведущих производителей, и хотя производство в Африке резко сократилось в последние годы из-за политических трудностей, остаются большие неиспользованные ресурсы. Кроме того, известно, что огромные количества меди существуют в виде «глубоководных конкреций», разбросанных по дну океана, хотя высокие затраты на добычу до сих пор препятствуют их коммерческой эксплуатации.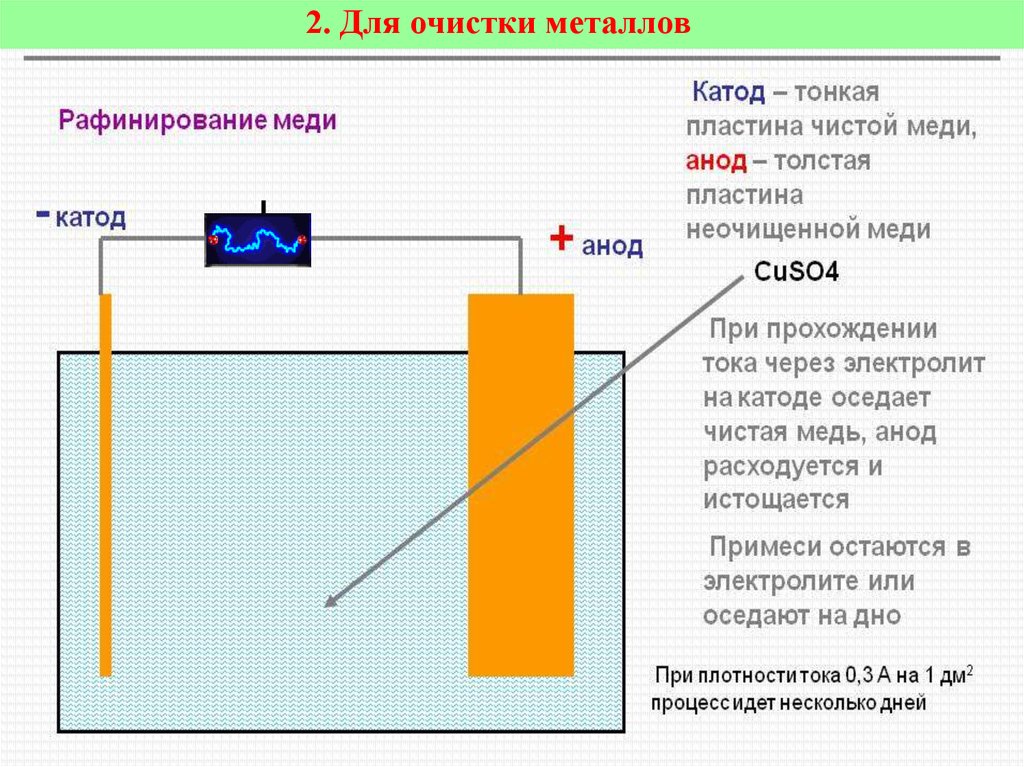 Чили и США являются, соответственно, двумя ведущими странами-производителями меди в мире, причем Чили обогнала США в начале 19 века.90-е.
Чили и США являются, соответственно, двумя ведущими странами-производителями меди в мире, причем Чили обогнала США в начале 19 века.90-е.
Добыча
Руды сначала механически дробят и измельчают, чтобы почти все частицы медных минералов были освобождены от пустой породы. Флотацию с нагнетанием воздуха и интенсивным перемешиванием проводят с пылевидной рудой, находящейся во взвешенном состоянии в воде, к которой добавлены поверхностно-активные вещества. В процессе получают концентраты , содержащие примерно 30% меди, которые последовательно подают в плавильный цех , печь, в которой удаляется большая часть железа и серы, затем в 9конвертер 0291 или конвертер печь , где удаляется большая часть остаточного железа и других примесей. (В зависимости от типа используемой плавильной и конвертерной печи может быть извлечено до 99+% серы. Она используется для производства серной кислоты, которая продается или используется для непосредственного выщелачивания меди из подходящих руд, тем самым обходя весь цикл плавки-конверсии. ) В результате получается нечистая (98+%) форма металла, известная как черновая медь (из-за ее внешнего вида). Затем блистер подвергается дальнейшей огневой очистке, чтобы отрегулировать содержание серы и кислорода, в результате чего получается металл, достаточно чистый для многих других применений, кроме электрических. Однако, поскольку очищенный огнем металл может содержать коммерчески выгодные концентрации драгоценных металлов (в основном серебра и золота), большая его часть отливается в толстые листы, известные как аноды, которые отправляются в большие электролизеры, где происходит окончательное рафинирование. Постоянный электрический ток, проходящий через ячейки, растворяет аноды и осаждает медь на катодах. Конечным продуктом процесса рафинирования является медь электролитического вязкого пека (ETP), обычно содержащая от 99,94 и 99,96% Cu. Катоды переплавляются в контролируемых условиях и отливаются в формы, пригодные для дальнейшей обработки.
) В результате получается нечистая (98+%) форма металла, известная как черновая медь (из-за ее внешнего вида). Затем блистер подвергается дальнейшей огневой очистке, чтобы отрегулировать содержание серы и кислорода, в результате чего получается металл, достаточно чистый для многих других применений, кроме электрических. Однако, поскольку очищенный огнем металл может содержать коммерчески выгодные концентрации драгоценных металлов (в основном серебра и золота), большая его часть отливается в толстые листы, известные как аноды, которые отправляются в большие электролизеры, где происходит окончательное рафинирование. Постоянный электрический ток, проходящий через ячейки, растворяет аноды и осаждает медь на катодах. Конечным продуктом процесса рафинирования является медь электролитического вязкого пека (ETP), обычно содержащая от 99,94 и 99,96% Cu. Катоды переплавляются в контролируемых условиях и отливаются в формы, пригодные для дальнейшей обработки.
Современные методы добычи обеспечивают экономичное выщелачивание и электрохимическое извлечение меди из бедных руд, а методы добычи постоянно совершенствуются и разрабатываются для достижения наиболее эффективного удаления меди из самых разных руд из источников по всему миру. Методы извлечения меди из окисленных руд сильно отличаются от тех, которые используются для сульфидных руд. Окисленные руды, состоящие из силикатов, карбонатов и сульфатов, обрабатывают несколькими методами, все из которых включают в себя ту или иную форму выщелачивания измельченной руды серной кислотой с получением нечистых растворов сульфата меди. Сегодня более 13% всей «новой» меди производится из фильтратов, которые обычно концентрируют с помощью экстракции растворителем (SX) и удаляют из них медь с помощью обычного электролиза (EW), так называемого процесса SXEW. Сульфидные руды не подвергаются эффективному воздействию серной кислоты, но они могут быть выщелочены при предварительном окислении при длительном воздействии атмосферы и при контакте с встречающимися в природе бактериями Thiobacillus Thiooxidans и Thiobacillus Ferrooxidans.
Методы извлечения меди из окисленных руд сильно отличаются от тех, которые используются для сульфидных руд. Окисленные руды, состоящие из силикатов, карбонатов и сульфатов, обрабатывают несколькими методами, все из которых включают в себя ту или иную форму выщелачивания измельченной руды серной кислотой с получением нечистых растворов сульфата меди. Сегодня более 13% всей «новой» меди производится из фильтратов, которые обычно концентрируют с помощью экстракции растворителем (SX) и удаляют из них медь с помощью обычного электролиза (EW), так называемого процесса SXEW. Сульфидные руды не подвергаются эффективному воздействию серной кислоты, но они могут быть выщелочены при предварительном окислении при длительном воздействии атмосферы и при контакте с встречающимися в природе бактериями Thiobacillus Thiooxidans и Thiobacillus Ferrooxidans.
В ноябрьском номере журнала «Инновации» за 1997 год была опубликована простая инфографика о добыче и добыче меди.
Медный век
Додинастические египтяне очень хорошо знали медь. В иероглифическом письме символ, используемый для обозначения вечной жизни, анкх, также использовался для обозначения меди. Позднее греческие философы приняли этот символ, слегка изменив его, как . Связь между вечной долговечностью и рентабельностью в течение всего срока службы меди и ее сплавов, безусловно, не случайна!
В иероглифическом письме символ, используемый для обозначения вечной жизни, анкх, также использовался для обозначения меди. Позднее греческие философы приняли этот символ, слегка изменив его, как . Связь между вечной долговечностью и рентабельностью в течение всего срока службы меди и ее сплавов, безусловно, не случайна!
Египтяне получали большую часть своей меди из Холмов Красного моря, но медь старше Древнего Египта на несколько тысячелетий, и теперь известно, что более старая цивилизация, основанная на Евфрате, также использовала новую медь и использовала хорошо развитые методы плавки. Самыми ранними известными артефактами, сделанными из плавленого металла, была медь, а раскопки в Чатал-Хуюке недалеко от Коньи в Южной Анатолии дали шлаки, полученные в результате плавки меди, датируемые 7000 годом до нашей эры. Другие цивилизации Ближнего и Среднего Востока, Индостана и Китая также использовали жизненно важный металл.
Греческий автор Гомер называл этот металл «халкосом»; поэтому медный век называют эпохой энеолита. В греческой мифологии богиня любви Афродита, как говорят, вышла из моря недалеко от Кипра, глядя на свое отражение в медном зеркале. Некоторые историки считают, что это показывает, что металлургия является древнейшей профессией. В римских писаниях медь упоминается как «aes Cyprium», поскольку в то время большая часть металла поступала с Кипра.
В греческой мифологии богиня любви Афродита, как говорят, вышла из моря недалеко от Кипра, глядя на свое отражение в медном зеркале. Некоторые историки считают, что это показывает, что металлургия является древнейшей профессией. В римских писаниях медь упоминается как «aes Cyprium», поскольку в то время большая часть металла поступала с Кипра.
‘Oetzti’, 5000-летний мумифицированный человек, недавно обнаруженный высоко в Альпах на итальянско-австрийской границе, был найден со многими орудиями, включая превосходный медный топор с мышьяком. Похоже, что он, вероятно, сам был медником, поскольку в его волосах была высокая концентрация меди и мышьяка, которые, вероятно, не могли быть получены ни из какого другого источника.
Бронзовый век
До 3000 г. до н.э. было обнаружено, что добавление олова к меди дает бронзу, сплав, более твердый и прочный, чем медь. Некоторые из самых ранних известных изделий из бронзы происходят из раскопок в Шумере и имеют значительную древность. Сначала совместное плавление медных и оловянных руд могло быть либо случайным, либо результатом ранних экспериментов, направленных на выяснение того, какие виды горных пород можно плавить.
Сначала совместное плавление медных и оловянных руд могло быть либо случайным, либо результатом ранних экспериментов, направленных на выяснение того, какие виды горных пород можно плавить.
Значительное инженерное применение меди было найдено еще в 2750 г. до н.э., когда она использовалась в Абусире в Египте для водопровода. (Некоторые древние египетские медные водопроводные трубы сохранились до наших дней, что является замечательной демонстрацией долговечности металла.) Медь и бронза использовались для изготовления зеркал большинством средиземноморских цивилизаций периода бронзового века. Уничтожение Карфагена римлянами затмило события того времени в Северной Африке. Лишь совсем недавно появились свидетельства значительных инженерных навыков карфагенян, в том числе самое раннее известное использование зубчатых колес, отлитых из бронзы. Бронза использовалась во многих артефактах повседневной жизни римлян — столовых приборах, иглах, украшениях, сосудах, украшениях, монетах, ножах, бритвах, инструментах, музыкальных инструментах и военном оружии. Этот образец использования, как правило, повторялся везде, где вводилась плавка бронзы и меди, хотя обязательно в разных временных масштабах.
Этот образец использования, как правило, повторялся везде, где вводилась плавка бронзы и меди, хотя обязательно в разных временных масштабах.
Средние века и позднее
Изобретение книгопечатания увеличило спрос на медь из-за легкости, с которой медные листы можно было гравировать для использования в качестве печатных форм для точного воспроизведения иллюстраций и карт. В Германии рисунки игральных карт гравировали на меди еще в 1430 году. Медные пластины долгое время считались лучшим средством для гравировки карт. Первые известные карты, отпечатанные с медных пластин, — это два итальянских издания, датированные 1472 г. географом Птолемеем.
Затем
Медная или бронзовая проволока стала очень важным продуктом, имеющим жизненно важное значение для ткацкой промышленности. Использование меди для обшивки корпусов деревянных лодок было первоначально разработано для предотвращения нападения червей тередо на древесину в субтропических водах, но впоследствии было обнаружено, что покрытые медью корпуса также устойчивы к морскому биологическому обрастанию.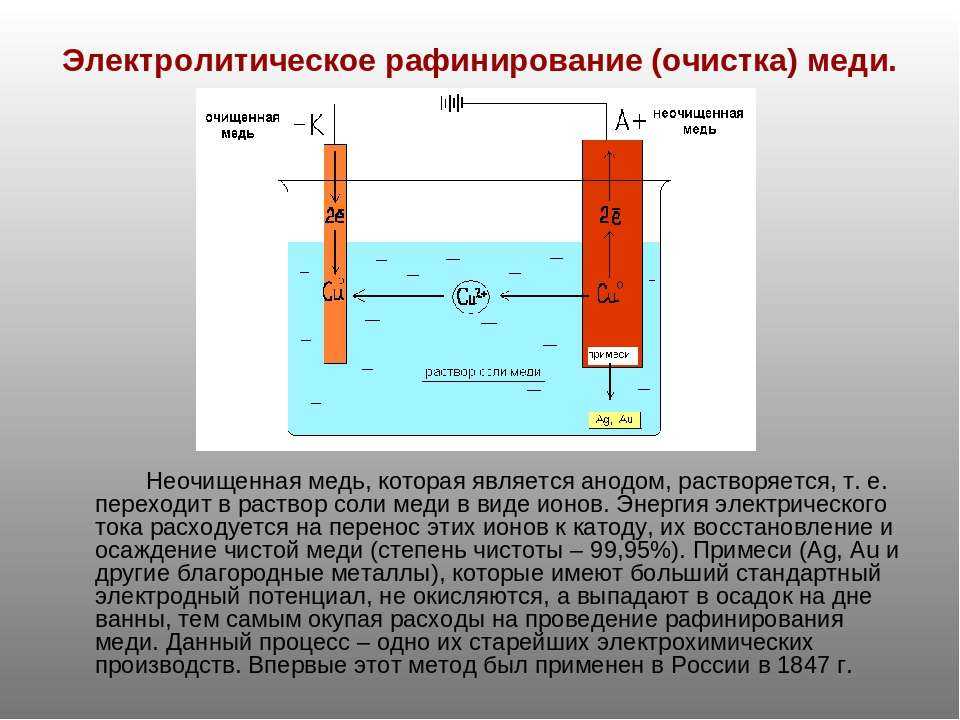 Это полезное свойство предотвращало сильное сопротивление, вызванное ростом водорослей, которое ограничивало скорость кораблей. (Сообщалось, что победа лорда Нельсона при Трафальгаре отчасти стала результатом скорости его облаченных в медь кораблей, которая позволила ему перехитрить своих противников.) В результате значительно увеличился спрос на медь.
Это полезное свойство предотвращало сильное сопротивление, вызванное ростом водорослей, которое ограничивало скорость кораблей. (Сообщалось, что победа лорда Нельсона при Трафальгаре отчасти стала результатом скорости его облаченных в медь кораблей, которая позволила ему перехитрить своих противников.) В результате значительно увеличился спрос на медь.
Рисунок 7 . Сравнение размеров медных и алюминиевых кабелей.
Тем не менее, наибольшее распространение в использовании меди произошло в результате открытия Майклом Фарадеем электромагнитной индукции в 1831 году и того, как этот эффект можно было использовать для производства электричества. Тот же принцип был использован для разработки электродвигателей. Электрическая лампа была изобретена сэром Джозефом Суоном в 1860 году и доведена до коммерческого дизайна Томасом Эдисоном в 1879 году. машиностроение. Медь обладает самой высокой тепло- и электропроводностью на единицу объема среди всех известных веществ, за исключением серебра, которое лишь немного превосходит ее в этом отношении. Поскольку проводимость меди зависит от ее чистоты, широко используется медь в ее нелегированной форме. Сегодня около половины производимой в мире меди приходится на электроэнергию.
Поскольку проводимость меди зависит от ее чистоты, широко используется медь в ее нелегированной форме. Сегодня около половины производимой в мире меди приходится на электроэнергию.
Горнодобывающая промышленность
Древнейшими способами извлечения породы из подземных шахт были кувалда и клин и не менее древняя техника поджига. В последнем случае огонь, устроенный против поверхности скалы, вызовет напряжения теплового расширения — скала либо раскрошится естественным образом, либо может быть разрушена закалкой водой. Через некоторое время после того, как исламский мир в 13 веке привез из Китая в Европу взрывчатые вещества, взрывчатые вещества были впервые использованы специально для добычи полезных ископаемых. Сегодня старые методы добычи были почти полностью заменены взрывными работами с использованием безопасных современных взрывчатых веществ и использованием мощного механического оборудования для резки, когда порода достаточно мягкая, чтобы заслуживать такую обработку.
Также в этом выпуске:
- Введение в медь: применение
- Знакомство с медью: типы меди
- Введение в медь: добыча и добыча
- Введение в медь: информационные бюллетени
- Phelps Dodge Morenci перевела все производство меди на добычу для выщелачивания
- Как гидрометаллургия и процесс SX/EW сделали медь «зеленым» металлом
- Введение в медь: горячие ссылки и дополнительная литература
2007 г.
|
2006 г.

 Чили также может похвастаться крупнейшим в мире (с точки зрения добычи) открытым медным рудником Escondida. Крупнейший медный рудник в Северной Америке (и крупнейший в мире рукотворный раскоп) — это рудник Бингем-Каньон недалеко от Солт-Лейк-Сити, штат Юта. Программа модернизации стоимостью 1,5 миллиарда долларов, завершенная в 1998 году, превратила Бингем-Каньон в производителя меди с самой низкой себестоимостью в Северной Америке, образец операционной эффективности и соблюдения экологических норм.
Чили также может похвастаться крупнейшим в мире (с точки зрения добычи) открытым медным рудником Escondida. Крупнейший медный рудник в Северной Америке (и крупнейший в мире рукотворный раскоп) — это рудник Бингем-Каньон недалеко от Солт-Лейк-Сити, штат Юта. Программа модернизации стоимостью 1,5 миллиарда долларов, завершенная в 1998 году, превратила Бингем-Каньон в производителя меди с самой низкой себестоимостью в Северной Америке, образец операционной эффективности и соблюдения экологических норм.