Презентация по химии "Сплавы"(9 класс). Таблица сплавов по химии
Сплавы . Химия 9 класс
Урок химии 9 класс
Тема урока «Сплавы»
Разработала учитель химии
МКОУ Гвазденская СОШ Гайворонская Т.М.

???
1. Какие вы знаете распространенные в быту и технике сплавы металлов?
2. Почему на практике почти не применяется чистое железо?
3. Чем вызвана необходимость создания разнообразных сплавов?

Сплав -
это гомогенная система, образованная сплавлением (спеканием) двух или более металлов, а также металлов и неметаллов (порошковая металлургия)

Сплавы отличаются от чистых металлов
1. Структурой
2. Более низкой температурой плавлениям
3. Более высокой прочностью и твердостью
4. Более меньшей электро- и теплопроводностью
5. Высокой коррозийной стойкостью

Классификация сплавов
1. Сплавляемые металлы взаимодействуют между собой, образуя интерметаллиды
Na 2 Pb, AuZn, MgPb
2. Жидкие металлы могут смешиваться в любых количественных соотношениях и при остывании образуют сплавы – твердые растворы (Ag –Cu Cu –Ni Mn – Fe )
3 . Механические смеси
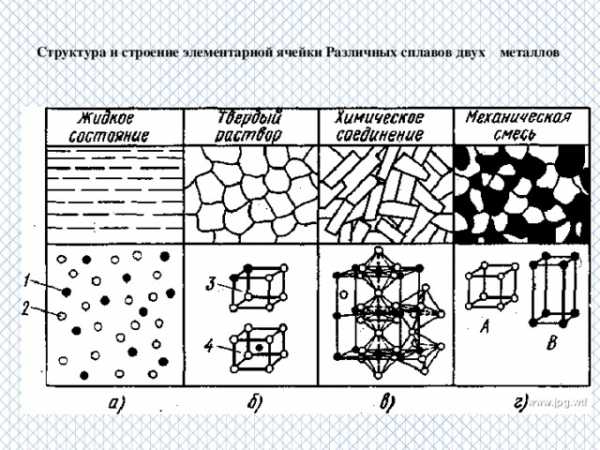
Структура и строение элементарной ячейки Различных сплавов двух металлов

Твердые растворы замещения
Условия образования
Совпадение типов кристаллических решеток
Близкие размеры радиусов атомов металлов
Например,
1. Мельхиор Cu – Ni
2. Бронза Cu – Sn
3. Дюралюминий Al – Cu, Mg, Mn, Ni
4. Латунь Cu – Zn

Изделия из мельхиора

Изделия из бронзы

Изделия из латуни

Изделия из дюралюминия

Твердые растворы внедрения
Условия образования
Значительное различие в радиусах атомов металлов (более 12%)
Например, Fe - C, Fe–B

Черные металлы – чугун и сталь
Чугун - сплав железа с углеродом (более 2%0 и примесями Mn, Si, S, P. ; он тверд и хрупок

Сталь -
Сталь - сплав железа, содержащий 1.7% С, примеси Mn, Si, S, P (добавки различных металлов, увеличивающих прочность, твердость сплава и т.д.

Механическая смесь (припой, «третники»)
При охлаждении смеси расплавленных металлов образуется сплав, состоящий из мельчайших кристалликов каждого металла
Например, Pb- Sn, Pb - Ag

Русские ученые - металлурги
Д.К. Чернов
П.П. Аносов
И.П. Бардин
1839-1921
1799-1851
1883-1960

Домашнее задание
§ 49, упр. 3, с. 223 по учебнику Н.Е. Кузнецовой
§ 38, упр.13-15, задача №2, с. 112 по учебнику Г.Е. Рудзитиса
§ 7, задача №2 , с. 34
multiurok.ru
Применение металлов и их сплавов — урок. Химия, 8–9 класс.
О том, что свойства металлов меняются при их сплавлении, стало известно ещё в древности. \(5\) тысяч лет тому назад наши предки научились делать бронзу — сплав олова с медью. Бронза по твёрдости превосходит оба металла, входящие в её состав.
Свойства чистых металлов, как правило, не соответствуют необходимым требованиям, поэтому практически во всех сферах человеческой деятельности используют не чистые металлы, а их сплавы.
Сплав — это материал, который образуется в результате затвердения расплава двух или нескольких отдельных веществ.
В состав сплавов кроме металлов могут входить также неметаллы, например, такие как углерод или кремний.
Добавляя в определённом количестве примеси других металлов и неметаллов, можно получить многие тысячи материалов с самыми разнообразными свойствами, в том числе и такими, каких нет ни у одного из составляющих сплав элементов.
Сплав по сравнению с исходным металлом может быть:
- механически прочнее и твёрже,
- со значительно более высокой или низкой температурой плавления,
- устойчивее к коррозии,
- устойчивее к высоким температурам,
- практически не менять своих размеров при нагревании или охлаждении и т. д.
Например, чистое железо — сравнительно мягкий металл. При добавлении в железо углерода твёрдость его существенно возрастает. По количеству углерода, а следовательно, и по твёрдости, различают сталь (содержание углерода менее \(2\) % по массе), чугун (\(С\) — более \(2\) %). Но не только углерод изменяет свойства стали. Добавленный в сталь хром делает её нержавеющей, вольфрам делает сталь намного более твёрдой, добавка марганца делает сплав износостойким, а ванадия — прочным.
Применение сплавов в качестве конструкционных материалов
Сплавы, используемые для изготовления различных конструкций, должны быть прочными и легко обрабатываемыми.
В строительстве и в машиностроении наиболее широко используются сплавы железа и алюминия.
Такие сплавы железа, как стали, отличаются высокой прочностью и твёрдостью. Их можно ковать, прессовать, сваривать.
Чугуны используют для изготовления массивных и очень прочных деталей. Например, раньше из чугуна отливали радиаторы центрального отопления, канализационные трубы, до сих пор изготавливают котлы, перила и опоры мостов. Изделия из чугуна изготавливаются с применением литья.
Сплавы алюминия, используемые в конструкциях, наряду с прочностью должны отличаться лёгкостью. Дюралюминий, силумин — сплавы алюминия, они незаменимы в самолёто-, вагоно- и кораблестроении.
В некоторых узлах самолётов используются сплавы магния, очень лёгкие и жароустойчивые.
В ракетостроении применяют лёгкие и термостойкие сплавы на основе титана.
Для улучшения ударопрочности, коррозионной стойкости, износоустойчивости сплавы легируют — вводят специальные добавки. Добавка марганца делает сталь ударопрочной. Чтобы получить нержавеющую сталь, в состав сплава вводят хром.
| Конструкция из стальных балок | Радиаторы центрального отопления | Ажурные перила, отлитые из чугуна |
Инструментальные сплавы
Инструментальные сплавы предназначены для изготовления режущих инструментов, штампов и деталей точных механизмов. Такие сплавы должны быть износостойкими и прочными, причём при разогревании их прочность не должна существенно уменьшаться. Таким требованиям отвечают, например, нержавеющие стали, которые прошли специальную обработку (закалку).
Добавление к сплавам веществ, улучшающих их свойства, называют легированием.
Для придания необходимых свойств инструментальные стали, как правило, легируют вольфрамом, ванадием или хромом.
Применение сплавов в электротехнической промышленности, электронике и приборостроении
Сплавы служат незаменимым материалом при изготовлении особо чувствительных и высокоточных приборов, различного рода датчиков и преобразователей энергии.
Например, на изготовление сердечников трансформаторов и деталей реле идёт сплав никеля. Отдельные детали электромоторов изготавливаются из сплавов кобальта.
Сплав никеля с хромом — нихром, отличающийся высоким сопротивлением — используется для изготовления нагревательных элементов печей и бытовых электроприборов.
Из сплавов меди в электротехнической промышленности и в приборостроении наиболее широкое применение находят латуни и бронзы.
Латуни незаменимы при изготовлении приборов, деталью которых являются запорные краны. Такие приборы используются в сетях подачи газа и воды.
Бронзы идут на изготовление пружин и пружинящих контактов.
| Нагревательные элементы бытовых электроприборов | Запорные краны для водопроводов и газопроводов | Пружинящие контакты электрических розеток |
Применение легкоплавких сплавов
Главным востребованным свойством легкоплавких сплавов является заданная низкая температура плавления. Это свойство, в частности, используется для пайки микросхем. Кроме того, эти сплавы должны иметь определённую плотность, прочность на разрыв, химическую инертность, теплопроводность.
Легкоплавкие сплавы производят из висмута, свинца, кадмия, олова и других металлов. Такие сплавы используют в термодатчиках, термометрах, пожарной сигнализации, например, сплав Вуда. А также в литейном деле для производства выплавляемых моделей, для фиксации костей и протезирования в медицине.
Сплав натрия с калием (температура плавления \(–\)\(12,5\) °С) используется как теплоноситель для охлаждения ядерных реакторов.
| Припой (сплав для паяния) имеет невысокую температуру плавления | Легкоплавкие сплавы используются в литейном деле | Легкоплавкие сплавы незаменимы в датчиках пожарной сигнализации |
Применение сплавов в ювелирном деле
Применение в чистом виде драгоценных металлов в ювелирном деле не всегда оправдано и целесообразно из-за их дороговизны, физических и химических особенностей.
Для придания ювелирным изделиям из золота большей твёрдости и износостойкости используются сплавы с другими металлами.
Самая лучшая добавка — это серебро (понижает температуру плавления) и медь (повышает твёрдость). Чистое золото используют очень редко, так как оно слишком мягкое, легко деформируется и царапается.
Из сплавов золота с \(10–30\) % других благородных металлов (платины или палладия) изготавливают форсунки лабораторных приборов, а из сплава с \(25–30\) % серебра — ювелирные изделия и электрические контакты.
| Ювелирные изделия из сплавов золота | Позолоченные электрические контакты |
Сплавы в искусстве
Оловянная бронза (сплав меди с оловом) — один из первых освоенных человеком сплавов металлов. Она обладает большей, по сравнению с чистой медью, твёрдостью, прочностью и более легкоплавка. Бронзы успешно применяют для получения сложных по конфигурации отливок, включая художественное литьё. Классической маркой бронзы является колокольная бронза.Одно из новых направлений в искусстве — производство художественных литых изделий из чугуна. Литые изделия из чугуна существенно превосходят по качеству кованые изделия.
Чугун — металл гораздо более хрупкий и не такой ковкий, как сталь. Но даже из такого, казалось бы, грубого материала можно получать настоящие произведения литейного искусства способом литья, например, такие как литые лестницы или решётки на окна. Такие изделия подвержены лишь поверхностной коррозии и не требуют тщательного ухода.
Бронзовая скульптура
| Колокола отливают из специального сорта бронзы | Чугунная лестница. Практично и очень красиво |
www.yaklass.ru
МЕТАЛЛЫ И СПЛАВЫ Химический состав металлов и сплавов (таблицы)
Химический состав металлов (сплавов), испытанных на коррозию и указанных в таблицах химической стойкости (табл. Э—18), приведен в табл. 2. [c.367]Глава первая. Химический состав металлов и сплавов (таблицы). ... 8 [c.352]
Основное содержание справочника составляют таблицы коррозионной стойкости. В первой графе таблиц приводится наименование материала, процентный состав его (по массе) и марка отечественного материала, близкого к нему по составу (указывается в скобках). Если материал выпускается промышленностью, то указывается только его марка, а состав определяется соответствующими ГОСТами. Условия предварительной термической или механической обработки материалов, если они известны, указываются в примечании или рядом с маркой материала. Материалы располагаются в следующем порядке. Вначале идут металлические материалы, которые начинаются с железа и железных сплавов как наиболее широко применяющиеся в практике. Затем следуют в алфавитном порядке наиболее распространенные металлы и сплавы алюминий и его сплавы, магний и его сплавы, медь и ее сплавы, никель и никелевые сплавы, титан и титановые сплавы. После этого в алфавитном порядке размещаются другие металлы и их сплавы. В последней части таблиц приводится химическая стойкость неметаллических материалов (по алфавиту). Скорость коррозии металлов и сплавов характеризуется потерей массы ( , г/м .ч) или глубинным показателем коррозии (/г , мм/год). Длительность коррозионных испытаний приводится в примечаниях или в отдельном столбце таблицы. Продолжительность испытания оказывает влияние на скорость коррозии (в частности, на среднюю скорость коррозии). Как правило, при более длительных испытаниях средняя скорость коррозии становится меньше. Большое влияние на скорость коррозии могут оказать перемешивание среды и примеси. В таблицах, по возможности, отмечены эти особенности. [c.4]
Все сказанное выше касается металлов и сплавов, химический состав которых приведен в таблицах Химический состав металлов и сплавов . [c.8]
Справочник состоит из трех глав. В первой главе приводится химический состав металлов и сплавов. Порядковые номера этих материалов приводятся затем в таблицах коррозионной стойкости, помещенных ва второй главе справочника, против названия металла или сплава. [c.3]
Гегнером и Вильсоном [55] непосредственно в производственных условиях было проведено исследование коррозионной стойкости титана и некоторых других металлов в химических средах, часто встречающихся в технологических процессах заводов хлорнощелочной группы. Химический состав исследованных сплавов приведен в табл. 17 титан, цирконий, тантал и алюминий были технической чистоты. Испытания проводились непосредственно в химических аппаратах, сосудах, трубах и на другом оборудовании. Результаты испытаний приведены в табл. 18 и 19 (ввиду того, что они взяты из одной работы, номера испытаний идут на этих таблицах последовательно). [c.32]
Каждому материалу в таблицах Химический состав металлов и сплавов присвоен порядковый номер, который затем переходит как основной номер в первую графу таблиц Коррозионная стойкость металлов и сплавов . В этих таблицах также указываются номер и наименование металла или сплава, характеристика агрессивной среды и величина скорости коррозии материала. [c.9]
Собственно справочный материал оригинален и не дублирует имеющиеся в СССР справочники. Бесспорное достоинство книги в том, что авторы собрали и обобщили данные по химическому составу металлов и сплавов, широко применяемых в технике. Несомненный интерес представляют Сравнительные таблицы составов различных металлов и сплавов согласно стандартам стран-изготовителей , которые позволяют установить состав сплавов, изготовленных по стандартам разных стран. В книге дана также уникальная по объему сводка торговых наименований металлических и неметаллических материалов и краткое описание их состава. В условиях расширяющейся международной торговли эти материалы представляют большой самостоятельный интерес, так как на их основе можно установить соответствие между торговыми марками материалов, выпускаемых в разных странах. Это поможет советским специалистам определить условия эксплуатации импортного оборудования. [c.6]
Таблица построена по следующему принципу. Материалы в таблице подразделены на две группы металлы и сплавы и неметаллические материалы. Их химический состав и свойства приведены в соответствующих таблицах (см. гл. 2 и 3). [c.262]
В последующих шести графах указывается, насколько сильно уменьшается или усиливается коррозия рассматриваемого металла под влиянием контак-тируемых с ним металлов и какие именно металлы и сплавы вызывают коррозию такого порядка. Химический состав этих металлов можно найти по проставленным в скобках номерам в таблицах главы I справочника.,. . [c.257]
Состав металлов и сплавов, приведенных в таблицах химической [c.367]
Технические металлы и сплавы, исследованные электрохимически и включенные в таблицы коррозионной стойкости, часто считаются гомогенными материалами. Это, возможно, правильно для чистых алюминия, меди, железа и т. д., но абсолютно неприемлемо для стали, латуни, алюминиевых сплавов и других структурных материалов. Для полной характеристики таких материалов должен быть известен не только их состав, но также металлургическая история — пластическая обработка в горячем или холодном состоянии, термообработка и т. д. Это относится и к нержавеющим сталям, которые образуют несколько групп и подгрупп, обладающих каждая своими специфическими металлургическими, физическими и химическими свойствами. [c.22]
Чем дальше отстоят элементы друг от друга в таблице элементов, вплоть до элементов, обладающих неметаллическими свойствами, тем меньше их взаимная растворимость. В этом случае образуются механические смеси твердых растворов, например сплав свинца с сурьмой, и, наконец, химические соединения разнообразных типов. Сначала эти химические соединения сохраняют металлические свойства, хотя и отличающиеся от свойств компонентов Mg d), имеют металлический блеск, электропроводность. Затем металлический характер соединений постепенно ослабевает (МдзВ ), уступая место солеобразным соединениям (MgS) — соединениям металла с неметаллами. Можно отметить некоторые общие закономерности в свойствах сплавов. Температура плавления сплава обычно ниже температуры плавления входящих в его состав металлов. Твердость сплавов в большинстве случаев выше твердости металлов. [c.397]
Предварительная обработка металлических поверхносте перед нанесением твердых смазочных покрытий способствует увеличению срока службы покрытий. Известно также, что при холодной вытяжке титановых сплавов предварительная обработка поверхности снижает усилие вытяжки. Для модифицирования поверхности металла можно применять пескоструйную обработку, кислотное травление, нанесение химических покрытий и механическую обработку. Возможны разнообразные варианты каждого из указанных способов обработки. Характер пескоструйной обработки зависит от природы распыляемого зернистого материала и распыляющего агента, давления распыления, расстояния от сопла пескоструйного аппарата до поверхности металла, диаметра сопла, угла распыла и длительности обработки. Состав, длительность обработки, температура и условия промывки являются важнейшими факторами 1фи нанесении химических покрытий такого типа, как фосфаты цинка, железа, марганца и др. При сопоставлении экспериментальных данных об износостойкости или сроке службы различных твердых смазок всегда необходимо учитывать вид предварительной обработки поверхностей трения перед нанесением ка них смазочных покрытий. Так, в табл. 38 приведены данные испытаний на машине трения Фалекс. Как известно, в машине этого типа стальные валики (А181-302) вращаются со скоростью 290 об/мин, будучи зажаты с силой 450 кГ между двумя У-об-разными плашками из стали А151-С1137. Твердый смазочный слой, наносившийся на испытуемые валики после их предвар -Таблица 38 [c.299]
При изучении формы и ширины рентгеновских Ках,2- и КРх-липий в химических соединениях было показано, что эти линии у атомов переходных элементов асимметричны. Это противоречит тому, чего следовало бы ожидать теоретически и что наблюдается у большинства элементов таблицы Менделеева. Эксперименты показывают, что изменение валентного состояния атомов переходных элементов в соединении или их вхождение в состав дефектной решетки, в которой, повидимому, различные группы атомов могут находиться в энергетически неэквивалентных состояниях, приводит к изменению формы рентгеновских Ка .з-ли-ний и, в частности, к изменению их индекса асимметрии. В связи с этим представляет большой интерес экспериментально твердо установленный факт асимметричности Ках,2-линий в чистых металлах и в сплавах переходных элементов. Величина индекса асимметрии К ,2-линий в металлах связана с порядковым номером переходного элемента. В пределах этой группы элементов она достигает максимальной величины у железа. Если для объяснения асимметричной формы рентгеновскихКа1,2-линий атомов переходных элементов в соединениях принять выдвинутое в настоящей работе представление об их сложной структуре, то применительно к металлам оно приводит к выводу [c.100]
chem21.info
Химические сплавы - Популярная химия
Известно, что в чистом виде металлы используются редко. Чаще всего нас окружают различные соединения металлов и их сплавы. Сплавы – это вещества, состоящие из химических элементов, один из которых является металлом.
Получение сплавов

Очень давно было замечено, что если смешать расплавленные металлы и остудить полученную смесь, то получается вещество, свойства которого отличаются от свойств каждого из металлов. Так, если в расплавленную медь добавить алюминий, то в результате химической реакции получается новое соединение с формулой АlСи.
Сплавы получают различными способами. Если смешивают расплавленные компоненты, а затем производят кристаллизацию полученного расплава, то получают литой сплав. Кристаллизация – это процесс перехода из жидкого состояния в твердое. При этом образуется соединение с кристаллической структурой. А если смешивают порошки компонентов, а затем спекают смесь при высокой температуре, то получают сплав, который называется порошковым сплавом. Для улучшения свойств в сплавы вводятся элементы, которые называются легирующими.
Виды сплавов
В состав сплавов могут входить только металлы или соединения металлов с неметаллами. Свое название сплав обычно получает от названия элемента, который содержится в сплаве в самом большом количестве и составляет основу сплава. Так, если основой сплава является железо, то сплавы называются чёрными. А если основа сплавов - цветные металлы, то и сплавы называются цветными. Бывают ещё сплавы редких металлов и сплавы радиоактивных металлов.
Черные сплавы

В сплавах могут быть два и более компонентов.
Наиболее известные чёрные сплавы – сталь и чугун. Оба эти сплава являются смесью железа и углерода. Но чугун содержит углерода намного больше, чем сталь. Кроме углерода, в чугун входят сера, фосфор, марганец и кремний. В сталь также добавляются эти элементы, но в гораздо меньших количествах. Чугун – хрупкий материал. Его применяют там, где не требуется ковка. А вот сталь не только прочный, но и пластичный материал. Поэтому она широко применяется в промышленности в металлических конструкциях, механизмах, деталях, для изготовления режущих инструментов и т. д. В нашем доме нас окружают изделия из нержавеющей стали: ножи, вилки, ложки, ножницы, тёрки, кастрюли.
Цветные сплавы

Самые известные сплавы меди – бронза и латунь.
Сплав меди с оловом называют бронзой. В III тысячелетии до н.э из меди изготавливались орудия труда, так как залежи меди в то время были огромны. Выяснилось, что если медь соединить с оловом, то получается вещество, более поддающееся литью. Так впервые была получена бронза. Следующее тысячелетие назвали «бронзовым веком». В XV в. из бронзы начали отливать пушки. В наше время бронза применяется в машиностроение для изготовления различных деталей.
Латунь – сплав меди с цинком. Используется в производстве техники, автомобилестроении, в химической промышленности. Интересно, что латунь внешне схожа с золотом. Поэтому до XIX века ее часто выдавали за золото.
Соединение меди с алюминием называют алюминиевой бронзой. Алюминиевая бронза - очень пластичный материал.
Мельхиор — сплав меди и никеля. Используется для изготовления столовых приборов и художественных изделий.
Известный алюминиевый сплав дюралюминий – соединение алюминия с медью, магнием и марганцем. Применяется в авиационной промышленности и авиастроении.
Магниевые, титановые, берилиевые сплавы также находят свое применение в промышленности и медицине.
Металлы и сплавы играют очень важную роль в различных видах жизнедеятельности человека. Невозможно перечислить все сферы, в которых металлы и их сплавы находят применение.

ximik.biz
Доклад по химии Тема: “Сплавы”
МОСКОВСКИЙ ДЕПАРТАМЕНТ ОБРАЗОВАНИЯ
ШКОЛА — ЛАБОРАТОРИЯ № 799
Доклад по химии
Тема: “Сплавы”
Ученика Кудашева Алексея
Окружающие нас металлические предметы редко состоят из чистых металлов. Только алюминиевые кастрюли или медная проволка имеют чистоту около 99,9%. В большинстве же других случаев люди имеют дело со сплавами. Так, различные виды железа и стали содержат наряду с металлическими добавками незначительные количества углерода, которые оказывают решающее влияние на механическое и термическое поведение сплавов. Все сплавы имеют специльную маркировку, т.к. сплавы с одним названием (например, латунь) могут иметь разные массовые доли других металлов.
Для изготовления сплавов применяют различные металлы. Самое большое значение среди всех сплавов имеют стали различных составов. Простые конструкционные стали состоят из железа относительно высокой чистоты с небольшими (0,07—0,5%) добавками углерода. Так, чугун, получаемый в доменной печи, содержит около 10% других металов, из них примерно 3% составляет углерод, а остальные — кремний, марганец, сера и фосфор. А легированные стали получают, добавляя к железу кремний, медь, марганец, никель, хром, вольфрам, ванадий и молибден.
Никель наряду с хромом является важнейшим компонентом многих сплавов. Он придает сталям высокую химическую стойкость и механическую прочность. Так, известная нержавеющая сталь содержит в среднем 18% хрома и 8% никеля. Для производства химической аппаратуры, сопел самолетов, космических ракет и спутников требуются сплавы, которые устойчивы при температурах выше 1000 °С, то есть не разрушаются кислородом и горючими газами и обладают при этом прочностью лучших сталей. Этим условиям удовлетворяют сплавы с высоким содержанием никеля. Большую группу составляют медно-никелевые сплавы.
Сплав меди, известный с древнейших времен, – бронза содержит 4-30% олова (обычно 8-10%). До наших дней сохранились изделия из бронзы мастеров Древнего Египта, Греции, Китая. Из бронзы отливали в средние века орудия и многие другие изделия. Знаменитые Царь-пушка и Царь-колокол в Московском Кремле также отлиты из сплава меди с оловом. В настоящее время в бронзах олово часто заменяют другими металлами, что приводит к изменению их свойств. Алюминиевые бронзы, которые содержат 5-10% алюминия, обладают повышенной прочностью. Из такой бронзы чеканят медные монеты. Очень прочные, твердые и упругие бериллиевые бронзы содержат примерно 2% бериллия. Пружины, изготовленные из бериллиевой бронзы, практически вечны. Широкое применение в народном хозяйстве нашли бронзы, изготовленные на основе других металлов: свинца, марганца, сурьмы, железа и кремния.
Сплав мельхиор содержит от 18 до 33% никеля (остальное медь). Он имеет красивый внешний вид. Из мельхиора изготавливают посуду и украшения, чеканят монеты («серебро»). Похожий на мельхиор сплав -нейзильбер -содержит, кроме 15% никеля, до 20% цинка. Этот сплав используют для изготовления художественных изделий, медицинского инструмента. Медно-никелевые сплавы константан (40% никеля) и манганин (сплав меди, никеля и марганца) обладают очень высоким электрическим сопротивлением. Их используют в производстве электроизмерительных приборов. Характерная особенность всех медно-никелевых сплавов – их высокая стойкость к процессам коррозии – они почти не подвергаются разрушению даже в морской воде. Сплавы меди с цинком с содержанием цинка до 50% носят название латунь. Латунь "60" содержит, например, 60 весовых частей меди и 40 весовых частей цинка. Для литья цинка под давлением применяют сплав, содержащий около 94% цинка, 4% алюминия и 2% меди. Это дешевые сплавы, обладают хорошими механическими свойствами, легко обрабатываются. Латуни благодаря своим качествам нашли широкое применение в машиностроении, химической промышленности, в производстве бытовых товаров. Для придания латуням особых свойств в них часто добавляют алюминий, никель, кремний, марганец и другие металлы. Из латуней изготавливают трубы для радиаторов автомашин, трубопроводы, патронные гильзы, памятные медали, а также части технологических аппаратов для получения различных веществ.
По следующим рецептам можно получить легкоплавкие сплавы. Сплав Ньютона: 31 массовая часть свинца, 19 частей олова и 50 частей висмута. Температура плавления 95 °С. Сплав Вуда: 25 частей свинца, 12,5 частей олова, 50 частей висмута и 12,5 частей кадмия. Температура плавления 60 °С. Ложка из такого сплава расплавится, если ею помешать горячий кофе. Раньше это демонстрировали в качестве шутливого опыта. Однако перемешанный таким образом напиток ядовит из-за солей свинца и висмута!
Очень давно было замечено, что если смешать расплавленные металлы и остудить полученную смесь, то получается вещество, свойства которого отличаются от свойств каждого из металлов. Так, если в расплавленную медь добавить алюминий, то в результате химической реакции получается новое соединение с формулой АlСи.
Сплавы получают различными способами. Если смешивают расплавленные компоненты, а затем производят кристаллизацию полученного расплава, то получают литой сплав. Кристаллизация – это процесс перехода из жидкого состояния в твердое. При этом образуется соединение с кристаллической структурой. А если смешивают порошки компонентов, а затем спекают смесь при высокой температуре, то получают сплав, который называется порошковым сплавом. Для улучшения свойств в сплавы вводятся элементы, которые называются легирующими.
Виды сплавов
В состав сплавов могут входить только металлы или соединения металлов с неметаллами. Свое название сплав обычно получает от названия элемента, который содержится в сплаве в самом большом количестве и составляет основу сплава. Так, если основой сплава является железо, то сплавы называются чёрными. А если основа сплавов – цветные металлы, то и сплавы называются цветными. Бывают ещё сплавы редких металлов и сплавы радиоактивных металлов.
ЧЕРНЫЕ СПЛАВЫ
В сплавах могут быть два и более компонентов.
Наиболее известные чёрные сплавы – сталь и чугун. Оба эти сплава являются смесью железа и углерода. Но чугун содержит углерода намного больше, чем сталь. Кроме углерода, в чугун входят сера, фосфор, марганец и кремний. В сталь также добавляются эти элементы, но в гораздо меньших количествах. Чугун – хрупкий материал. Его применяют там, где не требуется ковка. А вот сталь не только прочный, но и пластичный материал. Поэтому она широко применяется в промышленности в металлических конструкциях, механизмах, деталях, для изготовления режущих инструментов и т. д. В нашем доме нас окружают изделия из нержавеющей стали: ножи, вилки, ложки, ножницы, тёрки, кастрюли.
ЦВЕТНЫЕ СПЛАВЫ

Самые известные сплавы меди – бронза и латунь.
Сплав меди с оловом называют бронзой. В III тысячелетии до н.э из меди изготавливались орудия труда, так как залежи меди в то время были огромны. Выяснилось, что если медь соединить с оловом, то получается вещество, более поддающееся литью. Так впервые была получена бронза. Следующее тысячелетие назвали «бронзовым веком». В XV в. из бронзы начали отливать пушки. В наше время бронза применяется в машиностроение для изготовления различных деталей.
Латунь – сплав меди с цинком. Используется в производстве техники, автомобилестроении, в химической промышленности. Интересно, что латунь внешне схожа с золотом. Поэтому до XIX века ее часто выдавали за золото.
Соединение меди с алюминием называют алюминиевой бронзой. Алюминиевая бронза – очень пластичный материал.
Мельхиор — сплав меди и никеля. Используется для изготовления столовых приборов и художественных изделий.
Известный алюминиевый сплав дюралюминий – соединение алюминия с медью, магнием и марганцем. Применяется в авиационной промышленности и авиастроении.
Магниевые, титановые, берилиевые сплавы также находят свое применение в промышленности и медицине.
Металлы и сплавы играют очень важную роль в различных видах жизнедеятельности человека. Невозможно перечислить все сферы, в которых металлы и их сплавы находят применение.
kursak.net
Коллекция металлов Таблица псхэ. Оборудование согласно инструкции Химические реактивы Таблица растворимости. Металлы и сплавы
Химия 8класс| Темы | Оборудование |
| 1.Ведение (6часов) | Изделия из стекла и алюминия. Модели молекул. Правила техники безопасности труда в кабинете химии. Запрещается! Правила техники безопасности труда в кабинете химии. Осторожно! |
| 2.Атомы химических элементов (10 часов) | Модели атомов. Таблица ПСХЭ Химические знаки |
| 3. Простые вещества (7час) | Коллекция металлов Таблица ПСХЭ. Химические соединения количеством вещества 1 моль. |
| 4.Соединения химических элементов (12 часов) | Образцы оксидов. Таблицы: Кислоты, оксиды, основания, соли. Таблица растворимости, Кристаллические решетки Таблица ПСХЭ Химические реактивы Изменение максимальных степеней окисления химических элементов Бинарные соединения. Номенклатура солей. Названия кислот |
| 5.Практикум 1. «Простейшие операции с веществами» | Оборудование согласно инструкции Спиртовка Химические реактивы Растворы и смеси |
| 6.Растворение. Растворы (15час) | Таблица ПСХЭ. Таблицы: Кислоты, оксиды, основания, соли. Таблица растворимости. Химические реактивы Растворы и смеси. Взвешивание. Приготовление растворов. Фильтрование |
| 7. Практикум 2 «Свойства растворов электролитов» | Оборудование согласно инструкции Химические реактивы Таблица растворимости. |
Химия 9класс
| Темы | Оборудование |
| Повторение основных вопросов курса 8 класса (6час) | Образцы оксидов. Таблицы: Кислоты, оксиды, основания, соли. Таблица растворимости, Кристаллические решетки Таблица ПСХЭ Химические реактивы |
| 1.Металлы (15час) | Коллекция металлов Таблица ПСХЭ. Оборудование согласно инструкции Химические реактивы Таблица растворимости. Металлы и сплавы |
| 2.Практикум 1.(3час) Свойства металлов и их соединений | Оборудование согласно инструкции Химические реактивы |
| 3.Неметаллы (23час) | Образцы соединений серы Химические реактивы Таблица растворимости. |
| 4.Практикум 2 (3часа) Свойства неметаллов и их соединений | Оборудование согласно инструкции Химические реактивы |
| 5.Органические соединения (10 час) | Модели молекул органических веществ. Образцы изделий из пластмассы и каучука. Химические реактивы |
| 6. Обобщение знаний по химии за курс школы (6 час) | Таблица ПСХЭ. Таблицы: Кислоты, оксиды, основания, соли. Таблица растворимости. Кристаллические решетки |
Химия 10класс
| Темы | Оборудование |
| 1.Теория строения органических соединений (2час) | Модели молекул органических веществ. |
| 2.Углеводороды (8час) | Модели молекул органических веществ. Таблицы: Номенклатура органических соединений. Предельные углеводороды Непредельные углеводороды |
| 3.Кислородосодержащие органические соединения (10час) | Таблицы: Номенклатура органических соединений. Функциональные производные углеводородов. |
| 4.Азотосодержащие органические соединения (7 час) | Первичная структура белка. Вторичная структура белка Третичная структура белка. Четверичная структура белка Денатурация белков. Гетероциклы с атомом азота Принцип комплементарности. Нуклеиновые кислоты |
| 5.Биологически активные вещества (4ч ) | Таблица «Витамины» |
| 6.Искусственные и синтетические органические соединения (4час) | Коллекция пластмасс и волокон и изделий из них Набор хлопок. Набор шелк |
Химия 11 класс
| Темы | Оборудование |
| 1.Строение атома и периодический закон (3час) | Таблица ПСХЭ. |
| 2.Строение атома (14час) | Таблица ПСХЭ. Кристаллические решетки. Строение атома Электронная орбиталь. Модели атомов некоторых элементов |
| 3.Химические реакции (8час) | Химические реактивы.Таблицы: Физические явления и химические реакции. Закон сохранения массы веществ. Классификация химических реакций. Тепловой эффект химической реакции. Окислительно-восстановительные реакции |
| 4.Вещества и их свойства (10час) | Коллекция металлов, неметаллов. Таблица ПСХЭ. Химические реактивы. Образцы кислот, солей, оснований. |
Таблицы по химии
1.Химические знаки
2.Распространенность химических элементов в оболочках земли
3.Масса и объём 1 моля газообразных веществ
4.Кислород в природе. Круговорот О2 в природе
5.Кислотно-основные свойства элементов группы А
6.Строение и свойство пламени свечи
7.Приготовление растворов
8.Растворы и смеси (дисперсные системы)
9.Генетическая связь
10.Атомные радиусы элементов 1-4 пер.
11.Форма и перекрывание электронных облаков
12.Ковалентная связь
13.Ионная связь
14.Соотношение между видами химических связей
15.Окислительно-восстановительный процесс
16.Относительная электроотрицательность элементов группы А периодической системы.
17.Типы кристаллических решёток
18.Изменение максимальных степеней окисления химических элементов
19.Названия кислотХимические реакции1.Физические явления и химические реакции
2.Закон сохранения массы веществ
3.Классификация химических реакций
4.Тепловой эффект химической реакции
5.Окислительно-восстановительные реакции
6.Электролиз
7.Генетическая связь классов неорганических веществ
8.Генетическая связь классов органических веществСтроение веществ
1.Строение атома
2.Элетронная орбиталь
3.Модели атомов некоторых элементов
4.Кристаллы
5.Химическая связь
6.Валентность
7.Степень окисления
8.Изомерия
9.Изомерия 2
10.Гомология
Номенклатура
1.Бинарные соединения
2.Номенклатура солей
3.Номенклатура органических соединений
4.Предельные углеводороды
5.Непредельные углеводороды
6.Функциальные производные углеводороды Белки и нуклеиновые кислоты1.Первичная структура белка
2.Вторичная структура белка
3.Третичная структура белка
4.Четверичная структура белка
5.Денатурация белков
6.Гетероциклы с атомом азота
7.Принцип комплементарности
8.Нуклеиновые кислотыХимия клетки
1.Белки. Ферменты
2.Нуклеиновые кислоты
3.АТФ
Лабораторное оборудование5.Спиртовка
6.Газовая горелка
7.Электронагреватели
8.Нагревание
9.Приёмы обращения с лабораторным штативом
10.Получение и собирание газов
11.Обращение с твёрдыми веществами
12.Обращение с жидкими веществами
13.Взвешивание
14.Приготовление растворов
15.Фильтрование
16.Перегонка
17.Правила техники безопасности труда в кабинете химии. Запрещается!
19.Правила техники безопасности труда в кабинете химии. Осторожно!
Модели
1.Модели кристаллических решеток
2. Модели молекул органических веществ
УМК
1.Программа О.С.Габриеляна по химии 8-11 классы М. Дрофа 2013г
2. Учебник О.С.Габриеляна химия 8 класс М. Дрофа 2008г
9класс М. Дрофа 2009г
10класс М. Дрофа 2008г
11 класс М. Дрофа 2010г
3.Методическая литература:
1.Поурочные разработки по химии 11класс Москва «Вако» 2011
2.Поурочные планы по учебнику О.С.Габриеляна 10класс М. Дрофа 2007
3. Поурочные разработки по химии 9 класс Москва «Вако» 2008
4. Поурочные разработки по химии 8 класс Москва «Вако» 2008
5.Уроки химии. Неметаллы. 9класс с применением информационных технологий. М. Планета 2011
6.Мастер-класс учителя химии 8-11классы с применением информационных технологий. М. Планета 2010
7.Контрольные и проверочные работы. Химия.8 класс к учебнику О.С.Габриеляна М. Дрофа 2007
Химия.9 класс к учебнику О.С.Габриеляна М. Дрофа 2007
Химия.10 класс к учебнику О.С.Габриеляна М. Дрофа 2008
Химия.11 класс к учебнику О.С.Габриеляна М. Дрофа 2008
8.Химия. Внеклассные мероприятия 8-11 классы. Е.П.Ким. Издательство «Учитель» 2011
9. Органическая химия в тестовых заданиях 10-11 классы. М.А.Ахметов М. «Вентана-Граф» 2010
10.Химия. Сборник задач 8-9 классы. Е.В.Савинкова. М. «Аст-Пресс» 2008
11.Химия.Справочные материалы. Ю.Д.Третьяков М. «Просвещение» 1998
12.Химия. Справочник для школьника. М. 1995
13. Химия. Решение задач по химии. Справочник для школьника. М. 1995
14.Неорганическая химия. Весь школьный курс в таблицах. Минск. «Современная школа» «Кузьма» 2009
15.Органическая химия. Весь школьный курс в таблицах. Минск. «Современная школа» «Кузьма» 2009
16. Химия. Справочные материалы. Е.А.Еремина, Н.Е.Кузменко М. Дрофа 2008
17.Пособие для поступающих в ВУЗы. Справочник по химии. Е.П.Сидоров М. 1998
18.Тесты по химии к учебнику О.С.Габриеляна Химия 10 класс. Базовый уровень. М.А.Рябов. М. «Экзамен» 2011
ИКТ
1. Открытая химия
2.Уроки химии Кирилла и Мефодия» 8-9 класс
3.Уроки химии Кирилла и Мефодия» 10-11 класс
4 Органическая химия 10-11 класс
5.Химия. Общая и неорганическая 10-11класс
6.Химия 8 класс Габриелян О.С.
7.Химия 9 класс Габриелян О.С.
8.Химия 10 класс Габриелян О.С.
9. Химия 11класс Габриелян О. С.
| Химия8класс-9 класс 10-11 класс | Таблицы Нагревание и нагревательные приборы Получение и собирание газов Обращение с различными веществами Основные приемы работы в химической лаборатории Обработка пробок и стеклянных трубок Строение вещества 8-11класс Периодический закон Д. И.Менделеева Воздух Воздух Вода Серия таблиц по неорганической химии Серия инструктивных таблиц по химии Комплект транспарантов по неорганической химии Химия клетки. Белки и нуклеиновые кислоты Номенклатура Строение атома углерода Этан и метан Пространственная изомерия Производство ацетилена из метана Комплект портретов ученых-химиков Серия таблиц по органической химии Комплект транспарантов по органической химии Модели Набор кристаллических решеток набор для моделирования строения органических веществ Коллекции Алюминий Волокна Каменный уголь и продукты его переработки Каучук Металлы и сплавы Нефть и важнейшие продукты переработки Пластмассы Стекло и изделия из стекла Топливо Чугун и сталь Шкала твердости Набор хлопок Набор гранит Набор шелк Учебно-практические и учебно-лабораторное оборудование. Приборы, наборы посуды и лабораторных принадлежностей Для химического эксперимента общего назначения Весы Нагревательные приборы (спиртовки) Доска для сушки посуды Набор посуды и принадлежностей для демонстрационных опытов по химии Столик подъемный Штатив металлический Штатив для пробирок Озонатор Эвдиометр Прибор для получения газовКомплекты для лабораторных опытов и практических занятий по химии Весы Набор посуды и принадлежностей для ученического эксперимента Набор банок для хранения твердых реактивов Набор пробирок Нагревательные приборы (спиртовки) Штатив лабораторный химический Аппарат Киппа Набор посуды для реактивов НПРРеактивы Набор №1 ОС «Кислоты» Набор №2 ОС «Кислоты» Набор № 3 ОС « Гидроксиды» Набор №4 ОС « Оксиды металлов» Набор №5 ОС «Металлы» Набор № 7ОС « Огнеопасные вещества» Набор № 10 ОС «Сульфаты .Сульфиты. Сульфиды.» Набор № 3 ВС «Гидроксиды» Набор № 12 ВС «Соли» Набор № 18 ВС «Соединения хрома» Набор № 22 ВС «Индикаторы» Набор № 12 ОС «Соединения марганца» Набор № 18 ОС «Минеральные удобрения» Набор № 22 ОС «Углеводы. Амины» Набор № 17 ОС «Индикаторы» | 1 1 1 1 1 1 1 1 1 1 1 1 1 11 1 1 1 1 1 1 1 12 2 1 1 1 6 1 2 3 2 3 1 1 1 1 4 10 11 3 6 10 1 1 1 4 46 12 10 6 1 7 1 1 1 1 1 1 1 1 1 1 1 1 1 |
4.Тепловой эффект химической реакции
5.Окислительно-востановительные реакции
6.Электролиз
7.Генетическая связь классов неорганических веществ
8.Генетическая связь классов органических веществСтроение веществ
1.Строение атома
2.Элетронная орбита
3.Модели атомов некоторых элементов
4.Кристаллы
5.Химическая связь
6.Валентность
7.Степень окисления
8.Изомерия
9.Изомерия 2
10.Гомология
Номенклатура
1.Бинарные соединения
2.Номенклатура солей
3.Номенклатура органических соединений
4.Предельные углеводороды
5.Непредельные углеводороды
6.Функциальные производные углеводороды
Белки и нуклеиновые кислоты1.Первичная структура белка
2.Вторичная структура белка
3.Третичная структура белка
4.Четверичная структура белка
5.Денатурация белков
6.Гетероциклы с атомом азота
7.Принцип комплементарности
8.Нуклеиновые кислотыХимия клетки
1.Белки.Ферменты
2.Нуклеиновые кислоты
3.АТФ8 класс
Лабораторное оборудование5.Спиртовка
6.Газовая горелка
7.Электронагреватели
8.Нагревание
9.Приёмы обращения с лабораторным штативом
10.Получение и собирание газов
11.Обращение с твёрдыми веществами
12.Обращение с жидкими веществами
13.Взвешивание
14.Приготовление растворов
15.Фильтрование
16.Перегонка
17.Правила техники безопасности труда в кабинете химии. Запрещается!
19.Правила техники безопасности труда в кабинете химии. Осторожно!
l.120-bal.ru
Презентация по химии "Сплавы"(9 класс)
Инфоурок › Химия › Презентации › Презентация по химии "Сплавы"(9 класс)Описание презентации по отдельным слайдам:
1 слайд Описание слайда:
Описание слайда: Тема урока: Сплавы
2 слайд Описание слайда:
Описание слайда: Цель урока: Учащиеся должны получить общее представление о сплавах металлов, о принципе их образования и практической значимости. Знать: свойства отдельных сплавов и их отличие от чистых металлов. Уметь: выделять главное, сравнивать и обобщать;
3 слайд Описание слайда:
Описание слайда: «Найди ошибку» 1. Zn +2Н2O= Zn(OН)2 +Н2 2. Fe+ СI2= FeСI2. 3. ZnS+ O2= ZnO2+ SO2 4. Си+ FeSO4=.СиSO4+ Fe 5. Си +2Н СI= Н2+ СиСI2
4 слайд Описание слайда:
Описание слайда: Самый, самый, самый САМЫЙ ЛЕГКИЙ МЕТАЛЛ ТЯЖЕЛЫЙ МЕТАЛЛ ЛЕГКОПЛАВКИЙ МЕТАЛЛ ТУГОПЛАВКИЙ МЕТАЛЛ ТВЕРДЫЙ МЕТАЛЛ
5 слайд Описание слайда:
Описание слайда: Самый, самый, самый САМЫЙ ЛЕГКИЙ МЕТАЛЛ Li ρ = 0,53 г/см3 ТЯЖЕЛЫЙ МЕТАЛЛ Os ρ=22,5г/см3 ЛЕГКОПЛАВКИЙ МЕТАЛЛ Сs t пл =29°С ТУГОПЛАВКИЙ МЕТАЛЛ W tпл =3390С ТВЕРДЫЙ МЕТАЛЛ Cr
6 слайд Описание слайда:
Описание слайда: Повторение Какими физическими свойствами обладают металлы? Можно ли в структуру одного металла внедрить между ионами металла ионы другого металла и другие вещества? Изменяются свойства сплавов по сравнению со свойствами металлов, образующих их сплав.
7 слайд Описание слайда:
Описание слайда: Сплавы металлов Сплавы – это материалы с характерными свойствами, состоящими из двух или более компонентов, из которых по крайней мере один – металл.
8 слайд Описание слайда:
Описание слайда: Сплавы.
9 слайд Описание слайда:
Описание слайда: Способы получения сплавов 1.Сплавление (например. Получение третника) 2.Спекание (смесь нагревают под давлением, не доводя до плавления, образуются твердые растворы). 3.Диффузия в поверхностный слой одного металла ион-атоиов другого металла (амальгамирование, хромирование).
10 слайд Описание слайда:
Описание слайда: Строение сплавов: 1.Механическая смесь кристаллов (третник). 2.Замещение ион-атомов в кристаллической решетке. 3.Внедрение ион-атомов как инородных включений в металл.
11 слайд Описание слайда:
Описание слайда: Сообщения учащихся о сплавах
12 слайд Описание слайда:
Описание слайда: Сталь Сталь – сплав на основе железа, содержащий менее 2% углерода. Углеродистая сталь (мягкая, средняя – детали машин, трубы, болты, гвозди, скрепки; твёрдая – различные инструменты) Легированная сталь (самолёто -, ракето- и судостроение и.т.д.)
13 слайд Описание слайда:
Описание слайда: Применение. Сталь
14 слайд Описание слайда: 15 слайд
Описание слайда: 15 слайд  Описание слайда:
Описание слайда: дюралюминий
16 слайд Описание слайда:
Описание слайда: Цветные сплавы: бронза, латунь, мельхиор, дюралюминий Бронза – сплав на основе меди с добавлением (20%) олова. Подшипники, поршневые кольца, клапаны, художественное литьё. Латунь – медный сплав, содержащий от 10 до 50% цинка. Моторостроение. Мельхиор – сплав, содержащий около 80% меди и 20% никеля. Столовые приборы и художественные изделия. Дюралюминий – сплав на основе алюминия, содержащий медь, марганец, магний и никель. Самолето – и машиностроение.
17 слайд Описание слайда:
Описание слайда: Применение цветных металлов.
18 слайд Описание слайда:
Описание слайда: Чугун Чугун – сплав на основе железа, содержащий от 2 до 4,5 % углерода, марганца, кремния, фосфора, серы. Серый чугун Белый чугун
19 слайд Описание слайда:
Описание слайда: Применение черных металлов.
20 слайд Описание слайда:
Описание слайда: Латунь
21 слайд Описание слайда:
Описание слайда: Изделия из серебра и бронзы
22 слайд Описание слайда:
Описание слайда: Секрет булатных мечей. « Мне приснилась иная печаль Про седую дамасскую сталь. Я увидел, как сталь закалялась, Как из юных рабов одного Выбирали, кормили его, Чтобы плоть его сил набиралась. Выжидали положенный срок, А потом раскаленный клинок В мускулистую плоть погружали, Вынимали готовый клинок. Крепче стали не видел Восток, Крепче стали и горше печали.»
23 слайд Описание слайда:
Описание слайда: Металлы и человек. « Человек не может обойтись без металлов… Если бы не было металлов, люди влачили бы самую омерзительную и жалкую жизнь среди диких зверей» Георг Агрикола, 1556г.
Найдите материал к любому уроку,указав свой предмет (категорию), класс, учебник и тему:
Выберите категорию: Все категорииАлгебраАнглийский языкАстрономияБиологияВсемирная историяВсеобщая историяГеографияГеометрияДиректору, завучуДоп. образованиеДошкольное образованиеДругоеДругойЕстествознаниеИЗО, МХКИзобразительное искусствоИностранные языкиИнформатикаИскусствоИспанский языкИсторияИстория РоссииИстория Средних вековИтальянский языкКлассному руководителюКультурологияЛитератураЛитературное чтениеЛогопедияМатематикаМировая художественная культураМузыкаМХКНачальные классыНемецкий языкОБЖОбществознаниеОкружающий мирОсновы безопасности жизнедеятельностиПриродоведениеРелигиоведениеРисованиеРусский языкСоциальному педагогуТехнологияУкраинский языкФизикаФизическая культураФилософияФинский языкФранцузский языкХимияЧерчениеЧтениеШкольному психологуЭкология
Выберите класс: Все классыДошкольники1 класс2 класс3 класс4 класс5 класс6 класс7 класс8 класс9 класс10 класс11 класс
Выберите учебник: Все учебники
Выберите тему: Все темы
также Вы можете выбрать тип материала:
Общая информация
Номер материала: ДВ-467934
Похожие материалы
Оставьте свой комментарийinfourok.ru