Большая Энциклопедия Нефти и Газа. Иодирование металла
Иодирование металлов и неметаллов иодом
Иодирование металлов и неметаллов проводят при их нагревании в парах иода. Наиболее простой метод иодирования — совместное нагревание веществ в запаянных стеклянных или кварцевых ампулах. [c.43]
ИОДИРОВАНИЕ МЕТАЛЛОВ И НЕМЕТАЛЛОВ В ПАРАХ ИОДА В СМЕСИ С ВОДОРОДОМ, АЗОТОМ, ОКСИДОМ УГЛЕРОДА (IV) ИЛИ АРГОНОМ [c.44]
ИОДИРОВАНИЕ МЕТАЛЛОВ И НЕМЕТАЛЛОВ ИОДОМ В ВОДНЫХ И ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЯХ [c.45]Иодирование металлов и неметаллов иодом [c.85]
Иодирование металлов и неметаллов в парах иода в смеси с водородом, азотом, двуокисью углерода или аргоном [c.87]
Простейшая установка иодирования металлов и неметаллов в парах иода в смеси с газом-носителем приведена на рисунке 52. Если получаемый иодид возгоняется при 200—300° С, то для работы применяют четырехколенную трубку. В первое колено помещают металл, а затем иод 2. Металл нужно брать в виде тонкой проволоки, стружки или крупки и помещать его таким слоем, чтобы не было просветов и не наблюдалось проскоков паров иода во второе колено трубки. Вытесняют воздух из трубки водородом, азотом или аргоном и нагревают ее в том месте, где находится металл. При этом испаряется и иод. Газ-носитель захватывает пары иода и относит их к металлу. При достаточной толщине слоя металла во второе отделение будут поступать только пары иодида. После испарения всего иода нагревают колено Б, из которого пары иодида будут испаряться и током газа-носите-ля относиться в колено В, где вещество и запаивают. [c.87]
Иодирование металлов и неметаллов иодом в водных и органических растворителях [c.88]
Простейшая установка иодирования металлов и неметаллов Е парах иода в смеси с газом-носителем изо- [c.72]
Если иодид испаряется выше 400—500 °С, то для иодирования используют кварцевую или фарфоровую т рубку (рис. 16). Металл илн неметалл помещают в среднюю часть трубки или в лодочке. Иод помещают в начале трубки и подогревают его до 80—100°С. Пары иода увлекаются к металлу газом-носителем водородом, азотом, аргоном или оксидом углерода (IV). Его можно применять только в том случае, если оксид не окисляет металл (сурьма, висмут, ртуть, кадмий, свинец). После [c.44]
Если иодид испаряется выше 400—500° С, то для иодирования используют трехколенную трубку (рис. 52). Металл или неметалл помещают в среднее колено Б, над которым при нагревании пропускают пары иода. Для [c.87]
Если иодид испаряется выше 400—500°С, то для иодирования используют трехколенную трубку (рис. 52). Металл или неметалл помещают в среднее колено, над которым при нагревании пропускают пары иода. Для этого иод помещают в начале -трубки и подогревают [c.73]
Исходные металлы и неметаллы могут содержать примеси, например окислы кроме того, в реакционное пространство могут попасть вместе с галогенами или вследствие негерметичности прибора кислород и пары воды, под действием которых уже во время реакции могут образоваться окислы. Если окислы не вступают в реакцию с галогеном и не превраш,аются в галогениды, то они переходят в продукт реакции и загрязняют его. Нужно учитывать, что образование галогенидов из окислов при действии на последние галогенами затрудняется при переходе от фтора к иоду. Так, например, большинство окислов не поддается иодированию в то же время переход иодидов под действием кислорода в окислы термодинамически более вероятен, чем такой же переход других галогенидов, и особенно фторидов. Это обстоятельство следует особо принимать во внимание при получении галогенидов таких элементов, окислы которых образуются с выделением значительных количеств тепла (термически устойчивы), а галогениды [c.154]
chem21.info
Неорганический синтез - 0035 - Портал аналитической химии
Макет страницы
Глава VI
ИОДИРОВАНИЕ МЕТАЛЛОВ, НЕМЕТАЛЛОВ И ОКСИДОВ
§ 1. ИОДИРОВАНИЕ МЕТАЛЛОВ И НЕМЕТАЛЛОВ ИОДОМ
Иодирование металлов и неметаллов проводят при их нагревании в парах иода. Наиболее простой метод иодирования — совместное нагревание веществ в запаянных стеклянных или кварцевых ампулах.
Для работы используют ампулу, имеющую два колена (рис. 13).
Металл и иод, взятые по расчету, помещают раздельно в ампулу и запаивают ее по линии ав. Затем нагревают металл до 300—500 °С. Иод к металлу поступает в результате испарения. Если давление паров иодида при температуре 300—350 0C меньше 10 Па, то большая часть его останется в том же колене трубки, где и металл. В этом случае иод необходимо брать или точно в соответствии с уравнением реакции, или в небольшом избытке. При недостатке иода получаемый иодид будет загрязнен исходным материалом. Если же при температуре иодирования продукт имеет давление паров 5 кПа и более, то он будет возгоняться и конденсироваться во втором колене трубки и в суженной части. В этом случае металла нужно брать несколько больше теоретически рассчитанного количества, поскольку иодиды растворяют и присоединяют иод. Полученное вещество для удаления иода нужно снова перегнать из второго колена в первое, где находится еще не вступивший в реакцию металл. Для этого, не меняя положения трубки, нагревают второе колено, тогда вещество будет возгоняться в холодную часть трубки. Затем после охлаждения нужно снова нагреть возгон, чтобы он сконденсировался в колене, где был ранее иод. Во время этой операции иод, захваченный иодидом, будет вступать в реакцию с металлом. После вторичной возгонки иодид запаивают в трубке.
S 2. ИОДИРОВАНИЕ МЕТАЛЛОВ И НЕМЕТАЛЛОВ СМЕСЬЮ ПАРОВ ИОДА С ВОДОРОДОМ, АЗОТОМ, ОКСИДОМ УГЛЕРОДА (IV) ИЛИ
АРГОНОМ
Простейшая установка иодирования металлов и неметаллов парами иода в смеси с газом-носителем изображена на рисунке 15. Если получаемый иодид возгоняется при 200—300 °С, то для работы применяют четырехколенную трубку. В первое колено помещают металл 3, а затем иод 2. Металл нужно брать в виде тонкой проволоки, стружки или крупки и помещать его таким слоем, чтобы не было просветов и не наблюдалось проскоков паров иода во второе колено трубки. Вытесняют воздух из трубки
www.chemical-analysis.ru
Анодирование в домашних условиях - способы и технология
У многих красивое и непонятное слово «анодирование» ассоциируется со сложным физико-химическими технологиями, лабораторными условиями и прочей научной атрибутикой. Мало кто знает, что этот полезный и несложный процесс можно провести при помощи подручных средств: сделать анодирование титана и других металлов реально даже в домашних условиях. Но что это такое, и зачем это нужно для металла?

Название анодирования носит процесс, протекающий при использовании электролита и электрического тока различной величины и позволяющий получить на изделии прочную оксидную пенку, которая повышает прочность стали и обеспечивает защиту от коррозии. Прочностные и механические характеристики меняются в зависимости от состава металла, плотности и вида электролита, величины анодного и катодного воздействия, рассчитываемых по специальным уравнениям.
Собственно защитное покрытие не наносится, а образуется из самого железа в процессе электрохимической реакции. Технология, используемая в домашних условиях, схематично выглядит так:
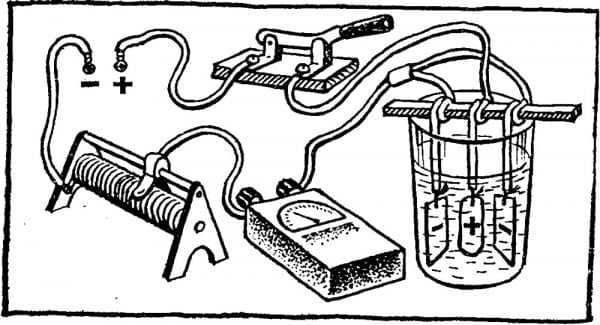 Схема процесса анодирования в домашних условиях
Схема процесса анодирования в домашних условиях- В диэлектрическую (не проводящую ток) емкость заливается электролит.
- Берется блок питания, способный обеспечить необходимое напряжение постоянного тока на выходе (это может быть аккумулятор или несколько батареек, соединенных в электронные цепи).
- К обрабатываемому предмету подключается зажим «+», и предмет погружается в емкость с раствором.
- Зажим «–» крепится на пластинку из свинца или нержавеющей стали и тоже опускается в жидкость.
- Подключается электрический ток нужной величины, согласно электрохимическому уравнению. Благодаря ему на поверхности изделия начинает выделяться кислород, способствующий образованию прочной защитной пленки.
Анодное оксидирование (анодирование) различных металлов, проведенное в домашних условиях, конечно, сильно уступает тому, что проводится с применением промышленного оборудования. Но, все же, оно способно обеспечить изделию ряд преимуществ:
- Повысить устойчивость к коррозии — благодаря тому, что оксидная пленка препятствует проникновению влаги к металлической основе, обеспечивая надежную защиту. Применение такого процесса на быстро ржавеющих предметах обихода или дисках и деталях бытовой техники способно значительно продлить срок их службы.
- Увеличить прочность металла и стали: оксидированное покрытие намного устойчивее к механическим и химическим повреждениям.
- Обработанная таким образом посуда нетоксична, устойчива к длительному нагреву, пища на ней не пригорает.

- Металлические изделия после анодированной обработки приобретают диэлектрические свойства (совсем или почти не проводят ток).
- Возможность провести гальваническое напыление другого металла (хромовое, титановое). Выполненное своими руками, оно способно значительно увеличить прочностно-механические характеристики или повысить декоративные качества (напыление под золото).
Кроме того, процесс дает возможность декорирования. Можно сделать цветное анодное оксидирование. Такой результат можно получить, изменяя уравнения силы подаваемого тока и плотности электролита (это возможно, когда проводится анодирование титана и других твердых материалов) или с использованием краски (чаще для алюминия и других мягких металлов, но этот процесс применяется и на твердых основах). Окрашенные таким образом предметы имеют более ровный и глубокий цвет.

Промышленный метод дает более высокую прочность покрытия, возможность провести глубокое анодирование с одновременным нанесением катодной электрохимической пенки, дающей дополнительную защиту от коррозии. Но, даже проведенная в домашних условиях анодно-катодная обработка поможет сделать диски или другие детали движущихся механизмов более прочными, износостойкими.
Разные способы
Провести процесс оксидированной обработки стали в домашних условиях можно двумя способами. Каждый из них имеет свои недостатки и преимущества.
Теплый метод
Наиболее легкий процесс для проведения своими руками. Успешно протекает при комнатной температуре, при использовании органической краски, позволяет создавать удивительно красивые вещи. Для этой цели можно использовать как готовые краски, так и аптечные красители (зеленку, йод, марганец).

Твердое анодирование по такой технологии получить не удастся, оксидная пенка получается непрочная, дает слабую защиту от коррозии, легко повреждается. Но, если сделать окрашивание поверхности после такой методики, то сцепление (адгезия) покрытия с основой будет очень высокой, нитроэмали или другие краски будут держаться прочно, не облезут, обеспечат высокую степень защиты от коррозии.
Холодный метод
Эта методика при проведении в домашних условиях требует внимательного контроля за температурой, допуская ее колебания от –10 до +10°C (оптимальная температура для проведения электрохимической реакции согласно уравнению – 0°C). Именно при таком температурном режиме анодная и катодная обработка поверхности протекает наиболее полно, медленно создавая прочную защитную оксидную пленку. Это позволяет домашнему умельцу своими руками провести твердое анодирование, обеспечив стали максимальную защиту от коррозии.

По этой методике можно сделать гальваническое напыление, нанеся на изделие медь, хром или золото, рассчитав силу тока по специальным уравнениям. После такой обработки повредить деталь или диски из стали очень сложно. Защита от коррозии эффективно действует на протяжении многих лет даже при контакте с морской водой, может использоваться для продления срока службы подводного снаряжения.
Маленьким минусом служит то, что краска на такой поверхности не держится. Для придания металлу цвета используется метод напыления (медь, золото) или электрохимическое изменение цвета под воздействием электрического тока (сила тока и плотность электролита высчитываются по специальному уравнению).
Технология анодного оксидирования
Весь процесс, проводимый своими руками, можно разделить на этапы:
- Поверхности дисков и других деталей из металла хорошо очищаются от загрязнений, моются, шлифуются.
- Проводится обезжиривание Уайт-спиритом или ацетоном.

- Выдерживается необходимое время в щелочном растворе (оно рассчитывается по уравнению, исходя из структуры материала).
- После этого диски или другие металлические изделия погружаются в электролит, где проводится анодная и катодная реакция наращивания оксидной пленки.
- Если проводилось холодное обрабатывание изделия, то после извлечения его из емкости следует тщательно промыть от кислоты, просушить. После завершения этого процесса ему обеспечена долгая надежная защита от коррозии.
- При тепловом процессе пленка будет пористая, мягкая, требующая дополнительного закрепления, проводимого путем окунания в чистую кипящую воду или посредством воздействия горячего пара. Потом ее нужно хорошо промыть.
Разновидности электролитов
В домашних условиях применяют не только промышленные химические кислотные растворы, но и простые средства, которые можно найти на любой кухне:
- Проводя анодирования титана, можно брать натрия хлорид, серную или ортофосфорную кислоты.
- Для алюминия применяют щавелевую, хромовую или серную кислоты.
- Вместо кислот для анодной и катодной обработки дисков или других предметов из стали можно использовать поваренную соль с пищевой содой. Сделать необходимый электролит можно, смешав 9 частей концентрированного содового раствора с одной частью солевого.

Время выдержки дисков, пластин, других металлических предметов в электролитной емкости под током рассчитывается по уравнению, исходя из физико-химических параметров.
Опасные моменты
При использовании кислот в качестве электролита необходимо строго соблюдать правила техники безопасности. Пренебрежение ими может привести к несчастным случаям:
- При попадании на кожу из-за того, что используется разбавленный препарат, возможны небольшие ожоги. Но для глаз такая концентрация опасна, поэтому не следует пренебрегать защитными очками и перчатками.
- Под воздействием тока выделяются кислородные и водородные пары, которые при смешивании образуют гремучий газ. Работая в плохо вентилируемом помещении, можно получить взрыв от любой искры, который может привести к смертельному исходу.
Соблюдая технику безопасности и этапы технологической обработки, можно получать прочные красивые вещи: хромировать автомобильные диски, создавать ювелирные украшения «под золото», добавлять прочности деталям бытовых механизмов в зависимости от применяемых технологий.
kraska.guru
Большая Энциклопедия Нефти и Газа, статья, страница 3
Иодирование
Cтраница 3
Иодирование самого бензола не идет, однако некоторые производные бензола, имеющие активирующие заместители, могут иодироваться. [31]
Иодирование белков может быть использ. Тирози-новые и значительно медл. Иодированные производные гнстидина разл. [32]
Иодирование аренов требует специальных условий. Иод с аренами непосредственно не реагирует, только образует слабые комплексы с переносом заряда, так как имеет меньшее сродство к электрону, чем бром и хлор. [33]
Иодирование метана, согласно значениям энергии, приведенным в схеме (9.9), уже невозможно, так как и зарождение цепи, и общая реакция сильно эндотермичны, поэтому реакция идет скорее в обратном направлении. Известно, что алкилиодиды легко превращаются в углеводороды и иод под действием йодистого водорода. [34]
Иодирование соединений, замещенных в пара-положении бензоильной группы, при кипячении трикетона со спиртовым раствором йода идет так же легко. Реакции замещения, вероятно, предшествует образование КПЗ трикетон-йод, так как при сливании их растворов при комнатной температуре происходит мгновенное увеличение оптической плотности по сравнению с плотностью раствора йода. [35]
Иодирование триалкилборанов в присутствии NaOH [214] пли ( что лучше) в присутствии NaOMe в метаноле [215], протекает аналогично бронированию. В первичных триалкилборанах в обоих случаях отщепляются две группы. В смешанных триорганилборанах отщепление групп идет со значительной селективностью. [36]
Иодирование метана, как видно из табл. 9.3, оказывается невозможным, поскольку здесь и старт цепи, и реакция в целом сильно эндотермичны и поэтому реакция скорее может идти в обратном направлении: известно, что алкилиодиды при действии йодистого водорода легко превращаются в углеводороды и иод. [37]
Интенсивное иодирование металлического гафния в вакууме ( 10 - 2 - 10 - 3 мм рт. ст.) начинается при температуре наружной стенки сосуда 270 С, заканчивается при 400 С, иногда наблюдается возгорание металла. [39]
Иодирование метана протекает очень медленно, поэтому реакцию считают практически неосуществимой. Первая стадия роста цепи эндотермична ( ДЯ - 31 ккал / моль) и имеет ЕакТ 34 ккал / моль, именно эта стадия и обусловливает трудности протекания процесса. Даже при 300 С доля атомов иода с необходимой энергией настолько ничтожна, что уже на первой стадии тормозится весь ход процесса. [40]
Иодирование металлов и неметаллов проводится при их нагревании в парах иода. [41]
Иодирование металлов и неметаллов проводят при их нагревании в парах иода. [42]
Иодирование диалкил-фосфитов также применяется при их количественном определении. [43]
Осторожное иодирование [ добавление по каплям 0 5 % - ного бензольного раствора иода к смеси ( Geh3) v -: - бензол ] приводит сначала к образованию иодполигермена, а затем GeI4, но иодирование проходит не до конца. [44]
Иодирование металлов и неметаллов проводят при их нагревании в najpax иода. [45]
Страницы: 1 2 3 4
www.ngpedia.ru
Мир современных материалов - Анодирование металлов
Анодирование металла - это процесс электрохимического наращивания оксидной пленки путем анодного окисления.
Оксидная плёнка, полученная путем анодирования, прочно держится на поверхности своего металла. Возможно формирование оксидной пленки на поверхности металла другим способом - за счет повышения температуры. Но данный процесс возможен только до некоторой толщины, выше которой оксидная пленка трескается, ломается и отслаивается. При анодировании можно получать более толстые оксидные пленки, сохраняющие защитные свойства и прекрасную адгезию к субстрату.
Анодирование возможно практически для любого металла. Однако при анодировании есть ряд требований к росту пленки и ее адгезии. Во-первых, анодируемый металл должен образовывать только один устойчивый оксид. Образование двух различных оксидов ухудшает адгезию и повышает вероятность растрескивания пленки. По этой причине анодирование железа и меди крайне затруднительно. Во-вторых, при хорошей адгезии к металлу оксидная плёнка должна вместе с тем оставаться пористой, чтобы обеспечить беспрепятственный доступ электролита к поверхности металла для лучшего окисления и ее более быстрого роста. Этим требованием удовлетворяет очень мало металлов. Фактически, анодированию подвергают только алюминий, титан и тантал. Наиболее широко распространено анодирование алюминия.
Окисление алюминия на аноде сопровождается выделением кислорода. Наиболее распространёнными являются ванны с серной кислотой. В особых случаях применяют ванны с хромовой или щавелевой кислотой. Разряжаемый кислород частично реагирует с алюминием анода, а частично теряется в виде газа. По этой причине образующаяся оксидная плёнка содержит массу микроканалов, через которые к поверхности металла может поступать электролит. В результате толщина оксидной плёнки может достигать довольно больших значений. Данный механизм иллюстрирует рис. 1.
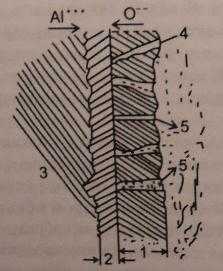
1 - гидратированный Al2O3; 2.- Al2O3; 3 - основной металл алюминий; 4 - микроканалы внутри плёнки; 5 - электролит (присутствует и внутри микроканалов)
Рис. 1. Механизм роста оксидной пленки алюминия.
В начале анодирования толщина пленки мала, ее сопротивление невелико и для поддержания необходимой плотности тока требуется небольшое напряжение. По мере роста толщины пленки и возрастания ее сопротивления, ток падает. При слишком большой толщине пленки она даже может начать растворяться. По закону Фарадея скорость образования пленки зависит от тока. Поэтому необходимо поддерживать требуемую плотность тока на протяжении всего процесса анодирования. Этого можно достичь постепенно увеличивая прикладываемое напряжение по мере анодирования.
Другой способ состоит в использовании менее крепкой кислоты. Однако ниже определенного значения крепость кислоты уменьшать нельзя. Поскольку в процессе анодирования кислота расходуется, при этом она должна обладать достаточной электропроводностью, иначе повышение прикладываемого напряжения вызовет ее разогрев.
Рабочие параметры процесса анодирования металлов приведены в табл. 1.
Таблица 1. Рабочие параметры процесса анодирования металлов.
|
Рабочие параметры |
Ванна на основе хромовой кислоты |
Ванна на основе серной кислоты |
Ванна на основе щавелевой кислоты |
|
Крепость |
3% |
10-30% |
3-8% |
|
Температура, °С |
40-45 |
20-25 |
25-30 |
|
Напряжение, В |
0-40 |
10-20 |
50-100 |
|
Плотность тока, мА/см2 |
3-10 |
4-15 |
50 |
|
Описание плёнки |
Полупрозрачная |
Прозрачная |
Прозрачная |
|
Растворимость плёнки |
Слабо растворима |
Умеренно растворима |
Практически нерастворима |
|
Рассеивающая способность |
Почти 100% |
Меньше |
Ещё меньше |
|
Время процесса, мин |
10-30 |
10-120 |
~40 |
Ванна не должна содержать более 1% хлоридов. Превышение этого порога повышает риск питтингообразования. По мере протекания процесса нарастает концентрация ионов алюминия. Считается, что эта величина не должна превышать 20 г/л, так как повышение содержания ионов алюминия повышает вязкость. Анод н катод должны отстоять друг or друга как можно дальше. Обычно катод размещают вблизи стенки ванны, а анод - по центру. Получаемая в процессе анодирования оксидная плёнка алюминия пористая, внутри пор накапливаются гидратированные гидроксид и сульфат алюминия, вода и некоторое количество свободной кислоты. После извлечения изделия из кислотной ванны его следует тщательно промыть, чтобы на его поверхности не осталось свободной кислоты.
Важно, чтобы поры в оксидной плёнке оказались в итоге заполненными. Оксидная плёнка алюминия способна поглотить самые разные вещества, которые могут придать ей тот или иной цвет. Заполнение пустот выполняется в водяной ванне при температуре около 80°С в течение нескольких минут в ванну добавляют около 1% карбоната натрия, который должен нейтрализовать свободную кислоту, если она осталась внутри пленки после промывки. Если не требуется дополнительного окрашивания, то анодированную поверхность обрабатывают ацетатом никеля. Он гидролизуется внутри пор пленки, давая осадок белого цвета.
В случае дополнительного окрашивания, после завершения требуется заполнить поры пленок. Состав ванн для окрашивания приведен в табл. 2.
Таблица. 2. Красители, применяемые для окрашивания оксидных плёнок
|
Первый раствор |
Второй раствор |
Образующийся краситель |
Внешний вид получающейся плёнки |
|
Вода (деионизованная) |
— |
— |
Прозрачная |
|
Аммоний-железа оксалат |
— |
Fe304 |
Золотистая |
|
Оксалат хрома |
— |
Сr203 |
Зелёная |
|
Ацетат кобальта |
КМn04 |
СоО |
Бронзового цвета |
|
Ацетат свинца |
Аммония гидросульфат |
PbS |
Коричнево-чёрная |
Эффективность полученных защитных покрытий чаще всего проверяют испытанием в соляном тумане.
Толщина оксидной пленки зависит от цели применения анодированного алюминия:
Архитектурное применение 2-5 мкм
Автомобильное применение 8-10 мкм
Внешние поверхности без регулярного ухода 20 мкм
Твердое анодирование 50 мкм
Литература:
Р. Ангал. Коррозия и защита от коррозии. Изд-во «Интеллект», 2013. – 344 с.Source: http://worldofmaterials.ru/spravochnik/tests/148-korrozionnye-ispytaniya-obshchie-svedeniya
Вас также может заинтересовать:
worldofmaterials.ru
Анодирование металла, его процесс на производстве и в домашних условиях
Содержание статьи
В современном мире имеется большое количество методов обработки металлов и металлических изделий. Они применяются и в промышленных масштабах, и в домашних условиях.
Характеристики анодирования

Анодирование представляет собой процедуру образования на поверхности различных металлов оксидной пленки путем анодного окисления. Наращивание оксидной пленки осуществляется в проводящей среде. На поверхности металла такая пленка держится достаточно хорошо.
Наращивание оксидной пленки может осуществлять и благодаря методу повышения температурного режима. Однако при этом она получается низкой по прочности и не держится длительное время. Благодаря электрохимическому способу образования оксидной пленки она получается оптимальной толщины и отлично держится на поверхности материала.
Анодированию можно подвергать разные виды металлов. Основным требованием является то, что они должны иметь возможность образовывать только один оксид. Он должен обладать максимальным уровнем устойчивости. Если металл обладает способностью образовывать сразу несколько оксидов, это может привести к тому, что пленка просто начнет трескаться и не появится защитного эффекта. Именно по этой причине только на редких промышленных объектах встречаются случаи анодирования железа или меди.
Кроме того оксидная пленка на поверхности металлов должна обладать пористой структурой. Это необходимо для того, чтобы электролиты лучше в нее проникали. В результате получается, что лишь небольшая часть всех имеющихся на земле металлов способны удовлетворять данным параметрам. К ним относятся алюминий, тантал, титан. В промышленной и бытовой сфере чаще всего встречается обработка при помощи анодирования алюминиевого материала.
Процесс анодирования
Технология анодирования различных видов металлов является несложной. Главное только иметь под рукой все необходимое для ее осуществления.
Она осуществляется в несколько этапов:
- Подготовка металлов к образованию оксидной пленки.
На данном этапе проводятся подготовительные работы для анодирования. Они заключаются в том, чтобы тщательным образом очистить и отмыть поверхность металла. Сначала удаляются все загрязнения и налеты. Затем при помощи воды или специальных растворов проводится промывка материала. После этой процедуры его необходимо высушить.
- Подготовка раствора
На данном этапе осуществляется подготовка раствора с кислой или любой другой средой и подключают к положительному плюсу источника тока.
- Покрытие поверхности металлов или их сплавов оксидной пленкой.
На данном этапе осуществляется погружения металла или изделии я из него в приготовленный раствор.
Материалы для анодирования
 Сегодня для анодирования используются различные металлические материалы.
Сегодня для анодирования используются различные металлические материалы.
В настоящее время выделяются такие виды анодирования в зависимости от используемых материалов, как:
Анодирование алюминия
Данный процесс сегодня встречается чаще всего. Он заключается в покрытии оксидной пленкой алюминиевого материала. Алюминий в процессе опускается в кислую среду, и к нему проводится положительный плюс источника тока. В результате на материале появляется тонкая оксидная пленка.
Анодирование титана
Всем известно, что титан относится к категории металлов, которые нашли широкое применение в промышленности, но они обладают низким уровнем износостойкости. Для придания ему прочности и устойчивости к разным условиям окружающей среды применяется процедура анодирования. При этом вся анодная обработка металла осуществляется в кислой среде при температуре от 40 до 50 градусов Цельсия.
Анодирование стали
Анодирование стали является сложным процессом. Для этого используется либо щелочная среда, либо кислая. В результате образуется оксидная пленка, которая придает высокий уровень прочности.
Анодирование меди
Медь является достаточно гибким видом металла. Для придания ей прочности используются различные методы. Одним из них является анодирование. Благодаря помещению медного материала в кислую среду, на поверхности образуется плотная пленка оксида, которая придает материалу большое количество полезных характеристик.
Таблица. Таблица совместимости металлов и сплавов
| Алюминий | Совм | Не совм | Совм | Не совм | Не совм | Не совм | Не совм | Не совм | Совм | Не совм | Совм |
| Бронза | Не совм | Совм | Не совм | Совм | Совм | Совм | Пайка | Пайка | Не совм | Совм | Не совм |
| Дюралюминий | Совм | Не совм | Совм | Не совм | Не совм | Не совм | Не совм | Не совм | Совм | Не совм | Совм |
| Латунь | Не совм | Совм | Не совм | Совм | Совм | Совм | Пайка | Пайка | Не совм | Совм | Не совм |
| Медь | Не совм | Совм | Не совм | Совм | Совм | Совм | Пайка | Пайка | Не совм | Совм | Не совм |
| Никель | Не совм | Совм | Не совм | Совм | Совм | Совм | Пайка | Пайка | Совм | нет данных | Совм |
| Олово | Не совм | Пайка | Не совм | Пайка | Пайка | II | Совм | Совм | Совм | нет данных | Совм |
| Оловянно-свинцовый сплав (припой ПОС) |
Не совм | Пайка | Не совм | Пайка | Пайка | Пайка | Совм | Совм | Совм | нет данных | Совм |
| Сталь нелегированная (углеродистая)/ чугун | Совм | Не совм | Совм | Не совм | Не совм | Совм | Совм | Совм | Совм | Совм | Совм |
| Хром | Не совм | Совм | Не совм | Совм | Совм | нет данных | нет данных | нет данных | Совм | Совм | Совм |
| Цинк | Совм | Не совм | Совм | Не совм | Не совм | Совм | Совм | Совм | Совм | Совм | Совм |
Анодирование в домашних условиях

В современном мире в бытовой сфере используется большое количество металлических предметов, которые используются для различных целей. Каждому их владельцу хочется защитить их появления коррозии, чтобы они прослужили длительный период времени. Для этой цели подходит анодирование в домашних условиях.
Важно: Процедуру домашнего анодирования любого металла необходимо осуществлять на улице или на балконе.
Сначала необходимо приготовить раствор. Для этого нужно смешать дистиллированную воду и кислоту в определенной пропорции. С серной кислотой важно обращаться предельно аккуратно, потому что она при попадании в глаза и на кожу может привести к появлению неприятной ситуации.
После этого можно подготовить детали из металлов для обработки. Для этой цели используются всевозможные вещества. Они способны очистить их для проведения процедуры.
На последнем этапе домашнего анодирования осуществляется погружения металлических деталей в раствор и подключение электрического тока.
Видео анодирования в домашних условиях
lkmprom.ru
Большая Энциклопедия Нефти и Газа, статья, страница 3
Иодирование
Cтраница 3
Иодирование самого бензола не идет, однако некоторые производные бензола, имеющие активирующие заместители, могут иодироваться. [31]
Иодирование белков может быть использ. Тирози-новые и значительно медл. Иодированные производные гнстидина разл. [32]
Иодирование аренов требует специальных условий. Иод с аренами непосредственно не реагирует, только образует слабые комплексы с переносом заряда, так как имеет меньшее сродство к электрону, чем бром и хлор. [33]
Иодирование метана, согласно значениям энергии, приведенным в схеме (9.9), уже невозможно, так как и зарождение цепи, и общая реакция сильно эндотермичны, поэтому реакция идет скорее в обратном направлении. Известно, что алкилиодиды легко превращаются в углеводороды и иод под действием йодистого водорода. [34]
Иодирование соединений, замещенных в пара-положении бензоильной группы, при кипячении трикетона со спиртовым раствором йода идет так же легко. Реакции замещения, вероятно, предшествует образование КПЗ трикетон-йод, так как при сливании их растворов при комнатной температуре происходит мгновенное увеличение оптической плотности по сравнению с плотностью раствора йода. [35]
Иодирование триалкилборанов в присутствии NaOH [214] пли ( что лучше) в присутствии NaOMe в метаноле [215], протекает аналогично бронированию. В первичных триалкилборанах в обоих случаях отщепляются две группы. В смешанных триорганилборанах отщепление групп идет со значительной селективностью. [36]
Иодирование метана, как видно из табл. 9.3, оказывается невозможным, поскольку здесь и старт цепи, и реакция в целом сильно эндотермичны и поэтому реакция скорее может идти в обратном направлении: известно, что алкилиодиды при действии йодистого водорода легко превращаются в углеводороды и иод. [37]
Интенсивное иодирование металлического гафния в вакууме ( 10 - 2 - 10 - 3 мм рт. ст.) начинается при температуре наружной стенки сосуда 270 С, заканчивается при 400 С, иногда наблюдается возгорание металла. [39]
Иодирование метана протекает очень медленно, поэтому реакцию считают практически неосуществимой. Первая стадия роста цепи эндотермична ( ДЯ - 31 ккал / моль) и имеет ЕакТ 34 ккал / моль, именно эта стадия и обусловливает трудности протекания процесса. Даже при 300 С доля атомов иода с необходимой энергией настолько ничтожна, что уже на первой стадии тормозится весь ход процесса. [40]
Иодирование металлов и неметаллов проводится при их нагревании в парах иода. [41]
Иодирование металлов и неметаллов проводят при их нагревании в парах иода. [42]
Иодирование диалкил-фосфитов также применяется при их количественном определении. [43]
Осторожное иодирование [ добавление по каплям 0 5 % - ного бензольного раствора иода к смеси ( Geh3) v -: - бензол ] приводит сначала к образованию иодполигермена, а затем GeI4, но иодирование проходит не до конца. [44]
Иодирование металлов и неметаллов проводят при их нагревании в najpax иода. [45]
Страницы: 1 2 3 4
www.ngpedia.ru