Содержание
Температура плавления цинка, химические и физические свойства
Главная » Сплавы » Какая температура плавления у цинка?
На чтение 4 мин
Содержание
- Что такое цинк
- Структура и состав
- Свойства и характеристики
- Физические
- Химические
- Области применения
- Содержание в природе
- Историческая справка
- Производство
Цинк — важный элемент, входящий в периодическую таблицу Менделеева. Его обозначение —Zn. Используется в разных отраслях промышленности. Людям, работающим с этим материалом, важно знать температуру плавления цинка, его химический, механические свойства.
Плавление цинка
Что такое цинк
Цинк — металл сине-белого цвета. Стоит под тридцатым номером в таблице Менделеева. При взаимодействии поверхности материала с кислородом, на ней образуется оксидная плёнка. Она скрывает естественный блеск металла, защищает его от окисления.
Структура и состав
В природе цинк нельзя найти в чистом виде. Он будет состоять по большей части из основного металла, дополнительно иметь примеси. К ним относится серебро, кадмий, свинец, медь, железо. Зависимо от процентного содержания дополнительных элементов проводится маркировка материала.
Он будет состоять по большей части из основного металла, дополнительно иметь примеси. К ним относится серебро, кадмий, свинец, медь, железо. Зависимо от процентного содержания дополнительных элементов проводится маркировка материала.
Свойства и характеристики
Характеристики металла зависят от его состава. Зависимо от физических и химических свойств мастера металлургии определяют, где лучше использовать материал, чтобы добиться наилучшей эффективности.
Физические
Физические свойства материала определяют его возможности изменения под воздействием сторонних сил. К ним относятся:
- Легко растворяется в щелочах и кислотах.
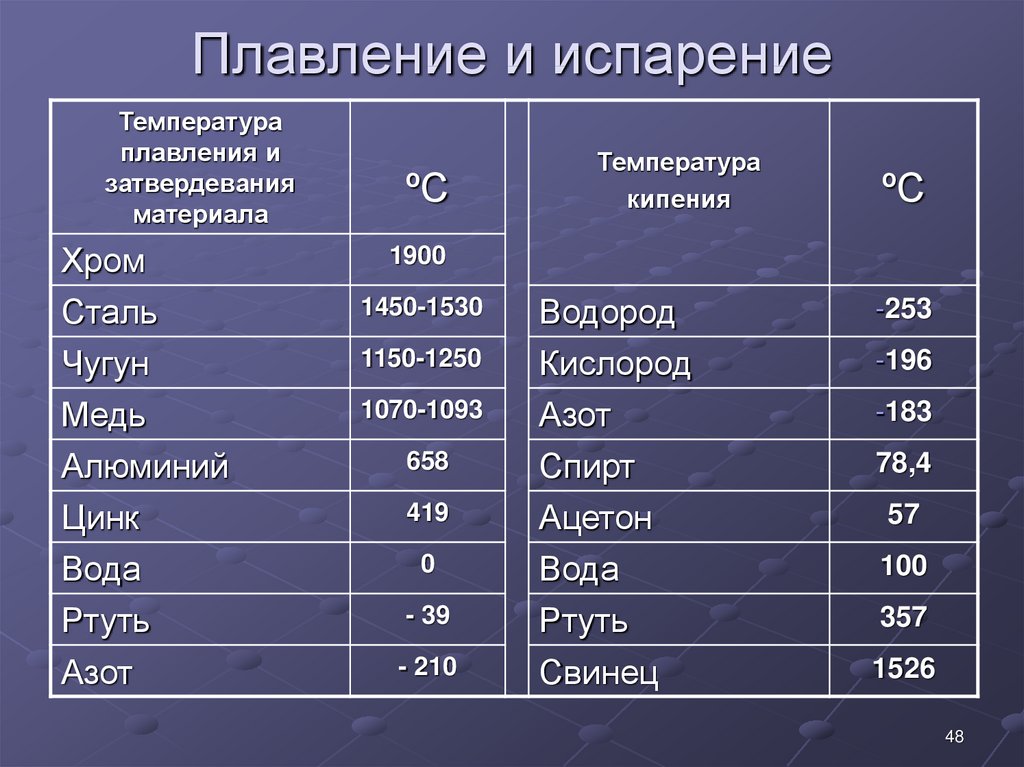
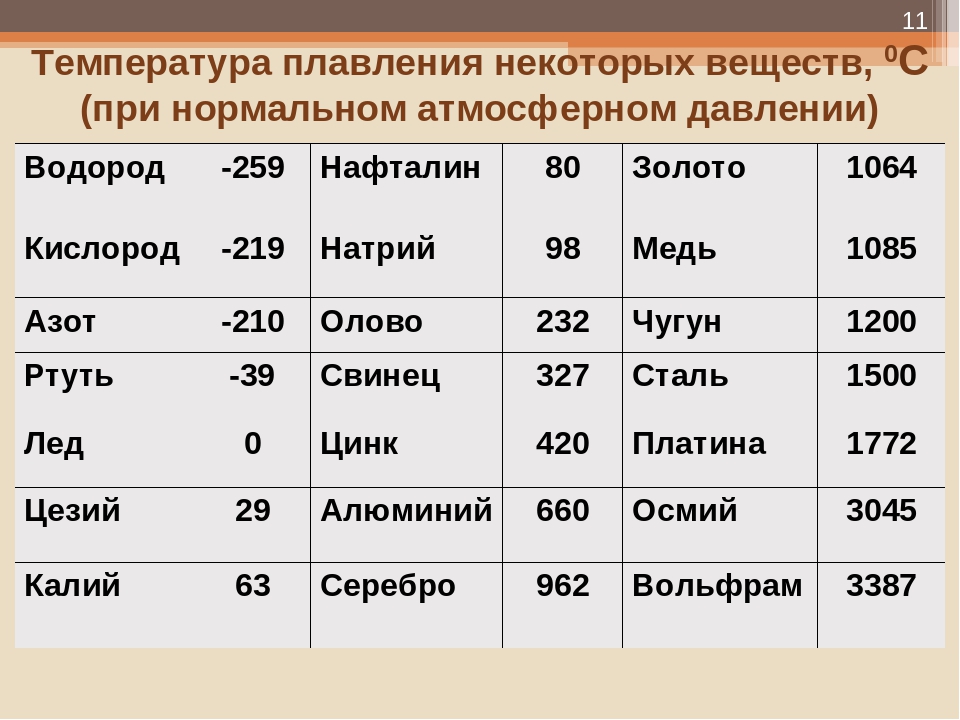
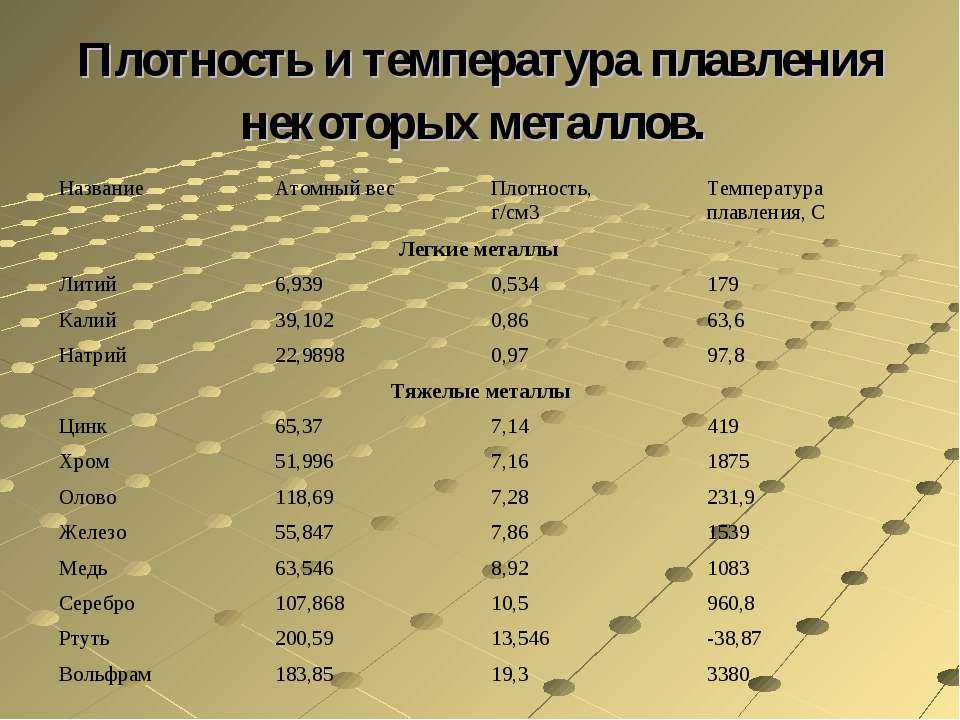
- Температура плавления — 419 градусов по Цельсию. Особенности плавления могут изменяться зависимо от присадок в составе цинка. Высокой пластичности материал достигает при нагревании до 100 градусов.
- Температура закипания — 906 градусов.
- Имеет средний показатель твердости.
- Во время охлаждения металл крошится.

- Плотность — 7,133 г/см3.
Механические свойства цинка не подходят для изготовления из него износоустойчивых деталей. Относительно нормальных условий эксплуатации он легко ломается, не устойчив к ударам, большим физическим нагрузкам.
Химические
На химические свойства материала влияют примеси, содержащиеся в его составе. Средние параметры:
- При снижении температур теряет блеск, покрывается оксидной плёнкой.
- Разрушается при длительном воздействии влажного воздуха.
- Активный металл, который относится к энергетическим восстановителям.
- Гидроизолируется при нагревании металла в воде. Во время этого процесса образуется белый осадок.
- Растворяется в мощных минеральных кислотах.
От процентного содержание примесей сторонних металлов зависит воздействие щелочей, кислот на материал.
Области применения
Используют цинк в различных сферах промышленности. Говоря о популярности этого материала относительно мирового масштаба, он стоит на третьем место по добыче среди других цветных металлов. Сферы применения:
Сферы применения:
- Металлургия — используется как защитное покрытие от коррозий для металлоконструкций. Защищает основу первым контактируя с агрессивными факторами окружающей среды. Используется при производстве стали.
- Ювелирное дело — применяется для восстановления золота и серебра после их добычи.
- Пиротехника — применяется при создании красителей для фейерверков.
- Используется при печати изображений в типографии.
- Медицина — цинк считается качественным антисептиком, добавляется в разные мази, зубные пасты.
Содержится в организме человека, продуктах питания.
С помощью цинка синтезируются различные гормоны, улучшается метаболизм витаминов, расщепляются остатки алкоголя в организме, улучшается работу простаты.
Металлургия
Содержание в природе
В природе нельзя найти чистый цинк. Его добывают из руд, которые содержат примеси других металлов. Основными месторождениями материала являются Россия, Иран, Боливия, Австралия, Казахстан.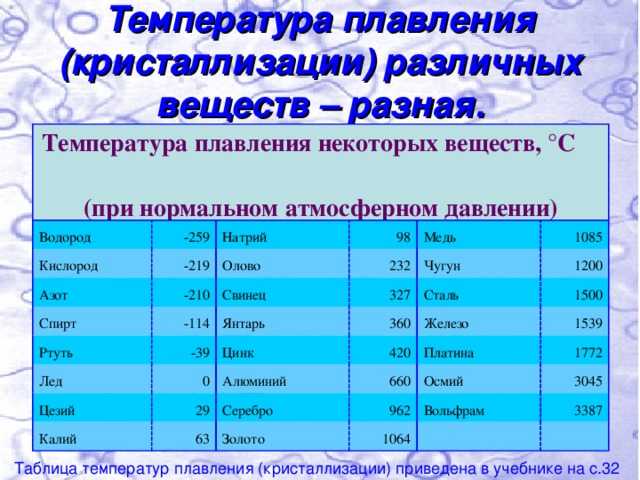
Историческая справка
Сплавы на основе цинка с добавлением латуни, меди известны давно. Они применялись в Древнем Египте, Индии, Древней Греции. Только к 1738 году люди научились получать более чистый металл. Для этого применялся дистилляционный способ. К 19 веку мастера металлургии научились получать чистый цинк с помощью технологического процесса прокатки.
Производство
Чтобы получить чистый материал, применяется две технологии:
- Электролитический метод. Масса, полученная из руды, помещается в ёмкость, заполненную серной кислотой. Через раствор пропускают ток. Металл отделяется от примесей. Далее его запекают с помощью промышленных печей.
- Пирометаллургический метод. Сначала проводится обжиг. Далее применяется коксовый уголь для восстановления готовой массы. Последний этапом является процесс отстаивания.
Во время обжига руды выделяется газ, который содержит большое количество серы. Его используют для создания серной кислоты.
youtube.com/embed/McEmVMSY44Y» frameborder=»0″ allowfullscreen=»allowfullscreen»>
( Пока оценок нет )
Поделиться
химические и физические, история получения и применение, температура плавления и плотность
Цинк — хрупкий металл белого цвета с голубым оттенком. На воздухе покрывается тонкой оксидной плёнкой. Латунь (медно-цинковый сплав) использовали ещё до нашей эры в Древней Греции и Древнем Египте. На сегодняшний день цинк — один из самых важных для многих отраслей человеческой деятельности. Он незаменим в промышленности, медицине. Важен для нормального функционирования человеческого организма
- Химические и физические свойства и история металла
- Месторождения и получение
- Свойства металла и использование в производстве
- Содержание в организме человека и продуктах питания
Химические и физические свойства и история металла
Несмотря на использование с давних времён в различных целях, чистый цинк получить никак не удавалось.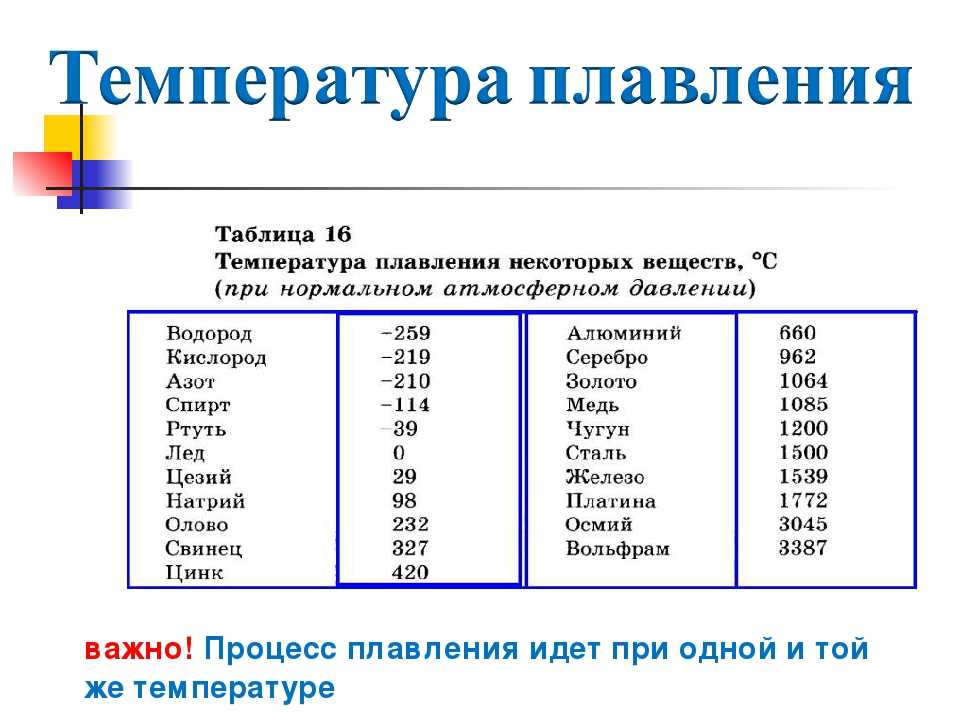 Только в начале восемнадцатого века Уильям Чемпион сумел открыть способ выделения этот элемент из руды с помощью дистилляции. В 1838 году он запатентовал своё открытие, а спустя 5 лет, в 1843 году, Уильямом Чемпионом был запущен первый в истории завод по выплавке этого металла. Спустя некоторое время Андреас Сигизмунд Маргграф открыл ещё один метод. Этот способ был признан более совершенным. Поэтому именно Маргграфа зачастую считают открывателем чистого цинка. Последующие открытия только поспособствовали расширению его популярности.
Только в начале восемнадцатого века Уильям Чемпион сумел открыть способ выделения этот элемент из руды с помощью дистилляции. В 1838 году он запатентовал своё открытие, а спустя 5 лет, в 1843 году, Уильямом Чемпионом был запущен первый в истории завод по выплавке этого металла. Спустя некоторое время Андреас Сигизмунд Маргграф открыл ещё один метод. Этот способ был признан более совершенным. Поэтому именно Маргграфа зачастую считают открывателем чистого цинка. Последующие открытия только поспособствовали расширению его популярности.
Месторождения и получение
Самородного цинка в природе не существует. Сегодня используется около 70 минералов, из которых его выплавляют. Самый известный — сфалерит (цинковая обманка), который содержится в незначительных количествах в организме человека и животных, а также в некоторых растениях. Больше всего — в фиалке.
Цинковые минералы добывают в Казахстане, Боливии, Австралии, Иране, России. Лидеры по производству — Китай, Австралия, Перу, США, Канада, Мексика, Ирландия, Индия.
Лидеры по производству — Китай, Австралия, Перу, США, Канада, Мексика, Ирландия, Индия.
На сегодняшний день самый популярный метод получения чистого металла — электролитический. Чистота получаемого металла почти стопроцентная (возможны лишь небольшие примеси в объёме не более нескольких сотых процента. В целом они незначительны, поэтому такой цинк считается чистым).
Общее производство цинка во всём мире оценивается примерно в более чем десять миллионов тонн в год.
Свойства металла и использование в производстве
Цвет чистого металла — серебристо-белый. Довольно хрупок при температуре двадцать-двадцать пять градусов (т.е. комнатной), особенно если содержит примеси. При нагревании до 100 — 150 градусов по Цельсию металл становится пластичным и ковким. При разогревании выше чем сто-сто пятьдесят градусов хрупкость опять возвращается.
youtube.com/embed/4F7zp7rzWlM»>
- Температура плавления цинка — 907 градусов по Цельсию.
- Относительная атомная масса цинка — 65,38 а. е. м. ± 0,002 а. е. м.
- Плотность цинка — 7,14 г/см3.
Металл цинк занимает четвертое место по использованию в различных сферах производства:
- Он применяется при добыче и обработке золотой и серебряной руды.
- Оцинковка защищает сталь от коррозии.
- Важную роль металл играет в батарейках и аккумуляторах.
- С помощью цинковых пластинок печатаются иллюстрации в журналах и книгах.
- В медицине цинковая окись используется как антисептик.
- Применяется в автомопроизводстве.
Содержание в организме человека и продуктах питания
Организм человека обычно содержит около двух граммов цинка. Многие ферменты содержат в себе этот металл. Элемент играет роль в синтезе важных гормонов, таких как тестостерон и инсулин. Элемент крайне необходим для полноценного функционирования мужских половых органов. Кстати, он даже помогает нам справиться с сильным похмельем. С его помощью выводится из нашего организма лишний алкоголь.
Элемент играет роль в синтезе важных гормонов, таких как тестостерон и инсулин. Элемент крайне необходим для полноценного функционирования мужских половых органов. Кстати, он даже помогает нам справиться с сильным похмельем. С его помощью выводится из нашего организма лишний алкоголь.
Недостаток цинка в рационе может привести к множеству нарушений функций организма. Такие люди подвержены депрессии, постоянной усталости, нервозности. Дневная норма для взрослого мужчины — 11 миллиграммов в день, для женщины — 8 миллиграмм.
Содержание в продуктах (в миллиграммах на 100 грамм продукта):
- устрицы — 40 мг;
- отруби — 16 мг;
- семена тыквы — 10 ;
- печень говяжья — 8 мг;
- говядина — 8 мг;
- баранина — 6 мг;
- семена подсолнуха — 5 мг;
- сыр — 4 мг;
- овёс — 4 мг;
- курица — 3 мг;
- орехи грецкие — 3 мг;
- фасоль — 3 мг;
- свинина — 3 мг;
- шоколад — 2 мг;
- кукуруза — 0,5 мг;
- бананы — 0,15 мг.

Избыток элемента в человеческом организме также приводит к серьёзным проблемам, поэтому не стоит хранить продукты в цинковой посуде.
Хранение радиоактивных материалов
Периодическая таблица Table Home
С тех пор как в августе 2003 года вышла моя научно-популярная статья о цинковом литье, я получил несколько
вопросы о том, действительно ли литье цинка безопасно, и несколько человек сказали мне, что это не так,
включая уважаемого профессора химии, который назвал меня «глупым» за рекомендацию цинка в качестве
литейный металл на том основании, что его использование вызовет серьезные проблемы со здоровьем.
Однако это не так: расплавленный чистый цинк не вызывает проблем со здоровьем, кроме очевидных
горит, если облить себя.
Есть два основных пути, по которым люди думают, что цинковое литье представляет опасность для здоровья:
Сварка оцинкованной (оцинкованной) стали и литье из латуни (медно-цинковый сплав).
Оба эти действия могут вызвать у вас тошноту от вдыхания паров оксида цинка, поэтому люди
озабоченность по поводу литья цинка не лишена оснований. Но эти действия различаются
важные пути отливки чистого цинка.
При оценке любого риска я всегда хотел бы сначала спросить, что самое худшее, что может случиться?
может случиться? В случае плавления свинца, например, ответ довольно мрачный: даже
небольшое количество свинца в организме может вызвать серьезные, долгосрочные неврологические повреждения
или, возможно, рак. Особенно для детей воздействие едва обнаруживаемых уровней
свинец тесно связан с повреждением головного мозга. Вы не хотите возиться со свинцом.
Следующий вопрос: существуют ли невидимые кумулятивные эффекты, которые могут причинить вам вред
без вашего ведома об этом, пока не стало слишком поздно. Например, горячая печь либо горит
вы или нет: если вы закончите готовить, не обжегшись, вы можете быть уверены,
что через неделю не проснешься с ожогом. Загар отличается: вы можете загореть
себя в течение многих лет, не болея, а затем внезапно обнаруживаете, что у вас рак кожи.
Свинец — еще один пример того, что оказывает невидимое долгосрочное вредное воздействие.
Так что же самое худшее может произойти от воздействия цинка, и может ли это вызвать скрытые долгосрочные
последствия?
При нагревании цинка до высокой температуры (при температуре кипения около 900°С или выше)
он горит и образует дым оксида цинка.
Как и любой дым, оксид цинка раздражает легкие, что приводит к затруднению дыхания:
Это неопасная ситуация, и она сразу же проясняется, когда вы уходите от
источник дыма. Люди, подвергающиеся воздействию высоких концентраций оксида цинка в течение длительного периода времени, могут
также развивается состояние, известное как «цинковый озноб», «лихорадка металлического дыма», «лихорадка медных литейщиков» или ряд
другие красочные термины. Это включает лихорадку, тремор и другие неприятные симптомы.
Однако лихорадка металлического дыма, которая редко встречается в наши дни, является чисто временным состоянием.
который проходит без каких-либо известных долгосрочных эффектов или осложнений. Смеяться точно не над чем
Смеяться точно не над чем
около, но максимальным недостатком воздействия цинка является лихорадка и озноб, которые проходят
и тогда вы поправляетесь. Это не похоже на свинцовый или солнечный загар, который может быть опасным для жизни.
последствия в будущем, или как угарный газ, который может убить вас на месте.
И вы даже не можете получить цинковый холод от плавления и литья чистого цинка.
При сварке оцинкованной стали образуются пары цинка, так как сварка происходит при очень, очень высоких температурах.
температуры: цинковое покрытие на дюйм или около того в каждом направлении от сварного шва
сгорел в клубящихся белых облаках оксида цинка. Тот, кто научился сваривать,
много раз предупреждали о необходимости носить специальную маску при сварке оцинкованной стали,
и это хорошая идея. Я всегда использую один при сварке оцинкованного листа.
При плавлении латуни (медно-цинкового сплава) также образуется большое количество паров оксида цинка,
потому что температура плавления латуни высока, близка к температуре кипения цинка. Фактически,
Фактически,
парциальное давление паров цинка над котлом с расплавленной латунью может составлять почти половину атмосферы!
Неудивительно, что такой котел испускает большое количество сине-белого дыма оксида цинка.
Но ситуация с кастрюлей с расплавленным чистым цинком при температуре плавления около 420°C очень
другой. Парциальное давление паров цинка над только что расплавленным цинком равно
примерно в 2500 раз ниже температуры плавления типичных латунных сплавов.
И котел с расплавленным цинком быстро образует корку из твердого шлака оксида цинка, что, вероятно,
снижает фактическое давление паров цинка до нуля, за исключением случаев, когда металл
только что перемешанный или вылитый (и тогда это все еще только 1/2500 количества, полученного литьем из латуни).
Пары оксида цинка очень легко увидеть: они представляют собой ярко-белые или сине-белые частицы
дым, видимый даже при очень низких концентрациях. Я видел, как создается оксид цинка
различными способами, включая сварку, обжиг металлического цинка паяльной лампой, перегрев
горшка с цинком и т. д. Я даже видел оксид цинка, полученный при плавлении цинка в микроволновой печи.
д. Я даже видел оксид цинка, полученный при плавлении цинка в микроволновой печи.
Но за все годы литья цинка я ни разу не видел дыма оксида цинка, исходящего из горшка.
цинка, расплавленного на электрической плите. Просто так не бывает, потому что температуры нет
достаточно высок.
Возможно, небольшая концентрация оксида цинка образуется ниже
порог видимости. Если бы это был свинец или оксид свинца, это было бы проблемой,
потому что вдыхать даже небольшое количество свинца действительно вредно. Но это явно
дело не в цинке. Вдыхание малых концентраций цинка не вызывает
долгосрочные или постепенные эффекты. Не накапливается в крови и нервной системе.
как свинец может. Если вы не чувствуете немедленного неприятного эффекта от того, что вы
делаете с цинком, то это не приносит вам никакого вреда.
На основании этих фактов я абсолютно убежден, как и ряд экспертов
химиков, металлургов и литейщиков, с которыми я консультировался, что плавление чистого цинка или
сплавы, содержащие цинк (но не свинец), которые плавятся при температуре около 450°С или ниже,
не представляет опасности для здоровья при вдыхании паров цинка.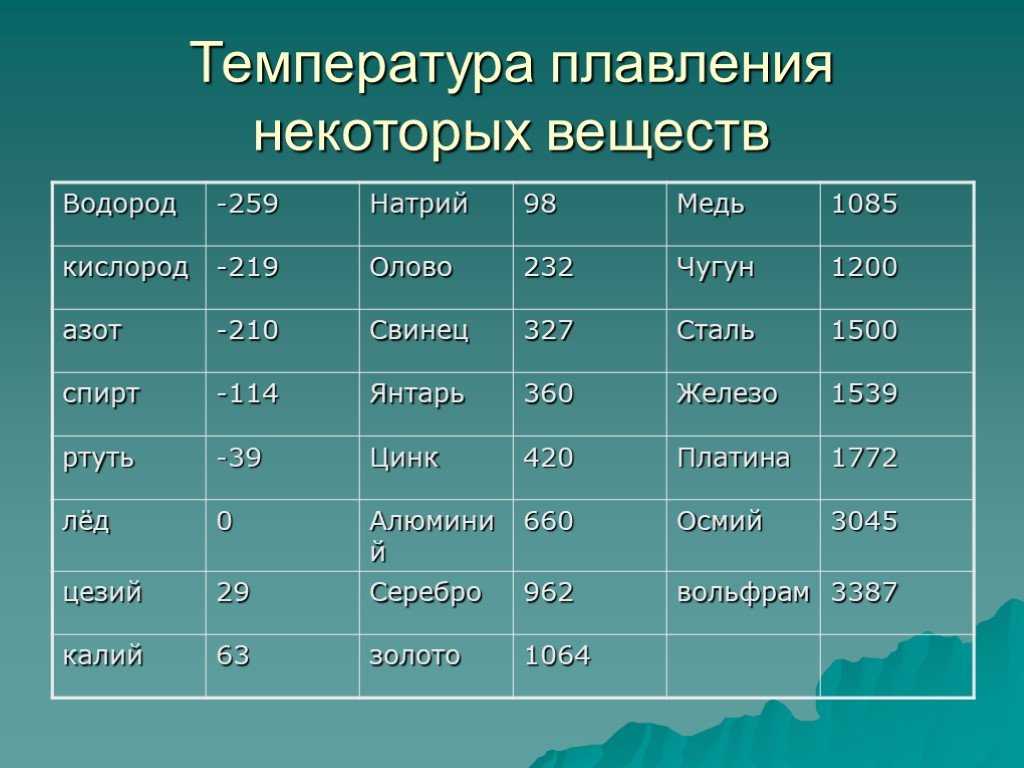 Да, вы можете определенно
Да, вы можете определенно
очень сильно обожжетесь, если прольете его, но это предел того, что вы
надо побеспокоиться.
Таблица Менделеева Главная
Факты о цинке (внешний вид, свойства и многое другое)
Пожалуйста, напишите или поделитесь этой статьей!
Электронная почта
ФБ
Цинк — переходный металл, находящийся в первой строке двенадцатого столбца периодической таблицы элементов.
Атомный номер цинка равен 30, так как он содержит 30 протонов, 30 электронов и 34 нейтрона.
Химический символ цинка — Zn, а его атомный вес — 65,38.
При комнатной температуре цинк выглядит как твердый металл, хотя его температура плавления составляет 419 градусов Цельсия, а температура кипения — 907 градусов Цельсия.
Характеристики и свойства
В своей стандартной, наиболее типичной форме цинк представляет собой твердый хрупкий металл сине-белого цвета, очень похожий на кобальт.
Кобальт
Однако хрупкость цинка переходит в более податливое, подвижное вещество всего лишь при 100 градусах Цельсия.
Большинство металлов имеют очень высокие температуры плавления и кипения, обычно выше 1000 градусов Цельсия. Тем не менее, температуры плавления и кипения цинка, как правило, примерно вдвое ниже, чем у металлов.
Таким образом, несмотря на то, что цинк может сохранять свою структуру и свойства при достаточно высоких температурах, он подвергается воздействию гораздо раньше, чем это наблюдается в других металлах.
Цинк также является относительно хорошим проводником электричества.
Вступает в реакцию при контакте с двуокисью углерода в воздухе: образуется карбонат цинка, который защищает цинк от коррозии под действием других элементов.
Однако цинк не вступает в реакцию при контакте с чистым кислородом, хотя он определенно будет реагировать на большинство типов кислот: известно, что он растворяется в большинстве типов кислот и даже в некоторых основаниях.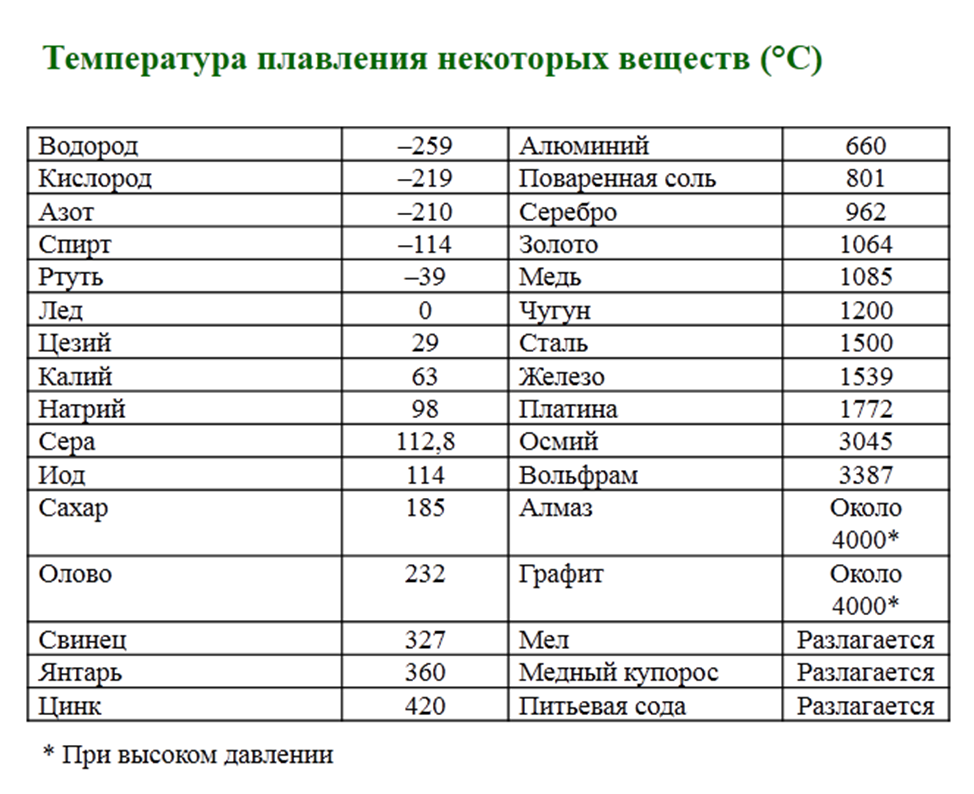
История
Интересно, что цинк использовался людьми со времен древних цивилизаций, и поэтому он использовался так долго, что мы не знаем, кто первым открыл цинк и когда это было.
Цинк можно найти среди других минералов во внешнем слое земной коры.
Однако, в отличие от кобальта и меди, он не встречается в чистом виде без предварительной очистки от других металлов.
Интересно, что цинк является двадцать четвертым по распространенности элементом на Земле, и небольшое количество его можно обнаружить в атмосфере Земли и в океане.
Цинк также можно добывать для использования человеком, а страны, которые добывают и распространяют больше всего цинка, включают Китай, Австралию и Перу.
Как цинк используется сегодня
Большая часть цинка, специально добываемого для использования, в основном используется для изготовления других инструментов из других металлов.
Фактически, цинк обычно используется для гальванизации стали и железа, а это означает, что цинк используется для покрытия и защиты других металлов, чтобы эти инструменты не ржавели и не подвергались коррозии.