Выяснение расположения меди в организме человека. Молекулы меди
Химические свойства и роль меди в организме - Биохимия меди - Молекулы и клетки
Дело в том, что химические свойства, благодаря которым медь играет столь важную роль в процессах обмена веществ в организме, выражены у нее в большей степени, чем у других металлов. Во-первых, ионы меди по сравнению с ионами других металлов активнее реагируют с аминокислотами и белками и поэтому медь образует с биологически активными веществами наиболее устойчивые комплексы (так называемые клешневидные, или хелатные, комплексы).
Например, в некоторых медьсодержащих ферментах ион меди связан настолько прочно, что не удаляется из белка даже при диализе (при диализе малые молекулы удаляются из раствора благодаря их избирательному прохождению через полупроницаемую мембрану). Ион меди может быть удален лишь путем сильного изменения структуры белка или может быть замещен агентом, образующим еще более прочную хелатную связь. Во-вторых, медь служит исключительно эффективным катализатором. Ион меди является, пожалуй, наиболее разносторонним катализатором из всех элементов, а в сочетании с белком его каталитическое действие еще более усиливается и приобретает сверх того специфичность, необходимую для работы медьсодержащих ферментов. В-третьих, медь легко переходит из одного валентного состояния в другое, что особенно благоприятствует ее метаболическим функциям (смотрите рисунок ниже).
Валентные состояния железа и меди
Обоим металлам в равной степени присущи два валентных состояния, чем и обусловлена их важная роль в обмене веществ. Атом меди может терять один или два электрона, в результате чего он становится одно- или двухвалентным. Та легкость, с которой двухвалентный ион Сu2+ приобретает электрон, расширяет каталитические возможности меди. Например, при окислении какого-либо субстрата ион Сu2+ временно приобретает электрон, а затем возвращается в прежнее состояние, отдавая электрон кислороду (см. рис. 4).
Обычно медь может находиться в трех состояниях: в виде свободных нейтральных атомов, в виде одновалентных ионов (когда недостает одного электрона) или в виде двухвалентных ионов (когда не хватает двух электронов).
Одни ионы, приобретая или теряя электрон, легко превращаются в другие. Поэтому в зависимости от обстоятельств ион меди может служить как донором, так и акцептором электронов. Кроме того, соединения, содержащие одновалентную медь, легко окисляются кислородом воздуха. Поэтому медьсодержащие ферменты, катализирующие процессы окисления (присоединение кислорода к субстрату), могут и сами быстро окисляться, в результате чего их функция восстанавливается.
«Молекулы и клетки», под ред. акад. Г.М.Франка
Популярные статьи разделаwww.medchitalka.ru
Медь в периодической таблице - Биохимия меди - Молекулы и клетки
Медь принадлежит к элементам первой переходной группы (смотрите рисунок ниже), которые в периодической таблице имеют номера с 21-го по 30-й.
Элементы первой переходной группы, в которую входит и медь
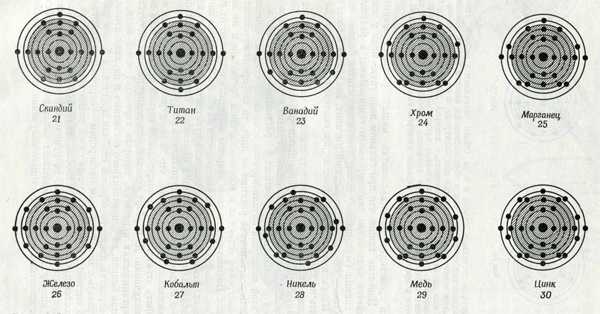
Элементы первой переходной группы, в которую входит и медь, различаются только числом электронов на lвух внешних электронных оболочках; поэтому все они имеют много общих физических и химических свойств. Среди элементов этой группы находится ряд металлов, играющих важную роль в процессах жизнедеятельности. В их число, помимо меди, входят марганец, железо, кобальт, цинк и, возможно, еще ванадий и хром. Хотя у них много общих свойств, каждый металл высокоспецифичен по своим биологическим функциям.
В эту группу входят скандий, титан, ванадий, хром, марганец, железо, кобальт, никель, медь и цинк. Они различаются только числом электронов на Зd-оболочке и имеют много общих физических и химических свойств. Некоторые из них в той или иной степени обладают теми важными свойствами, которые определяют ключевую роль меди в биологических процессах, и поэтому тоже входят в число биологических микроэлементов. Однако каждый из этих металлов выполняет свои специфические химические функции.
Биологическая роль меди многообразна, и установить ее не всегда легко. Одна из причин сравнительно позднего обнаружения меди в живых организмах связана с тем, что животные очень редко испытывают недостаток меди, а у человека таких случаев и вовсе не наблюдалось. Меди всегда много в пище и в питьевой воде, чему в немалой степени способствует употребление медной посуды. Избыток меди для организма вреден — вероятно, здесь решающую роль играет реакция ионов меди с сульфгидрильными группами ферментов, ведущая к утрате ферментативной активности. К счастью, в организме имеются специальные защитные механизмы, которые ограничивают всасывание меди и других металлов.
Последствия недостатка меди в организме изучались на животных, у которых такая недостаточность изредка встречается в естественных условиях (на собаках, ягнятах, свиньях, цыплятах), а также на лабораторных животных. Выяснилось, что при сильном недостатке меди у ягнят развивается атаксия (нарушение координации движений), у собак, свиней и цыплят нарушается развитие костей, а у овец и крыс обесцвечивается шерсть. Атаксия обусловлена рассасыванием белого вещества спинного мозга; в отсутствие меди животные утрачивают способность синтезировать фосфолипиды, образующие наружную оболочку нервного волокна. Обесцвечивание шерсти происходит из-за недостатка медьсодержащего фермента тирозиназы.
Известно также, что при сильном недостатке меди у животных уменьшается количество синтезируемого гемоглобина; в результате развивается анемия (малокровие) и ощущается недостаток белков, содержащих гем (гем — это железосодержащий пигмент, входящий в состав гемоглобина). Какую именно роль играет медь в синтезе гемоглобина, до сих пор установить не удалось.
«Молекулы и клетки», под ред. акад. Г.М.Франка
Популярные статьи разделаwww.medchitalka.ru
Масло сравнительно легко удаляется с чистой поверхности меди. Удалить ртуть с той же поверхности невозможно.
Масло смачивает медь, а ртуть растворяет - амальгама получается. Удаляется нагреванием, - ртуть испаряется.
а масло какое? подсолнечное, оливковое? Вместо ртути лучше поперчить побольше...
ну, во первых, мне кажеться молекулы масла слишком большие чтобы взаимодействовать с медью (дифуззия не возникает) , а вот ртуть вполне может просочиться в пространство между молекулами меди и начать с ними взаимодействоать. Ну а что можно сказать по этому поводу, так ответ уже содержиться в вопросе, то что взаимодеиствие между молекулами меди и ртути сильное а между молекулами масла и меди очень слабое.
Да, притяжение молекл ртути и меди может конечно и больше, но дело не совсем в этом. дело в том что это 2 металла. и ртуть проникнет в медь. образовав сплав даже при комнатной температуре. образуется амальгама меди. так же ртуть образует сплавы с золотом серебром. легко и непринужденно.
Да, притяжение молекл ртути и меди может конечно и больше, но дело не совсем в этом. дело в том что это 2 металла. и ртуть проникнет в медь. образовав сплав даже при комнатной температуре. образуется амальгама меди. так же ртуть образует сплавы с золотом серебром. лег ну, во первых, мне кажеться молекулы масла слишком большие чтобы взаимодействовать с медью (дифуззия не возникает) , а вот ртуть вполне может просочиться в пространство между молекулами меди и начать с ними взаимодействоать. Ну а что можно сказать по этому поводу, так ответ уже содержиться в вопросе, то что взаимодеиствие между молекулами меди и ртути сильное а между молекулами масла и меди очень слабое.
touch.otvet.mail.ru
Молекулы Никель – Медь – Молибденовой группы Попков И
Рисунки молекул новой периодической таблицы химических элементовМолекулы Никель – Медь – Молибденовой группы Попков И. И.Резюме: Работа посвящена новой периодической
системе химических элементов
Figures of molecules of a new periodic table of chemical elements
Molecules of Nickel - Copper - Molybdenum group Popkov I.I.The resume: Work is devoted to new periodic system
of chemical elements
С О Д Е Р Ж А Н И ЕНикель – Медь – Молибденовая группа молекул
- Молекула Никеля, состоящая из 88 атомов.………………………стр.1
- Молекула Меди, состоящая из 89 атомов.………………………стр.2-4
- Молекула Эрбия, состоящая из 90 атомов.…………………….…стр.5-6
- Молекула Эйнштейния, состоящая из 91 атома.…….……………стр.7
- Молекула Туллия, состоящая из 92 атомов.………………………стр.8
- Молекула Полония, состоящая из 93 атомов.………………………стр.9
- Молекула Лютеция, состоящая из 94 атомов.………………..…..стр.10
- Молекула Фермия, состоящая из 95 атомов.……………….…..…стр.11
- Молекула Висмута, состоящая из 96 атомов.………………..……стр.12
- Молекула Актиния, состоящая из 97 атомов.……………….……стр.13
- Молекула Молибдена, состоящая из 98 атомов.……………..стр.14-16
Рис. 1
Молекула Никеля - Ni
88 Атомов
Рис. 2
Молекула Меди - Сu
89 Атомов/ 88+1/
www.birmaga.ru
Молекулы Никель – Медь – Молибденовой группы Попков И
Рисунки молекул новой периодической таблицы химических элементовМолекулы Никель – Медь – Молибденовой группы Попков И. И.Резюме: Работа посвящена новой периодической
системе химических элементов
Figures of molecules of a new periodic table of chemical elements
Molecules of Nickel - Copper - Molybdenum group Popkov I.I.The resume: Work is devoted to new periodic system
of chemical elements
С О Д Е Р Ж А Н И ЕНикель – Медь – Молибденовая группа молекул
- Молекула Никеля, состоящая из 88 атомов.………………………стр.1
- Молекула Меди, состоящая из 89 атомов.………………………стр.2-4
- Молекула Эрбия, состоящая из 90 атомов.…………………….…стр.5-6
- Молекула Эйнштейния, состоящая из 91 атома.…….……………стр.7
- Молекула Туллия, состоящая из 92 атомов.………………………стр.8
- Молекула Полония, состоящая из 93 атомов.………………………стр.9
- Молекула Лютеция, состоящая из 94 атомов.………………..…..стр.10
- Молекула Фермия, состоящая из 95 атомов.……………….…..…стр.11
- Молекула Висмута, состоящая из 96 атомов.………………..……стр.12
- Молекула Актиния, состоящая из 97 атомов.……………….……стр.13
- Молекула Молибдена, состоящая из 98 атомов.……………..стр.14-16
Рис. 1
Молекула Никеля - Ni
88 Атомов
Рис. 2
Молекула Меди - Сu
89 Атомов/ 88+1/
birmaga.ru
Выяснение расположения меди в организме человека - Биохимия меди - Молекулы и клетки
Где и в каких именно белках присутствует медь, сказать очень трудно. С железом было легче: большая часть железа в организме находится в составе так называемых порфиринов; эти соединения составляют основу структуры красного белка крови гемоглобина и красных цитохромов — важных белков дыхательной системы.
Порфирины — достаточно сложные соединения, но биохимики сумели провести их анализ и выяснили их подробную химическую структуру. С медью дело обстоит сложнее. Она почти никогда не встречается в составе биологических соединений менее сложных, чем белки. Единственный известный медный порфирин — это ярко-красный пигмент турацин, обнаруженный только в крыльях красивой африканской птицы турако. Любопытно, что этот пигмент легко смывается с перьев водой, но перья у турако расположены таким образом, что пигмент защищен от дождя и крылья сохраняют свою окраску.
Впервые в живых организмах медь была обнаружена в составе дыхательных белков крови. Было известно, что некоторые моллюски (улитки, «осьминоги) и некоторые членистоногие (мечехвосты, скорпионы) выделяются среди прочих животных голубым цветом крови. (Стало быть, вот у кого действительно голубая кровь!) В XIX в. исследователи установили, что голубой цвет крови объясняется присутствием в ней медьсодержащего белка, который служит переносчиком кислорода, заменяя привычный для нас гемоглобин (смотрите рисунок ниже).
Способность связывать кислород у гемоглобина (сплошная кривая) меньше,чем у медьсодержащего белка гемоцианина (прерывистая кривая)
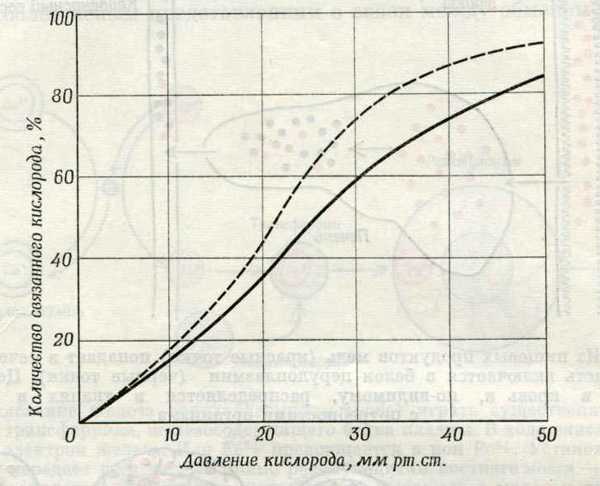
Гемоцианин служит переносчиком кислорода в крови некоторых членистоногих и моллюсков; кровь этих животных голубого цвета. Поскольку концентрация пигмента в крови этих животных ниже, чем у животных с красной кровью, в пересчете на всю кровь способность связывать кислород у животных с красной кровью выше.
Французский биолог Л. Фредерик назвал его гемоцианином (название несколько неудачное, так как в действительности гема в гемоцианине нет).
Гемоцианин довольно легко выделить, и он уже давно является объектом интенсивного изучения. Тем не менее химическая структура этого белка до сих пор неясна. Отчасти дело здесь в том, что гемоцианины относятся к разряду наиболее крупных белков. Молекулярный вес гемоцианинов может составлять от 450 000 до 6 680 000. Естественно, определить структуру такой громоздкой и сложной молекулы очень трудно и тем более нелегко узнать, где в ней расположена медь. Было установлено, что в гемоцианине моллюсков один атом меди приходится на каждые 250 аминокислот, а у членистоногих — на каждые 370 аминокислот.
Чтобы кислород удерживался столь же прочно, как в гемоглобине, в гемоцианине атомы меди должны размещаться парами. Вероятнее всего, медь связана с какими-то определенными аминокислотами, возможно с гистидином, поскольку к гистидину медь имеет сильно выраженное сродство. По-видимому, медь, связанная с белком, может находиться как в одновалентном, так и в двухвалентном состоянии, но получить прямые доказательства этого очень трудно; например, попытки непосредственно обнаружить присутствие неспаренных электронов успеха не дали.
«Молекулы и клетки», под ред. акад. Г.М.Франка
Популярные статьи разделаwww.medchitalka.ru
Чему равна масса (кг) одной молекулы медного купороса CuSO4, если атомные массы меди, серы и кислорода равны соответственно 64, 32
Укажите, в каком из ответов наиболее полно представлены основные положения молекулярно-кинетической теории строения вещества?- вещество состоит из элементарных частиц и они взаимно превращаются друг в друга- вещество состоит из мельчайших частиц и между ними действуют силы(*ответ*) вещество состоит из маленьких частей и они заполняют пространство- все тела состоят из молекул или атомов, которые непрерывно и хаотически движутся, между молекулами и атомами действуют силы притяжения и отталкивания. Какова масса одной молекулы воды (г), если ее молярная масса равна 18 г?- 10-23(*ответ*) 3•10-23- 3•10-24- 10-26 Определите отношение числа молекул в 36 г воды к числу молекул в 2 г водорода.- 0,5- 1(*ответ*) 2- 3 Оцените, во сколько примерно раз среднее расстояние между молекулами в газах при нормальных условиях больше размеров самих молекул газа.- 80-100- 800-1000- 8000-10000(*ответ*) 8-10 Число Авогадро: равно 6,02•1023 моль-1; это число атомов в 12 г углерода; равно числу молекул в одном моле любого вещества; равно числу молекул в 22,4 л любого газа, находящегося при нормальных условиях.- 1 и 2(*ответ*) 1, 2, 3 и 4- 1 и 4- 1, 2 и 3 Средняя кинетическая энергия теплового движения молекул: зависит от температуры; не зависит от температуры; зависит от массы молекул; не зависит от массы молекул; зависит от агрегатного состояния вещества; не зависит от агрегатного состояния вещества.- 2, 3 и5- 1, 3 и 5(*ответ*) 1, 4 и 6- 2, 3 и 6 Во сколько раз увеличится среднеквадратическая скорость молекул идеального газа при повышении абсолютной температуры в 2 раза?- 2√2(*ответ*) √2- 2- 4 Какое количество вещества (ноль) содержится в 144 г воды? ?(Н)=1 а.е.м., ?(O)=16 а.е.м.- 6(*ответ*) 8- 4- 10 При какой температуре (К) среднеквадратическая скорость атомов гелия будет такой же, как и среднеквадратическая скорость молекул водорода при температуре 300 К?- 50- 400- 100(*ответ*) 600 Чему равна масса (кг) одной молекулы медного купороса CuSO4, если атомные массы меди, серы и кислорода равны соответственно 64, 32 и 16 а.е.м., а число Авогадро составляет 6•1023моль-1(*ответ*) 2,67•10-25- 2•10-22- 2•10-23- 26,7•10-23
www.soloby.ru