Большая Энциклопедия Нефти и Газа. Есть у меди металлический блеск
есть ли у меди кристаллическая решетка?? ? по каким признакам это можно утверждать или не утверждать
Нет, нету. Медь - металл и связь между молекулами металлическая.
Медь образует кубическую гранецентрированную решётку, а утверждать это можно, зная правило
Сделайте ренгеновскую фотографию, исследуйте поверхность Ферми. Но проще всего книжку почитать. Поверьте, Вы очень не первый, кто пытается ответить на этот вопрос. Вопрос давно решен и изложен в букварях.
Медь относится к металлам. У металлов металлическая кристаллическая решётка. То есть ядро атомов не подвижно. Электроны образуют общее облако. Об этом свидетельствует металлический блеск. Постоянная температура плавления. Все металлы являются проводниками электрического тока.
Медь, как и другие металлы, относится к поликристаллическим телам, т. е. состоят из множества маленьких кристаллов. Убедиться в этом можно, если посмотреть на излом металла с помощью микроскопа или лупы. Как указывает Павел, определенная температура плавления характерна для кристаллических тел.
Как и у любого металла у меди есть кристаллическая решетка, при условии если этот сплав был получен методами традиционной металлургии (литье, деформация). Так как время остывания позволяет атомов меди занять свои позиции (дальный порядок - т. е. независимо от расточния все атомы расположены строго по законам кристаллографии). Так же существуют сплавы с ближним порядком (аморфные), подучают из тех же металлов но в лабораторных условиях при закалки от жидкого состояния- а вот в оморфных нет строгой ориентации атомов (т. к. скорость остывания не позволяет атомов занять свои позиции). Атомы в аморфных телах расположены хаотически (в амоофных маериалов соотвественно нет кристаллической решетки).
touch.otvet.mail.ru
Характерный металлический блеск - Большая Энциклопедия Нефти и Газа, статья, страница 1
Характерный металлический блеск
Cтраница 1
Характерный металлический блеск обусловлен взаимодействием электромагнитных световых волн со свободными электронами. [2]
Непрозрачность и характерный металлический блеск металлов обусловлены структурой энергетических уровней металлов. В этом случае электрон из валентной зоны, поглощая квант света, переходит в зону проводимости. Свет не отражается, а поглощается. В то же время металлам характерен блеск, который появляется в результате испускания света при возвращении возбужденных светом электронов на более низкие энергетические уровни. [3]
Металлы обладают характерным металлическим блеском в изломе, пластичностью ( ковкостью), а также высокой электро - и теплопроводностью. [4]
Металлы отличаются характерным металлическим блеском, ковкостью, тягучестью, могут прокатываться в листы или вытягиваться в проволоку, обладают хорошей тепло - и электропроводностью. При комнатной температуре все металлы ( кроме ртути) находятся в твердом состоянии. [5]
Металлы обладают характерным металлическим блеском; кроме того, они хорошо проводят тепло и электрический ток. [6]
Металлы отличаются характерным металлическим блеском, ковкостью, тягучестью, могут прокатываться в листы или вытягиваться в проволоку, обладают хорошей тепло - и электропроводностью. При комнатной температуре все металлы ( кроме ртути) находятся в твердом состоянии. [7]
Металлы отличаются характерным металлическим блеском, ковкостью, тягучестью, могут прокатываться в листы или вытягиваться в проволоку, обладают хорошей теплопроводностью и электрической проводимостью. При комнатной температуре все металлы ( кроме ртути) находятся в твердом состоянии. [8]
Радий обладает характерным металлическим блеском, быстро исчезающим под действием воздуха. Возможно, на воздухе поверхность радия покрывается пленкой нитрида радия. Металлический радий разлагает воду с образованием гидроокиси и выделением водорода. [9]
Металлы отличаются характерным металлическим блеском, ковкостью, тягучестью, могут прокатываться в листы или вытягиваться в проволоку, обладают хорошей тепло - и электропроводностью. При комнатной температуре все металлы ( кроме ртути) находятся в твердом состоянии. [10]
Металлы отличаются характерным металлическим блеском, ковкостью, тягучестью, могут прокатываться в листы или вытягиваться в проволоку, обладают хорошей теплопроводностью и электрической проводимостью. При комнатной температуре все металлы ( кроме ртути) находятся в твердом состоянии. [11]
Все металлы обладают характерным металлическим блеском, хорошо проводят тепло и электричество, все они, кроме ртути, при обычной температуре - твердые и большинство из них сравнительно легко куются. [13]
Цвет свиниово-серый с характерным металлическим блеском. [14]
В свободном состоянии металлы обладают характерным металлическим блеском, хорошо проводят тепло и электрический ток, куются, вытягиваются в проволоку, прокатываются в листы и вообще легко меняют свою форму при механических воздействиях. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
Металлы
 У всех металлов есть общие физические свойства, например блеск и электропроводность, однако в зависимости от химических свойств они делятся на несколько групп. Такие металлы, как калий и натрий, очень активны и мгновенно вступают в реакции с водой и воздухом, в то время как золото вообще не вступает в реакции. На рисунке изображена золотая маска царя Микен (см. статью «Загадочные жители Греции»)
У всех металлов есть общие физические свойства, например блеск и электропроводность, однако в зависимости от химических свойств они делятся на несколько групп. Такие металлы, как калий и натрий, очень активны и мгновенно вступают в реакции с водой и воздухом, в то время как золото вообще не вступает в реакции. На рисунке изображена золотая маска царя Микен (см. статью «Загадочные жители Греции»)
Свойства металлов
При комнатной температуре (20 °С) все металлы, кроме ртути, пребывают в твердом состоянии и хорошо проводят тепло и электричество. На срезе металлы блестят и некоторые, как железо и никель, обладают магнитными свойствами. Многие металлы пластичны — из них можно делать проволоку — и ковки — им несложно придать другую форму.
Благородные металлы
Благородные металлы в земной коре встречаются в чистом виде, а не в составе соединений. К ним относятся медь, серебро, золото и платина. Они химически пассивны и с трудом вступают в химические реакции с другими элементами. Медь — благородный металл. Золото — один из самых инертных элементов. Из-за своей инертности благородные металлы не подвержены коррозии, поэтому из них делают украшения и монеты. Золото настолько инертно, что древние золотые изделия до сих пор ярко сияют.
Щелочные металлы
Группу 1 в периодической таблице составляют 6 очень активных металлов, в т.ч. натрий и калий. Они плавятся при сравнительно низкой температуре (температура плавления калия 64 °С) и настолько мягкие, что их можно резать ножом. Вступая в реакцию с водой, эти металлы образуют щелочной раствор и поэтому называются щелочными. Калий бурно реагирует с водой. При этом выделяется водород, который сгорает сиреневым пламенем.
Щелочноземельные металлы
Шесть металлов, составляющих 2-ю группу периодической таблицы (в т.ч. магний и кальций), называются щелочноземельными. Эти металлы входят в состав множества минералов. Так, кальций имеется в кальците, прожилки которого можно обнаружить в известняке и меле. Щелочноземельные металлы менее активны, чем щелочные, они тверже и плавятся при более высокой температуре. Кальций содержится в ракушках, костях и губках. Магний входит в состав хлорофилла, зеленого пигмента, необходимого для фотосинтеза.
Металлы 3-й и 4-й групп
Семь металлов этих групп расположены в периодической таблице справа от переходных металлов. Алюминий — один из наименее плотных металлов, поэтому он легкий. А вот свинец очень плотный; из него делают экраны, защищающие от рентгеновских лучей. Все эти металлы довольно мягкие и плавятся при относительно низкой температуре. Многие из них используются в сплавах — создаваемых с определенными целями смесях металлов. Велосипеды и самолеты делают из алюминиевых сплавов.
Переходные металлы
Переходные металлы обладают типично металлическими свойствами. Они прочные, твердые, блестящие и плавятся при высоких температурах. Они менее активны, чем щелочные и щелочноземельные металлы. К ним относятся железо, золото, серебро, хром, никель, медь. Они все ковкие и широко применяются в промышленности — как в чистом виде, так и в виде сплавов. Около 77% от массы автомобиля составляют металлы, в основном сталь, т.е. сплав железа и углерода (см. статью «Железо, сталь и прочие металлы«). Ступицы колес делают из хромированной стали — для блеска и предохранения от коррозии. Корпус машины сделан из листовой стали. Стальные бамперы предохраняют автомобиль в случае столкновения.
Ряд активности
Положение металла в ряду активности показывает, насколько охотно металл вступает в реакции. Чем более активен металл, тем легче он отнимает кислород у менее активных металлов. Активные металлы трудно выделить из соединений, тогда как малоактивные металлы встречаются в чистом виде. Калий и натрий хранят в керосине, так как они моментально вступают в реакции с водой и воздухом. Медь – наименее активный металл из числа недорогих. Она используется в производстве труб, резервуаров для горячей воды и электрических проводов.
Металлы и пламя
Некоторые металлы, если поднести их к огню, придают пламени определенный оттенок. По цвету пламени можно определить присутствие в соединении того или иного металла. Для этого крупинку вещества помешают в пламя на конце проволоки из инертной платины. Соединении натрия окрашивают пламя в желтый цвет, соединения меди — в сине-зеленый, соединении кальции — в красный, и калия — в сиреневый. В состав фейерверков входят разные металлы, сообщающие пламени разные оттенки. Барий дает зеленый цвет, стронций — красный, натрий — желтый, а медь — сине-зеленый.
Коррозия
Коррозия — это химическая реакция, происходящая при контакте металла с воздухом или водой. Металл взаимодействует с кислородом воздуха, и на его поверхности образуется оксид. Металл теряет блеск и покрывается налетом. Высокоактивные металлы подвергаются коррозии быстрее, чем менее активные. Рыцари смазывали стальные доспехи маслом или воском, чтобы они не ржавели (сталь содержит много железа). Для предохранения от ржавчины стальной корпус автомобиля покрывают несколькими слоями краски. Некоторые металлы (например, алюминий) покрываются защищающей их плотной оксидной пленкой. Железо при коррозии образует неплотную пленку оксида, которая при реакции с водой дает ржавчину. Слой ржавчины легко осыпается, и процесс коррозии распространяется вглубь. Для предохранения от коррозии стальные консервные банки покрывают слоем олова — менее активного металла. Крупные сооружения, например мосты, спасает от коррозии краска. Движущиеся части машин, например велосипедные цепи, смазывают маслом, чтобы спасти от коррозии.
Способ предохранения стали от коррозии путем покрытия слоем цинка называется гальванизацией. Цинк активнее стати, поэтому он «оттягивает» от нее кислород. Даже если цинковый слой поцарапается, кислород воздуха будет быстрее взаимодействовать с цинком, чем с железом. Для зашиты судов от коррозии к их корпусам прикрепляют блоки цинка или магния, которые корродируют сами, но защищают судно. Для дополнительной защиты от коррозии стальные листы корпуса автомобилей чисто гальванизируют перед покраской. С внутренней стороны их иногда покрывают пластиком.
Как открывали металлы
Вероятно, люди узнали, как получить металлы, случайно, когда металлы выделялись из минералов при нагревании их в печах с древесным углем. Чистый металл выделяется из соединения при реакции восстановления. На таких реакциях основано действие доменных печей. Около 4000 г. до н.э. Шумеры (узнайте больше в статье «Повседневная жизнь Шумеров«) делали золотые, серебряные и медные шлемы и кинжалы. Раньше всего люди научились обрабатывать медь, золото и серебро, т.е. благородные металлы, поскольку они встречаются в чистом виде. Около 3500 г. до н.э. шумеры научились делать бронзу — сплав меди и олова. Бронза прочнее благородных металлов. Железо было открыто позднее, так как для извлечения его из соединений нужны весьма высокие температуры. На рисунке справа изображены бронзовый топор (500 г. до н.э.) и шумерская бронзовая чаша.
До 1735 г. люди знали всего несколько металлов: медь, серебро, золото, железо, ртуть, олово, цинк, висмут, сурьму и свинец. Алюминий был открыт в 1825 г. В наши дни ученые синтезировали ряд новых металлов, облучая в ядерном реакторе атомы урана нейтронами и другими элементарными частицами. Эти элементы нестабильны и очень быстро распадаются.
www.polnaja-jenciklopedija.ru
Медный блеск - Большая Энциклопедия Нефти и Газа, статья, страница 1
Медный блеск
Cтраница 1
Медный блеск 550 Медный колчедан 42 - 8, 550 Медный купорос 372, 554 Мезоморфизм 160 Мел 462 Мельхиор 554 Менделевий см. Актиноиды Металлы 139 ел. [1]
Минерал медный блеск содержит 79 87 % меди и 20 13 % серы. [2]
Халькозин ( медный блеск) занимает третье место по содержанию меди - 79 86 % ( первое - медь самородная, второе - куприт - 88 82 %), но по распространенности и экономическому значению несколько уступает только халькопириту и борниту. [3]
Окисленные медные руды ( медный блеск, лазурит, малахит) с содержанием меди от 15 до 45 % брикетировали с добавками глины, слабо обжигали, после чего выщелачивали раствором Ре2 ( 8О4) з и подвергали электролизу со свинцовыми анодами. Отработанный раствор, обогащенный кислотой, вновь возвращался на выщелачивание. [4]
ХАЛЬКОЗИН - минерал, медный блеск Cu2S с примесями железа, серебра, кобальта, никеля, свинца, золота и др. X. [5]
Темно-коричневый кристаллический пооошок с медным блеском, технический продукт светло-коричневый, температура плавления 225 - 230 С, давление паров меньше 5 - 10 - 7 мм рт. ст. при 20 С, почти нерастворим в воде, растворяется в ацетоне, бензоле, хлорбензоле, этиловом и метиловом спирте, хлороформе и диок-сане. Быстро разрушается под воздействием сильных и слабых щелочей, концентрированных кислот. Слабые кислоты разрушают препарат только при нагревании. [6]
Это коричнево-фиолетовое твердое вещество с медным блеском, нерастворимое в неокисляющих минеральных кислотах, но растворимое в концентрированной азотной кислоте; при этом молибден окисляется до состояния VI. [7]
Природный сульфид меди ( I) - медный блеск - применяется в металлургии для получения металлической меди. [8]
Соответствующие реакции объясняют миграцию меди и образование медного блеска. [9]
Какие из медных руд: медный колчедан, медный блеск, красная медная руда - наиболее богаты медью. [10]
Самыми распространенными сульфидными рудами являются медный колчедан, медный блеск и др. Все медные руды являются бедными и обычно содержат 1 - 2 %, иногда меньше 1 % меди. [12]
Марковникова правило 255 Массовое число 32 Материя 5 Медный блеск 396 Медный колчедан см. Халькопирит Медь 396 и ел. [13]
При повторном использовании медной проволоки последнюю очищают до медного блеска. По истечении указанного срока определяют тангенс угла диэлектрических потерь. [14]
Иодинин - пигмент сине - фиолетового цвета с медным блеском - образуется при культивировании Ps. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
| Наименование группы лома цветного металла | Категории лома цветных металлов | Характеристики лома цветных металлов | Процент засора, базовый процент |
| МЕДНАЯ ГРУППА ЛОМА | Микс медь | Медный микс, это вид лома цветных металлов, который состоит преимущественно из меди, любых размеров, форм, в любом состоянии, допускаются следы коррозии и окисла, допускаются примеси изделий латуни — не более половины процента от общего веса, краски, лаков. Например, все домашние медные изделия лампы, элементы нагревательных приборов, трубки, провода, детали приборов, медные батареи, старые медные газовые колонки и луженая медь. | Минимальный или базовый засор 0,5% — этот процент может быть изменен в зависимости от качеств а- на лом медных радиаторов засор ставят от 25%, на газколонки 1%, луженая медь 6 % |
| Кусок Медь | Кусковая медь это различный медный лом толщина которого свыше 2мм, а размер не менее 5х5 см, в данной категории не разрешены остатки краски и лака, клеммы, наконечники, следы пайки и изоляции. Разрешен измененный цвет пленки и следы термической обработки. | Базовый засор не ставится | |
| Блеск Медь | Уже из названия понятны требования к этому виду лома меди — это отсутствие следов коррозии, затемнений, без следов грязи, лака, краски, термической обработки, масла и бумаги. Так же не должно быть остатков наконечников, клемм, различной пайки, оплавки – в общем, это медный кабель яркого, блестящего цвета с жилами от 1,5 до 5мм. | Минимальный засор не ставится | |
| Медь Тонкий блеск | Тонкий блеск – вид медного лома из проводников толщиной 0,5-1,5мм длиной от 30 см, которые уложены жгутом, требования такие же как и у Блеск-меди. | Минимальный засор не ставится | |
| Механическая Медь | Подвид медной группы лома, включающей в себя жилы от 0,5мм, трансформаторные шины любой толщины и проводники уложенные жгутами длиной от 30см, все они должны быть очищены механическим путем, без засоров в виде клемм, лаков, красок, без следов коррозии, без оплавленных концов, без остатков изоляции. Разрешается потемнение поверхностной пленки. | Минимальный засор не ставится | |
| Медь Масло | Это медный кабель механически очищенный с толщиной каждой жилы свыше 2мм. Требования к чистоте лома такие же как и выше – без окислов, следов краски, лака, полуды, бумаги, золы, грязи, без клемм и оплавленных концов, без следов изоляции, в масле. | Минимальный засор от 2%, может быть увеличен до 10% по результату оценки чистоты и внешнему виду лома. | |
| Медь Отожженная | Это лом медных проводников, прошедшие термическую обработку, каждая жила от 1 мм, не разрешены остатки масла, наконечников, изоляции, полуды. Не допустимы изменения цвета в результате коррозии. | Базовый засор на отожженную медь выставляется от 0,5% | |
| Микс бронзы | Бронза микс – это лом в составе которого меди свыше 70%. Как правило приемка в два этапа, сначала отдают на химический анализ по акту ответ.хранения, а затем, после результатов экспертизы уже происходит непосредственно сама приемка | Базовый засор на покрашенный бронзовый лом 1% | |
| Латунь микс | Этот вид медесодержащего лома состоит из любых бронзовых и латунных сплавов, изделий и деталей с допустимыми следами термообработки, разрешены следы краски, лака, полуд. Как правило это различные латунные сантехнические изделия и их лом, различные латунные трубки. | Базовый засор на латунный микс от 1% и может быть увеличен по результату оценки чистоты и внешнему виду лома. | |
| Латунные радиаторы | Вкратце это батареи отопления с медными пластинами, имеющими в своей конструкции латунные трубки. Разрешен следы пайки. Не допускаются следы черных металлов. | Минимальный засор на радиаторы из латуни выставляется от 1%, может быть увеличен до 4% по результату оценки чистоты и внешнему виду лома. | |
| Алюминиевая группа, лом цветного металла, имеющего в составе алюминий | Микс | Это лом цветного металла, имеющего в своем составе алюминий. Сюда относятся любые изделия за минусом цинкосодержащих. Разрешены остатки пластика, креплений, железа, главное, что их вес не должен быть выше 5% от общей массы сдаваемого алюминиевого лома | Базовый засор на алюминиевый микс от 2% и может быть увеличен по результату оценки чистоты и внешнему виду лома. |
| Профиль | Уже из названия понятно, что сюда относятся алюминиевые изделия, из сплавов марки АД. Требования намного выше, чем в предыдущей категории алюминиевого лома, так например разрешены следы краски, но запрещены любые составляющие, т.е. никаких деревянных, пластиковых крепежей ручек | Минимальный засор ставится от 2% вне зависимости от качества и внешнего вида. Однако, на пластиковые термовставки засор выставляется минимум 17% | |
| Силумин | Категория Алюминий силумин – характеризуется в первую очередь по методу изготовления, это отливка. Сюда относятся все станины, изделия, конструкции, изготовленные этим методом. Разрешены остатки пластика, креплений, железа, главное, что их вес не должен быть выше 5% от общей массы сдаваемого алюминиевого лома | Базовый засор на алюминиевый лом категории силумин ставится 2-5% по результату оценки чистоты и внешнему виду лома. | |
| Электротехнический | Часто еще именуют категорию Электротех – это кабеля и провода из алюминия, их необходимо разделать механическим способом от оплетки, клемм, наконечников, очистить от следов краски и других включений. Разрешены следы масла, затемнения. лом алюминиевого проводника из кабеля, разделанного механическим способом. Не допускается наличие клемм (наконечников), остатков изоляции, краски, неметаллических включений. | Минимальный засор на электротехнический алюминиевый лом не ставится. 2 — 5% в зависимости от чистоты и внешнего вида. | |
| Пищевой | Иногда можно встретить название этой категории как бытовой алюминиевый лом, как правило это различная посуда, сушилки, ложки, тарелки, предметы обихода и интерьера, главное требование они должны быть изготовлены методом давления и гибки, но не отливки как в категории силумин, т.е. те же домашние казаны сюда не относятся. Пищевой алюминиевый лом не должен иметь в своем составе железо, дерево, бумагу, тефлоновое покрытие, так же нужно удалить крепежи и пластик. | Засор ставится 2% и не зависит от чистоты и внешнего вида | |
| Шина | Лом алюминиевой шины это проводники, применяемые при монтаже кабеля. Его нужно очистить механически от оплетки, железа и алюминиевых сплавов, удалить все клеммы. Разрешено потемнение, маслянные следы, остатки краски. | Засор до 2%, базовый не выставляется | |
| Цинк | Цинковые сплавы, ЦАМ | Можно его отнести к категориям алюминиевого лома, но в целом, лучше отдельно характеризовать. Сюда относятся цинксодержащие сплавы и изделия из них, например детали смесителей, ручки от старых холодильников, карбюраторы. Нет жестких требований по приему ЦАМ, можно и следы пластика, и других неотъемлемых частей конструкции, главное что бы их вес не превышал 5 % от общего веса к цинкового лома. | Засор 2 — 5% в зависимости от чистоты и внешнего вида. Минимальный 2 %. |
| Свинцовая группа | Аккумуляторные батареи (АКБ) | К свинцовой группе лома относятся классические батарейки и аккумуляторы допускается протекший электролит или вовсе без него. Щелочные акб принимаются поштучно. | Минимальный засор не ставится |
| Оплетка | У многих кабелей имеется свинцовая оплетка, она так же может стать предметом сдачи лома. Эта свинцовая оплетка должна быть разделана механически, но требования не строгие на ней могут быть засоры в виде бумаги, битума, масла. | Минимального засора нет, на чистую оплетку как правило нет засора, если есть следы масла тогда засор 3%, смола 5% смола+бумага или картон 8%. В зависимости от степени загрязнения засор может быть увеличен до 15% | |
| Переплав | Лом цинксодержащий в категории переплав, примерно тоже самое, что и микс, нет требований к качеству и чистоте лома, он может быть с пластмассой, древесиной, включениями из других металлов. | Минимальный засор на Переплав не ставится, все зависит от чистоты и качества сдаваемого лома. |
mednic.ru
Медный блеск - Справочник химика 21
Справочник химика 21
Химия и химическая технология
Медный блеск
Окисленные медные руды (медный блеск, лазурит, малахит) с содержанием меди от 15 до 45% брикетировали с добавками глины, слабо обжигали, после чего выщелачивали раствором Ре2(804)з и подвергали электролизу со свинцовыми анодами. Отработанный раствор, обогащенный кислотой, вновь возвращался на выщелачивание. [c.219]
ХАЛЬКОЗИН — минерал, медный блеск СиаЗ с примесями железа, серебра. кобальта, никеля, свинца, золота и др. X. имеет окраску от свинцово-серой до черной, применяют как медную руду. [c.272]
Получение. Процесс получения меди весьма сложный. Упрощенно процесс ее производства из медного блеска отразить можно так [c.105]
Природные ресурсы. Содержание в земной коре составляет Си 4,7-10-3%, Agl-10-5%, Au 5-10-8%. g e рассматриваемые металлы встречаются в свободном состоянии. Наиболее крупные медные, самородки имеют массу сотни килограммов, золотые — десятки килограммов. Медь, в основном, находится в виде сулЬфидных руд. Главные минералы, содержащие медь халькопирит uFeSa, халькозин (медный блеск) U2S, ковеллин uS, малахит Си2(ОН)2СОз. Самородное серебро встречается редко. Ag находится, главным образом, в виде сульфидных минералов (аргентит — серебряный блеск Ag S и др.), которые обычно содержатся как примесь в полиметаллических рудах (спутники Си, Ni, РЬ). Золото, наоборот, встречается преимущественно в самородном состоянии в виде вкраплений в кварц. Продуктом разрушения таких пород является золотоносный песок. Золото, так же как и серебро, бывает примесью в полиметаллических рудах. но содержание в них Аи меньше, чем Ag. [c.581]
Затем оксид меди (I) вступает в реакцию с оставшимся медным блеском — получается медь [c.106]
Оче[1ь распрост 1анены соединения серы с различгсыми металлами. Многие из них являются цепными рудами (иапример, свинцовый блеск РЬ5, цннковая обманка 2п5, медный блеск Си23), и служат источником получения цветных металлов. [c.380]
Важнейшими минералами, входящими в состав медных руд, являются халькозин. или медный блеск, LI2S халькопирит. или медный колчедан. uFeSj малахит (СиОН)2СОз. [c.570]
Относительное число атомов каждого элемента в сэедннении указывается его химической формулой. Например, минерал халькозин. медный блеск или сульфид меди (1), содержит по два атома меди на калщнй атом серы. Эти сведения полезны при определении количества меди, содержащегося в том или ином образце ее соединения с известной химической )ормулой. [c.148]
Важнейшими минералами, входящими в состав медных руд, являются халькозин. или медный блеск, СигЗ халькопирит. или медный колчедан. uFeSa малахит Си(СОз)(ОН)2. В России богатые месторождения медных руд находятся на Урале. [c.534]
Природные ресурсы. Содержание в земной коре составляет Си 4,7 10 %, Ag 7 10 %, Au S 10 %. Медь в основном находится в земной коре в виде сульфцдных руд. Главные минералы, содержащие медь халькопирит СиРеЗг. халькозин (медный блеск) ujS, ковеллин uS, малахит u2(OH)2 Oj. Встречается (но редко) самородная медь. Наиболее крупные медные самородки имеют массу в сотни килограммов. [c.551]
К физическим способам относятся такие методы, как гравитационный, основанный на различии в плотностях руды и пустой породы. и флотационный. Метод флотации связан с различной смачиваемостью поверхности зерен руды и пустой породы водой, содержащей поверхностно-активные вещества. Например, частицы руды — медный блеск ujS лучше, чем частицы пустой породы. адсорбируют на себе пузырьки пены, образованной воздухом, продуваемым через воду с сосновым маслом. В результате этого они вместе с пеной всплывают (флотируют) на поверхность, а пустая порода тонет. Сливая с поверхности пену с налипшими частицами руды и отжав из них флотоаг ент, получают концентрат руды, в котором содержание металла увеличено в несколько раз (для медй — до 16—22%), Используется и магнитный способ обогащения руд, основанный на разделении минералов по их магнитным свойствам. [c.293]
Нахождение в природе. Медь встречается в самородном состоянии в небольших количествах, но чаще она бывает в виде кислородных соединений куприт СозО, мелаконит СиО сернистых — медный блеск 038 углекислых (основных) — малахит СиСОд Си (0Н)2, азурит 2СиСОз- [c.396]
Важнейшие руды-сульфиды железный, или серный, колчедан (пирит) РеЗа, медный блеск СизЗ, свинцовый блеск РЬ8, цинковая обманка 2п5, серебряный блеск Ag2S, киноварь HgS. [c.261]
Массовое число атома 61 Медный блеск 362 Мел 285. Иельхиор 282 [c.705]
Учебник общей химии (1981) -- [ c.412 ]
Неорганическая химия (1981) -- [ c.417 ]
Общая химия в формулах, определениях, схемах (1996) -- [ c.396 ]
Общая химия в формулах, определениях, схемах (0) -- [ c.396 ]
Курс аналитической химии Том 1 Качественный анализ (1946) -- [ c.148 ]
Общая химия в формулах, определениях, схемах (1985) -- [ c.396 ]
Общая химия в формулах, определениях, схемах (0) -- [ c.396 ]
Минеральные кислоты и основания часть 1 (1932) -- [ c.82. c.199 ]
Очерк общей истории химии (1969) -- [ c.41 ]
Неорганическая химия (1950) -- [ c.317 ]
Общая и неорганическая химия (1981) -- [ c.581 ]
Неорганическая химия (1981) -- [ c.417 ]
Неорганическая химия (1978) -- [ c.418 ]
Неорганическая химия (1950) -- [ c.257 ]
Лекционные опыты и демонстрации по общей и неорганической химии (1976) -- [ c.157. c.196 ]
Технология серной кислоты и серы Часть 1 (1935) -- [ c.36 ]
Курс технологии минеральных веществ Издание 2 (1950) -- [ c.37 ]
Общая химия Издание 18 (1976) -- [ c.563 ]
Вредные неорганические соединения в промышленных выбросах в атмосферу (1987) -- [ c.84 ]
ПОИСК
http://chem21.info
legkoe-delo.ru
Металлы
Металлы
- Положение металлов в ПСХЭ и строение их атомов.
В Периодической системе Д. И. Менделеева каждый период, кроме первого, начинается с активного химического элемента-металла. Эти начальные элементы образуют главную подгруппу 1 группы ( их атомы содержат на внешнем уровне 1 электрон) и называются щелочными металлами.
В соответствии с ростом радиуса атома восстановительные свойства щелочных металлов усиливаются от лития к францию.
Следующие за щелочными металлами элементы, составляющие главную подгруппу 2 группы, также являются типичными металлами, обладающими сильной восстановительной способностью (их атомы содержат на внешнем уровне 2 электрона). Из этих металлов кальций, стронций, барий и радий называют щелочноземельными металлами.
К металлам относят и элементы главной подгруппы 3 группы, исключая бор. Элементы главной подгруппы 4 группы: германий, олово, свинец. Элементы главной подгруппы 5 группы: сурьма и висмут. Элементы главной подгруппы 6 группы: полоний.
Побочные подгруппы образованы только элементами-металлами.
Характерное химическое свойство всех металлов - их восстановительная способность, т. е. способность атомов легко отдавать внешние электроны, превращаясь в положительные ионы. Металлы не могут присоединять к себе электроны.
- Физические свойства металлов.
Физические свойства металлов обусловлены строением металлической кристаллической решетки. В узлах решеток располагаются атомы и положительные ионы металлов, связанные посредством обобществленных внешних электронов, которые принадлежат всему кристаллу.
Твердость. Все металлы, кроме ртути, при обычных условиях – твердые вещества. Однако это свойство различно у каждого из металлов.
Плотность. Металлы делятся на легкие и тяжелые.
Плавкость. Металлы делятся на легкоплавкие и тугоплавкие.
Электрическая проводимость металлов обусловлена присутствием в их кристаллических решетках подвижных электронов, которые направлено перемещаются под действием электрического поля.
Теплопроводность металлов тоже вызвана высокой подвижностью свободных электронов: сталкиваясь с колеблющимися в узлах решетки ионами, электроны обмениваются с ними энергией.
Металлический блеск – результат отражения световых лучей от электронов, находящихся в межатомном пространстве.
Пластичность металлов обусловлена тем, что под внешним воздействием одни слои ион - атомов в кристаллах легко смещаются, как бы скользят, по отношению к другим без разрыва связей между ними.
Некоторые металлы обладают звуком.
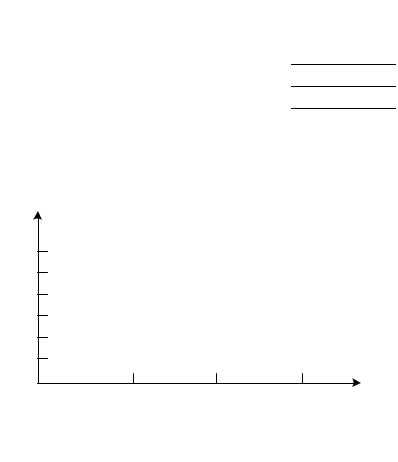
Физические свойства металлов.
|
Металлы |
Твердость |
Плотность г/cm3 |
Температура плавления гр.С |
|
1.Натрий |
0,4 |
0,97 |
98 |
|
2.Калий |
0,5 |
0,86 |
63,5 |
|
3. Свинец |
1,5 |
11,34 |
328 |
|
4.Олово |
1,8 |
7,30 |
232 |
|
5.Магний |
2,1 |
1,74 |
651 |
|
6.Кальций |
2,2 |
1,54 |
851 |
|
7.Золото |
2,5 |
19,3 |
1063 |
|
8.Цинк |
2,5 |
7,14 |
419 |
|
9.Серебро |
2,7 |
10,5 |
961 |
|
10.Алюминий |
2,9 |
2,70 |
660 |
|
11.Медь |
3 |
8,9 |
1083 |
|
12.Железо |
4 |
7,87 |
1539 |
|
13.Платина |
4,3 |
21,45 |
1755 |
|
14.Никель |
5 |
8,9 |
1452 |
|
15.Вольфрам |
7 |
|
3370 |
|
16.Ртуть |
- |
13,6 |
-39 |
- Сплавы.
Сплавы – это материалы с характерными свойствами, состоящие из двух или более компонентов, из которых один металл. По состоянию компонентов сплавы могут быть однородными, когда при сплавлении образуется как бы раствор одного металла в другом, и неоднородными, представляющими собой механическую смесь металлов.
Представители сплавов:
Бронза-сплав меди с другими элементами, в основном металлами. В зависимости от состава различают: оловянную бронзу, алюминиевую бронзу, свинцовую бронзу, кремниевую бронзу. Применяют для изготовления частей машин и для художественных отливок.
Латунь-сплав меди с цинком. Обладает высокой пластичностью. Используют для изготовления приборов, деталей машин, предметов домашнего обихода.
Баббиты-сплавы, уменьшающие трение, изготовляются на основе олова или свинца с добавками сурьмы, меди и других металлов. Применяют для заливки подшипников
Нихром-сплав никеля, хрома, железа и марганца, обладает большим электрическим сопротивлением и жаропрочностью, поэтому его применяют для изготовления электрических нагревательных приборов.
Припой «третник»- легкоплавкий сплав, состоит из олова и свинца. Используют при паянии.
Победит-сплав углерода, вольфрама, кобальта. По твердости он близок к алмазу, применяют в металлообработке и при бурении горных пород.
Дюралюминий-сплав алюминия, магния, меди и марганца. Очень прочный и легкий сплав. По прочности он равен стали, но в три раза легче её. Применяют в самолетостроении.
Мельхиор-сплав, состоящий из меди и никеля, похож по внешнему виду на серебро. Используется для изготовления недорогих столовых и художественных изделий.
Чугун-сплав на основе железа, углерода, марганца, кремния, фосфора, серы. Применяется для изготовления массивных деталей.
Сплав из олова и индия используют для спайки стекла и металла.
Сплавы рения с танталом и вольфрамом - самые жаростойкие из всех известных.
Легкие сплавы на основе титана сохраняют прочность и коррозийную устойчивость при повышенных температурах и давлениях. Из них изготавливают отдельные части реактивных двигателей, корпуса атомных подводных лодок.
4.Химические свойства металлов.
Электрохимический ряд напряжения металлов
Li, K, Ba, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Co, Sn, Pb, (H), Cu, Hg, Ag, Au
4.Общие свойства металлов
- Взаимодействие с кислородом воздуха:
А) легко взаимодействуют щелочные и щелочноземельные металлы, быстро окисляются при обычной температуре;
Б) менее активные металлы медленно окисляются при обычной температуре или при нагревании;
В) золото, медь, серебро и платиновые металлы не окисляются ни при каких условиях.
- Взаимодействие с водой.
А) щелочные и щелочноземельные металлы легко реагируют с водой при обычной температуре с выделением водорода и образованием гидроксида;
Б) менее активные металлы взаимодействуют с водой только в раскаленном виде с выделением водорода и образованием оксида.
- Взаимодействие с неметаллами.
А) с галогенами;
Б) с серой;
В) с азотом;
Г) с углеродом;
Д) с водородом.
- Взаимодействие с кислотами.
А) металлы, стоящие в ряду напряжений левее водорода, вытесняют его из растворов кислот, кроме щелочных металлов;
Б) металлы, стоящие правее водорода с кислотами не реагируют, растворяются в «царской водке» ;
В) реакция идет, если в реакции металла с кислотой образуется растворимая соль;
Г) концентрированная серная кислота и азотная кислота любой концентрации реагирует с металлами по-особому, при этом водород не образуется.
- Взаимодействие с солями.
А) каждый металл вытесняет из растворов солей другие металлы, находящиеся правее него в ряду напряжений, и сам может быть вытеснен металлами, расположенными левее;
Б) реакция идет при образовании растворимой соли;
В) правило не распространяется на щелочные металлы.
5.Получение металлов.
Металлы в природе могут встречаться в трех формах:
1. Только в свободном виде встречаются золото и платина;
2. И в самородном виде, и в форме соединений могут находиться в природе серебро, медь, ртуть, олово;
3. Все остальные металлы, которые находятся в ряду напряжений до Sn, встречаются в природе только в виде соединений:
- хлоридов;
- нитратов;
- сульфатов;
- карбонатов;
- силикатов;
- сульфидов;
- фосфатов и апатитов.
Способы получения.
- Пирометаллургия- восстановление металлов из руд при высоких температурах с помощью восстановителей (углерода, оксида углерода (2), водорода, металлов - алюминия, магния).
- Гидрометаллургия - методы получения металлов, основанные на химических реакциях, происходящих в растворах.
- Электрометаллургия - методы получения металлов, основанные на электролизе, т. е. выделении металлов из растворов или расплавов их соединений при пропускании через них постоянного электрического тока.
- Коррозия металлов.
Коррозией называется самопроизвольное разрушение металлов и сплавов под влиянием окружающей среды. Коррозия вызывает серьезные экологические последствия.
Виды коррозии:
- Химическая коррозия металлов – это разрушение металлов в результате их химического взаимодействия с веществами окружающей среды (вода, кислород, оксиды углерода и серы, водные растворы солей).
- газовая коррозия;
- кислородная коррозия;
- водородная коррозия.
- Электрохимическая коррозия – это разрушение металлов, которое сопровождается возникновением электрического тока.
По характеру разрушения:
- Сплошная коррозия – распределяется равномерно по всей поверхности металла или сплава.
- Местная коррозия – её очаги распределяются неравномерно - в виде коррозийных пятен или точек.
- Коррозийная язва или питтинг – глубокое поражение материала с небольшой внешней поверхностью разрушения.
- Интеркристаллитная коррозия – распространяется по границам кристалла в глубь металла.
- Экстрактивная коррозия – это удаление одного из компонентов сплава.
Способы защиты от коррозии:
- Нанесение защитных покрытий на поверхности предохраняемого от коррозии металла.
- Использование нержавеющих сталей, содержащих специальные добавки.
- Введение в рабочую среду ингибиторов.
- создание контакта с более активным металлом – протектором.
Тестовая система « Проверь себя».
А 1. Сравнивая элементы In, Sn, Sb, Te, можно заметить, что металлические свойства преобладают у…
1) In 2) Sn 3) Sb 4) Te
А 2. В ряду Na – K – Rb химическая активность металлов:
1) увеличивается от Na к Rb
2) уменьшается от Na к Rb
3) не изменяется
4) увеличивается от Na к К, а затем уменьшается
А 3. По сравнению с третьей, в четвертой группе Периодической системы…
1) количество металлов должно увеличиваться
2) количество металлов должно уменьшаться
3) количество металлов не должно изменяться
4) количество неметаллов должно уменьшаться
А 4. Справедливо следующее утверждение…
1) в первой группе Периодической системы есть только неметаллы
2) все периоды Периодической системы содержат металлы
3) все элементы побочных подгрупп Периодической системы – металлы
4) металлы содержатся только в главных подгруппах Периодической системы
А 5. Пара металлов, обладающих наиболее сходными свойствами:
1) Al и Na 2) Ca и Zn 3) K и Na 4) Mn и Mg
А 6. Верно следующее утверждение: Фторид калия…
1) имеет молекулярное строение
2) имеет металлическое строение
3) имеет атомное строение
4) имеет ионное строение
А 7. Латунь является сплавом металлов меди и цинка. Верно следующее утверждение…
1) латунь – это соединение меди с цинком, состав которого можно определить по валентности
2) латунь- это сложное вещество, которому соответствует формула CuZn
3) в составе латуни оба элемента сохраняют свои химические свойства
4) в составе латуни цинк образует положительные, а медь отрицательные ионы
А 8. Металлы, с которых начинается ряд активности металлов (до Al),…
1) встречаются в природе в виде самородных металлов
2) образуют природные залежи оксидов и сульфидов
3) не образуют природных залежей
4) чаще всего встречаются в виде солей
А 9. При взаимодействии кальция с водой происходит образование:
1) оксида кальция
2) гидроксида кальция и водорода
3) гидроксида кальция
4) оксида кальция и водорода
А 10. В реакциях взаимодействия с водой металлы…
1) выступают в качестве окислителей
2) выступают в качестве восстановителей
3) могут быть как окислителями, так и восстановителями
4) не могут проявлять ни окислительных, ни восстановительных свойств
А 11. В ряду активности металлы от Li до Pt расположены в порядке:
1) увеличения зарядов ионов этих металлов
2) усиления окислительных свойств
3) ослабления восстановительных свойств
4) усиления восстановительных свойств
А 12. Вытесняют водород из кислот оба металла:
1) Cu и Hg 2) Ag и Cu 3) Fe и Hg 4) Fe и Cr
А 13. Реакция замещения возможна:
1) между серебром и железом
2) между хлоридом железа (2) и серебром
3) между нитратом меди (2) и серебром
4) между нитратом серебра и железом
А 14.При непосредственном контакте железных и медных деталей…
1) медь подвергается интенсивной коррозии
2) оба металла разрушаются быстрее, чем при отсутствии контакта
3) происходит окисление меди железом
4) железо разрушается быстрее, чем медь
А 15. Среди оксидов калия, кальция, меди и цинка наиболее выраженными основными свойствами обладает:
1) оксид меди 2) оксид калия 3) оксид цинка 4) оксид кальция
А 16. Растворяются в щелочах:
1) оксид и гидроксид меди
2) оксид и гидроксид магния
3) оксид и гидроксид алюминия
4) оксид и гидроксид железа (2)
А 17. Ионы алюминия (3+) можно обнаружить, добавляя к исследуемому раствору:
1) щелочь 2) гидроксид алюминия 3) кислоту 4) воду
А 18. Металлический алюминий получают:
1) восстановлением оксида железом
2) обжигом руды, содержащей алюминий
3) электролизом растворов солей
4) электролизом расплава оксида
А 19. Сущностью процесса получения железа из руды является:
1) расплавление железа
2) окисление железной руды
3) восстановление окисленного железа
4) восстановление кокса и известняка
А 20. При взаимодействии калия с водой происходит образование:
1) оксида калия
2) гидроксида калия и водорода
3) гидроксида калия
4)оксида калия и водорода
Занимательные опыты.
- Как звучат металлы.
На длинный женский волос подвесьте золотое кольцо, серебряное кольцо, медное кольцо (или любой медный предмет), деревянной палочкой ударьте поочередно по кольцам и вы услышите, как звучат металлы.
- «Алхимическое золото»
Налить в два стакана по 100 мл воды. В одном стакане растворить 8 г KI, в другом 8 г Pb(CH 3 COO)2 и слить эти растворы. Образуется желтый осадок. Дать отстояться, затем жидкость над осадком слить, а к осадку добавить 10 мл 4%-ый Ch4 COOH и довести раствор до кипения. Добавлять воду до тех пор, пока осадок не растворится. Стакан с горячим раствором перенести на демонстрационный стол и осветить лампой на фоне черного экрана. Видно, что в стакане выпали желтые кристаллы PbI2 . Кристаллов выпадает тем больше, чем медленнее мы будем охлаждать раствор.
- Растворение золота
Берем старый черепок тарелки с золотой каймой и проводим следующий опыт: наносим на него каплю соляной кислоты. Ничего не происходит. Наносим каплю «царской водки» - капля растворяет золотой ободок
- «Медная шуба».
В раствор 10%-го сульфата меди помещается фигурка человечка, вырезанная из цинка.
- «Фейерверк».
(Для опыта необходимо смешать равные количества перманганата калия, порошка железа и древесного угля. Насыпать смесь в металлический наперсток и внести его в пламя спиртовки.)
Желаем удачи !
skolniki.narod.ru